名校
1 . 氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物性质描述错误 的是


| A.均可以与磷酸反应形成离子化合物 |
| B.可用红外光谱区分,但不能用核磁共振氢谱区分 |
C.与足量的 发生加成反应后,分子的手性碳原子数均发生了改变 发生加成反应后,分子的手性碳原子数均发生了改变 |
| D.羟基氯喹比氯喹的水溶性更好,在人体胃肠道吸收更快 |
您最近一年使用:0次
2 . 一种重要的降血糖药物M(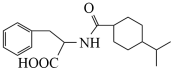 )的合成路线如下(略去部分反应条件):
)的合成路线如下(略去部分反应条件):
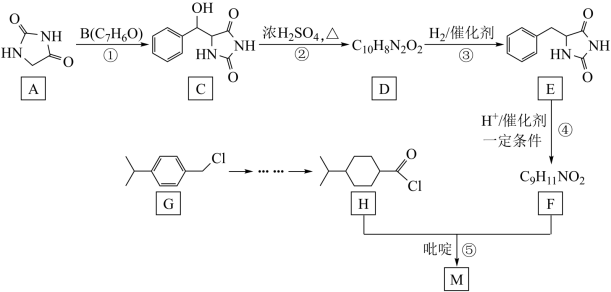
已知: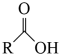
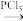
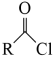
回答下列问题:
(1)B的名称为________ ,F的结构简式为________ 。
(2)反应②的反应类型为________ 。
(3)下列关于上述涉及的有机物的说法正确的是________ (填标号)。
a.化合物E能使酸性高锰酸钾溶液褪色
b.化合物F既能与盐酸反应,又能与 溶液反应
溶液反应
c.M中含氧官能团的名称为酯基、酮基
(4)写出 的化学方程式:
的化学方程式:________ 。
(5)由G可制得物质I( ),写出满足下列条件的I的同分异构体的结构简式:
),写出满足下列条件的I的同分异构体的结构简式:________ 。
①能与 溶液发生显色反应
溶液发生显色反应
②除苯环外不含其他环
③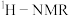 谱中峰面积之比为
谱中峰面积之比为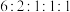
(6)请设计以G为原料合成H的合理路线流程图(无机试剂任选)。_______________
 )的合成路线如下(略去部分反应条件):
)的合成路线如下(略去部分反应条件):
已知:

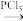

回答下列问题:
(1)B的名称为
(2)反应②的反应类型为
(3)下列关于上述涉及的有机物的说法正确的是
a.化合物E能使酸性高锰酸钾溶液褪色
b.化合物F既能与盐酸反应,又能与
 溶液反应
溶液反应c.M中含氧官能团的名称为酯基、酮基
(4)写出
 的化学方程式:
的化学方程式:(5)由G可制得物质I(
 ),写出满足下列条件的I的同分异构体的结构简式:
),写出满足下列条件的I的同分异构体的结构简式:①能与
 溶液发生显色反应
溶液发生显色反应②除苯环外不含其他环
③
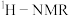 谱中峰面积之比为
谱中峰面积之比为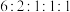
(6)请设计以G为原料合成H的合理路线流程图(无机试剂任选)。
您最近一年使用:0次
2020-07-15更新
|
926次组卷
|
4卷引用:山东省2019-2020学年高二下学期第二次联合考试化学试题
山东省2019-2020学年高二下学期第二次联合考试化学试题青海省海东市2019-2020学年高二下学期期末联考化学试题(已下线)2021年高考化学押题预测卷(新课标Ⅲ卷)(02)(含考试版、答题卡、参考答案、全解全析)辽宁省鞍山市2020-2021学年高二下学期期末考试化学试题
名校
解题方法
3 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
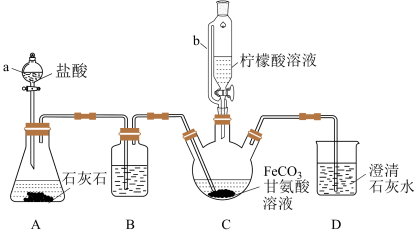
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
名校
4 . 下列各物质,既能与NaOH溶液反应,又能与稀HNO3反应,还能够水解的是
①Al2O3;②对羟基苯甲酸钠;③酶;④纤维素;⑤甘氨酸;⑥KHSO3;⑦Al(OH)3;⑧NH4I;⑨硬脂酸钠;⑩(NH4)2CO3
①Al2O3;②对羟基苯甲酸钠;③酶;④纤维素;⑤甘氨酸;⑥KHSO3;⑦Al(OH)3;⑧NH4I;⑨硬脂酸钠;⑩(NH4)2CO3
| A.②③⑥⑧⑩ | B.①③⑤⑥⑦⑩ | C.①②③⑤⑦⑨⑩ | D.全部 |
您最近一年使用:0次
2020-08-28更新
|
911次组卷
|
3卷引用:黑龙江省哈尔滨师范大学附属中学2019-2020学年高二下学期期末考试化学试题
5 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是一种用于治疗缺铁性贫血的药物,用下图装置可以在实验室中制备甘氨酸亚铁:

有关物质性质如下表所示:
实验步骤如下:
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是___________ ,d的作用是___________ 。
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭___________ 打开___________ (填“K2”或“K3”);步骤Ⅱ中若调节溶液pH偏高,则所得粗产品中会混有杂质___________ (写化学式)。
(3)c中生成甘氨酸亚铁的化学方程式是___________ 。
(4)下列关于该实验的说法正确的是___________ (填字母)。
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:_______ 。
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是_______ (填字母)。
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失

有关物质性质如下表所示:
| 甘氨酸(H2NCH2COOH) | 易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中溶解度大于在乙醇中的溶解度。 |
| 柠檬酸 | 易溶于水和乙醇,酸性较强,有强还原性。 |
| 甘氨酸亚铁 | 易溶于水且在水中难电离,难溶于乙醇、冰醋酸。 |
Ⅰ.打开K1、K3,向c中通入气体,待确定c中空气被排尽后,将b中溶液加入到c中。
Ⅱ.在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加适量NaOH溶液调溶液pH至5.5左右,使反应物充分反应。
Ⅲ.反应完成后,向c中反应混合液中加入无水乙醇,析出沉淀,将沉淀过滤、洗涤得粗产品,将粗产品纯化后得精品。
回答下列问题:
(1)仪器b的名称是
(2)步骤Ⅰ中将b中溶液加入到c中的操作是关闭
(3)c中生成甘氨酸亚铁的化学方程式是
(4)下列关于该实验的说法正确的是
a.反应混合液中加入柠檬酸的作用是防止Fe2+被氧化
b.步骤Ⅰ中可由d中导管是否还有气泡冒出来判断装置中的空气是否排尽
c.步骤Ⅲ中加入无水乙醇的作用是降低甘氨酸亚铁的溶解度
d.步骤Ⅲ中沉淀洗涤时,用蒸馏水作洗涤剂
(5)①工业上常用高氯酸(不与冰醋酸反应)标准溶液在非水体系中滴定甘氨酸的方法测定产品中的甘氨酸的含量。请设计实验,将所得粗产品中的甘氨酸分离出来直接用于滴定:
②滴定过程中下列操作会使甘氨酸的测定结果偏高的是
a.滴定时未用高氯酸标准溶液润洗滴定管
b.读数时,滴定前平视,滴定后俯视
c.摇动锥形瓶时有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后消失
您最近一年使用:0次
解题方法
6 . 某抗抑郁药物有效成分F的合成路线如图。
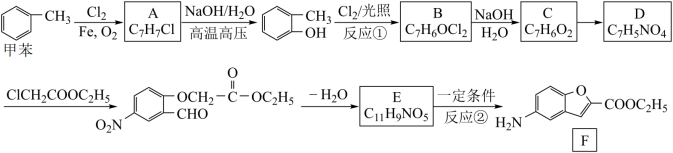
已知:①同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基
②
回答下列问题:
(1)D分子中除—CHO外的含氧官能团结构简式为_______ 。
(2)E的结构简式为_______ ;反应①的反应类型为 _______ 。
(3)反应B→C的化学方程式为_______ ;ClCH2COOC2H5加热条件下与足量NaOH反应后酸化所得的有机物发生聚合反应的化学方程式为 _______ 。
(4)化合物C中含有苯环的同分异构体有_______ 种,其中苯环上只有一个侧链且能发生银镜反应的有机物结构简式为 _______ 。
(5)下列有关F的叙述正确的是_______ 。
a.分子式为C11H10O3N
b.既能与盐酸反应生成盐,也能在NaOH反应生成盐
c.1mol F最多可以与2mol H2发生加成反应
d.既能发生加成反应也能发生取代反应

已知:①同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基
②

回答下列问题:
(1)D分子中除—CHO外的含氧官能团结构简式为
(2)E的结构简式为
(3)反应B→C的化学方程式为
(4)化合物C中含有苯环的同分异构体有
(5)下列有关F的叙述正确的是
a.分子式为C11H10O3N
b.既能与盐酸反应生成盐,也能在NaOH反应生成盐
c.1mol F最多可以与2mol H2发生加成反应
d.既能发生加成反应也能发生取代反应
您最近一年使用:0次
7 . 甘氨酸(结构如图)常作食品的调味剂,还可预防氧化、延缓衰老等。甘氨酸与酸反应生成阳离子(用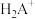 表示)。
表示)。 甘氨酸聚合成多肽,生成
甘氨酸聚合成多肽,生成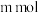 水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,
水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,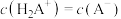 。下列叙述错误的是
。下列叙述错误的是
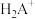 表示)。
表示)。 甘氨酸聚合成多肽,生成
甘氨酸聚合成多肽,生成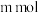 水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,
水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,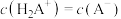 。下列叙述错误的是
。下列叙述错误的是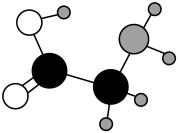
| A.甘氨酸是蛋白质水解的最终产物之一 |
| B.甘氨酸是两性化合物 |
| C.甘氨酸溶液调pH后,在等电点时显中性 |
| D.当n=m+1时合成的肽为肽链 |
您最近一年使用:0次
2023-06-27更新
|
192次组卷
|
5卷引用:吉林省白山市六所盟校2022-2023年高二下学期期未联考化学试题
吉林省白山市六所盟校2022-2023年高二下学期期未联考化学试题湖北省十堰市2022-2023学年高二下学期期末调研考试化学试题吉林省松原市前郭尔罗斯蒙古族自治县榆树实验,九台一中,前郭,农安2022-2023学年高二下学期7月期末考试化学试题吉林省两地六县重点中学2022-2023学年高二下学期期末联考化学试题(已下线)专题07 生物大分子 合成高分子-备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)
名校
8 . 我国科学家成功合成抗新冠肺炎新药Ebselen。一种合成Ebselen的流程如下(已知:氨基 具有强还原性):
具有强还原性):
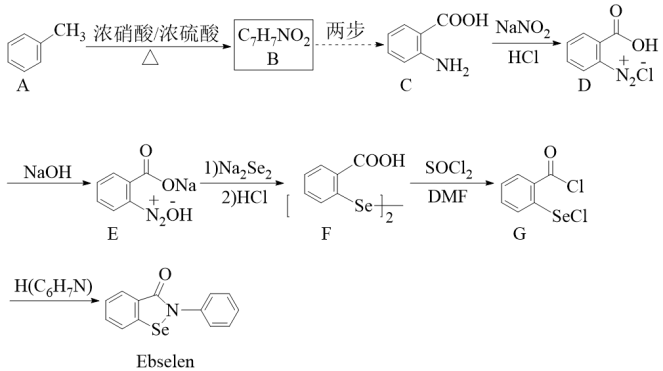
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是_______ 。H的结构简式为_______ 。
(2)一定条件下,E能与苯酚、NaOH反应生成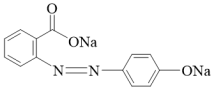 。写出该反应的化学方程式:
。写出该反应的化学方程式:_______ 。其有机反应类型是_______ 。
(3)生成G时,F中所断裂化学键是_______(填标号)。
(4)已知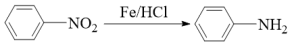 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑_______ 。
(5)在C的芳香族同分异构体中,同时具备下列条件的结构有_______ 种。
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备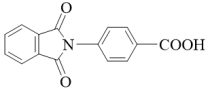 的微流程如下:
的微流程如下: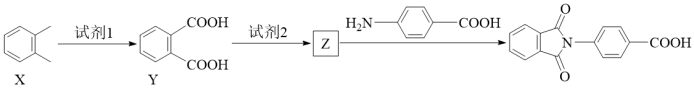
试剂2是_______ (填化学式)。
 具有强还原性):
具有强还原性):
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和
 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是(2)一定条件下,E能与苯酚、NaOH反应生成
 。写出该反应的化学方程式:
。写出该反应的化学方程式:(3)生成G时,F中所断裂化学键是_______(填标号)。
A.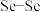 | B.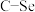 | C. | D.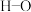 |
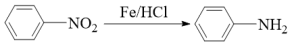 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑(5)在C的芳香族同分异构体中,同时具备下列条件的结构有
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备
 的微流程如下:
的微流程如下:
试剂2是
您最近一年使用:0次
9 . 某药物K的合成路线如图:

已知:①R1CH2COOR2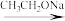
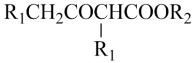
②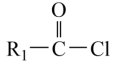

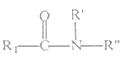
(1)下列说法正确的是____ 。
(2)I的结构简式是____ 。
(3)F→G的化学方程式为____ 。
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式____ 。
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):____ 。
CH2=CHCH3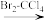 ____。
____。

已知:①R1CH2COOR2
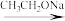
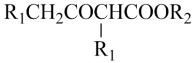
②
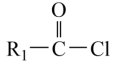


(1)下列说法正确的是
| A.1molG最多可以和3molH2发生加成反应 |
| B.化合物H既能和HCl溶液发生反应又能和NaOH溶液反应 |
| C.化合物J的分子式为C15H20N2 |
| D.K中有1个手性碳原子 |
(3)F→G的化学方程式为
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):
CH2=CHCH3
 ____。
____。
您最近一年使用:0次
名校
解题方法
10 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示(夹持和加热、搅拌仪器已省略)。
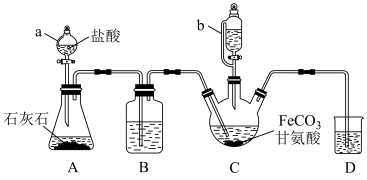
有关物质性质如下表:
实验过程:
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)装置B中盛有的试剂是_______ ;实验过程中装置D的导管需要一直浸入液面下的必要性是_______ 。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和_______ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)可以用_______ 试剂(写化学式)检验产品中是否含有Fe3+。
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是_______ 。

有关物质性质如下表:
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 |
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是
(2)装置B中盛有的试剂是
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为
(5)过程II中加入无水乙醇的目的是
(6)可以用
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是
您最近一年使用:0次



