1 . 喹啉类药物在治疗疟疾方面有广泛应用,一种喹啉类药物中间体M的合成路线如图所示:
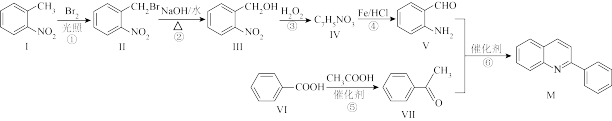
回答下列问题:
(1)喹啉(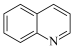 )常作配体,配位原子为
)常作配体,配位原子为________ (填元素符号)。
(2)反应②化学方程式是________ 。
(3)下列反应的反应类型分别是反应③________ 反应,④________ 反应。
(4)根据V的结构特征,分析预测其可能的化学性质,完成表格。
(5)化合物VI与乙酸反应可表示为VI+CH3COOH→VII+H2O+Y,则Y的分子式为_______ 。
(6)写出一种满足下列条件的VII的同分异构体结构简式_______ 。
①是芳香族化合物
②能发生加聚反应
③有酸性且能与FeCl3溶液发生显色反应
④核磁共振氢谱峰面积之比为1:1:2:2:2
(7)参照上述信息,写出以苯酚和化合物V为有机原料制备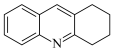 的合成路线:
的合成路线:_______ 。
(无机试剂任选,合成路线可表示A B……
B…… 目标产物)
目标产物)

回答下列问题:
(1)喹啉(
 )常作配体,配位原子为
)常作配体,配位原子为(2)反应②化学方程式是
(3)下列反应的反应类型分别是反应③
(4)根据V的结构特征,分析预测其可能的化学性质,完成表格。
| 序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
| a | 加成反应 | ||
| b | 氧化反应(生成氨基酸) |
(5)化合物VI与乙酸反应可表示为VI+CH3COOH→VII+H2O+Y,则Y的分子式为
(6)写出一种满足下列条件的VII的同分异构体结构简式
①是芳香族化合物
②能发生加聚反应
③有酸性且能与FeCl3溶液发生显色反应
④核磁共振氢谱峰面积之比为1:1:2:2:2
(7)参照上述信息,写出以苯酚和化合物V为有机原料制备
 的合成路线:
的合成路线:(无机试剂任选,合成路线可表示A
 B……
B…… 目标产物)
目标产物)
您最近一年使用:0次
解题方法
2 . Cu元素在生命活动中占有举足轻重的地位,缺铜会造成贫血、记忆力减退、反应迟钝、运动失常等。设计如下实验制备有机补铜剂顺式甘氨酸合铜水合物并测定其组成。
查阅资料:
①制备反应为:
②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:
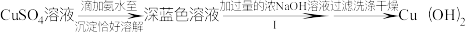

回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是_______ ,可采用的加热方式为_______ 。
(2)下列有关说法正确的是_______。
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知: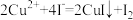
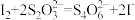
请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100L溶液→a→________ ,重复操作3次,消耗Na2S2O3标准液平均值为amL。
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为_______ ,若要提高产品的纯度,所用的实验方法名称是_______ 。
查阅资料:
①制备反应为:

②该反应同时生成顺式产物(天蓝色针状)和反式产物(蓝紫色鳞片状),其反应进程如图所示:

制备有机补铜剂顺式甘氨酸合铜水合物实验过程为:
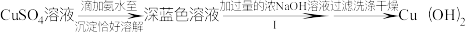

回答下列问题:
(1)步骤Ⅱ中控制反应温度为70℃的原因是
(2)下列有关说法正确的是_______。
| A.CuSO4和NaOH快速生成的Cu(OH)2絮状沉淀易裹挟杂质,故不采用CuSO4和NaOH直接反应制备Cu(OH)2 |
| B.步骤Ⅲ中趁热过滤是为了防止杂质析出 |
| C.步骤IV加入95%的乙醇可以得到纯度更高的产品,说明顺式甘氨酸的极性大于反式甘氨酸 |
| D.步骤V用25%酒精和丙酮分别洗涤晶体的目的是:25%酒精用于除去可溶性杂质(剩余反应物),丙酮用于除去晶体中残余的水 |
(3)用间接碘量法测定产物中Cu(Ⅱ)的质量分数。
已知:
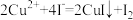
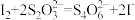
请选择以下正确的操作排序:
取2.0g所制备的产品,用稀硫酸溶解配成100L溶液→a→
a.取25mL该溶液转移入锥形瓶
b.立即用酸式滴定管中0.01 molL-1Na2S2O3标准液快速进行滴定
c.立即用碱式滴定管中0.01 mol L-1Na2S2O3标准液快速进行滴定
d.当溶液变为浅黄色时,加入1mL淀粉溶液
e.加入蒸馏水和过量的KI溶液,得到棕黄色溶液
f.继续滴定至溶液蓝色恰好褪去
g.继续滴定至溶液由无色变为蓝色
根据实验数据,所得晶体中Cu(Ⅱ)质量分数为
您最近一年使用:0次
3 . 甘氨酸(结构如图)常作食品的调味剂,还可预防氧化、延缓衰老等。甘氨酸与酸反应生成阳离子(用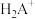 表示)。
表示)。 甘氨酸聚合成多肽,生成
甘氨酸聚合成多肽,生成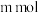 水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,
水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,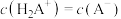 。下列叙述错误的是
。下列叙述错误的是
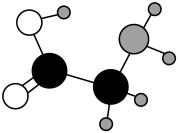
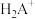 表示)。
表示)。 甘氨酸聚合成多肽,生成
甘氨酸聚合成多肽,生成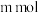 水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,
水分子。调节甘氨酸溶液的pH,当净电荷等于0时称为等电点,此时,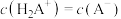 。下列叙述错误的是
。下列叙述错误的是
| A.甘氨酸是蛋白质水解的最终产物之一 |
| B.甘氨酸是两性化合物 |
| C.甘氨酸溶液调pH后,在等电点时显中性 |
| D.当n=m+1时合成的肽为肽链 |
您最近一年使用:0次
2023-06-27更新
|
152次组卷
|
4卷引用:吉林省白山市六所盟校2022-2023年高二下学期期未联考化学试题
名校
解题方法
4 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
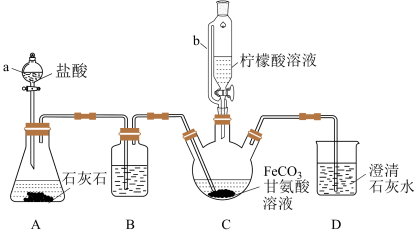
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
名校
5 . 我国科学家成功合成抗新冠肺炎新药Ebselen。一种合成Ebselen的流程如下(已知:氨基 具有强还原性):
具有强还原性):
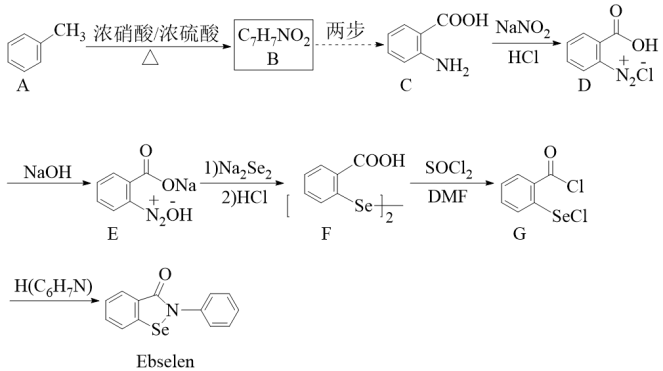
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是_______ 。H的结构简式为_______ 。
(2)一定条件下,E能与苯酚、NaOH反应生成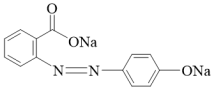 。写出该反应的化学方程式:
。写出该反应的化学方程式:_______ 。其有机反应类型是_______ 。
(3)生成G时,F中所断裂化学键是_______(填标号)。
(4)已知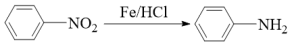 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑_______ 。
(5)在C的芳香族同分异构体中,同时具备下列条件的结构有_______ 种。
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备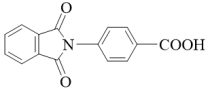 的微流程如下:
的微流程如下: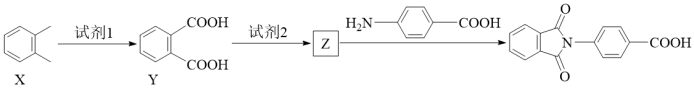
试剂2是_______ (填化学式)。
 具有强还原性):
具有强还原性):
请回答下列问题:
(1)D是一种重氮盐,易分解生成N2和
 ,含氯有机产物的化学名称是
,含氯有机产物的化学名称是(2)一定条件下,E能与苯酚、NaOH反应生成
 。写出该反应的化学方程式:
。写出该反应的化学方程式:(3)生成G时,F中所断裂化学键是_______(填标号)。
A.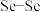 | B.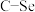 | C. | D.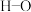 |
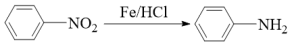 (具有强还原性),B、C之间两步反应的顺序设计中,要考虑
(具有强还原性),B、C之间两步反应的顺序设计中,要考虑(5)在C的芳香族同分异构体中,同时具备下列条件的结构有
①能发生银镜反应;②苯环上含氨基
(6)以邻二甲苯和对氨基苯甲酸为主要原料制备
 的微流程如下:
的微流程如下:
试剂2是
您最近一年使用:0次
解题方法
6 . 某抗抑郁药物有效成分F的合成路线如图。
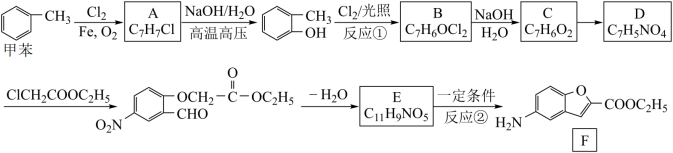
已知:①同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基
②
回答下列问题:
(1)D分子中除—CHO外的含氧官能团结构简式为_______ 。
(2)E的结构简式为_______ ;反应①的反应类型为 _______ 。
(3)反应B→C的化学方程式为_______ ;ClCH2COOC2H5加热条件下与足量NaOH反应后酸化所得的有机物发生聚合反应的化学方程式为 _______ 。
(4)化合物C中含有苯环的同分异构体有_______ 种,其中苯环上只有一个侧链且能发生银镜反应的有机物结构简式为 _______ 。
(5)下列有关F的叙述正确的是_______ 。
a.分子式为C11H10O3N
b.既能与盐酸反应生成盐,也能在NaOH反应生成盐
c.1mol F最多可以与2mol H2发生加成反应
d.既能发生加成反应也能发生取代反应

已知:①同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基
②

回答下列问题:
(1)D分子中除—CHO外的含氧官能团结构简式为
(2)E的结构简式为
(3)反应B→C的化学方程式为
(4)化合物C中含有苯环的同分异构体有
(5)下列有关F的叙述正确的是
a.分子式为C11H10O3N
b.既能与盐酸反应生成盐,也能在NaOH反应生成盐
c.1mol F最多可以与2mol H2发生加成反应
d.既能发生加成反应也能发生取代反应
您最近一年使用:0次
7 . 某药物K的合成路线如图:

已知:①R1CH2COOR2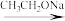
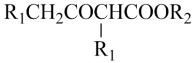
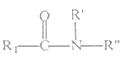
②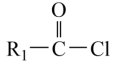

(1)下列说法正确的是____ 。
(2)I的结构简式是____ 。
(3)F→G的化学方程式为____ 。
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式____ 。
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):____ 。
CH2=CHCH3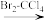 ____。
____。

已知:①R1CH2COOR2
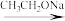
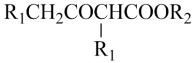
②
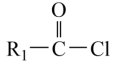


(1)下列说法正确的是
| A.1molG最多可以和3molH2发生加成反应 |
| B.化合物H既能和HCl溶液发生反应又能和NaOH溶液反应 |
| C.化合物J的分子式为C15H20N2 |
| D.K中有1个手性碳原子 |
(3)F→G的化学方程式为
(4)已知有机物L是H的同系物,且比H少1个C原子。写出同时符合下列条件的L所有同分异构体的结构简式
①属于芳香族化合物
②核磁共振氢谱显示4个吸收峰
③红外光谱谱图显示不含氢氧键、氧氧键、碳氮键
(5)根据题目所给信息,以A(丙烯)为原料,设计合成B(丙烯酸)的反应路线(用流程图表示,无机试剂任选):
CH2=CHCH3
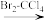 ____。
____。
您最近一年使用:0次
名校
8 . 化合物H是一种用于合成γ-分泌调节剂的药物中间体,其人工合成路线如下:

(1)F分子中采取sp2杂化的碳原子数目是_______ 。
(2)B→C的反应类型为_______ ,D的分子式为C10H11NO4,其结构简式为_______ 。
(3)B的一种同分异构体X同时满足下列条件,写出X的结构简式:_______ 。
①X既能与盐酸反应,又能与NaHCO3溶液反应。
②分子中不同化学环境的氢原子个数比是3∶2∶2∶2。
③苯环上有4个取代基。
(4)已知: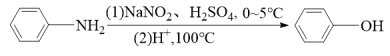 ,写出以
,写出以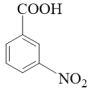 、(CH3)2SO4为原料制备
、(CH3)2SO4为原料制备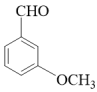 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

(1)F分子中采取sp2杂化的碳原子数目是
(2)B→C的反应类型为
(3)B的一种同分异构体X同时满足下列条件,写出X的结构简式:
①X既能与盐酸反应,又能与NaHCO3溶液反应。
②分子中不同化学环境的氢原子个数比是3∶2∶2∶2。
③苯环上有4个取代基。
(4)已知:
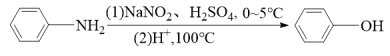 ,写出以
,写出以 、(CH3)2SO4为原料制备
、(CH3)2SO4为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
名校
9 . 磷酸氯喹是一种老的抗疟药,最新研究表明,它对新冠肺炎也有较好疗效。某研究小组按如下路线合成磷酸氯喹。
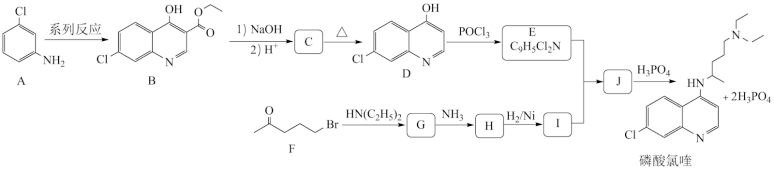
已知: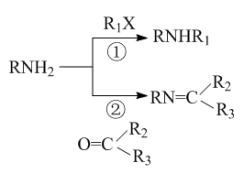 ,R为烃基或H
,R为烃基或H
按要求回答下列问题:
(1)B中含氧官能团名称为:___________ ,E的结构简式___________ 。
(2)下列有关说法正确的是___________。
(3)写出B生成C的第一步化学方程式___________ 。
(4)写出有机物F同时符合下列条件的同分异构体的结构简式___________ 。(写两种即可得分)
①分子中含有四元环结构
② 谱显示分子中有3种化学环境不同的氢原子
谱显示分子中有3种化学环境不同的氢原子
③IR谱检测表明分子中无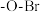 键
键
(5)以2-丙醇为原料制备 的合成路线,用流程图表示
的合成路线,用流程图表示___________ (无机试剂任选,合成中须用到上述①②两条已知信息)。

已知:
 ,R为烃基或H
,R为烃基或H按要求回答下列问题:
(1)B中含氧官能团名称为:
(2)下列有关说法正确的是___________。
A.有机物 的过程中有无色无味气体产生 的过程中有无色无味气体产生 |
B.反应 、 、 均为取代反应 均为取代反应 |
| C.有机物I具有弱碱性 |
D.磷酸氯喹的分子式为 |
(4)写出有机物F同时符合下列条件的同分异构体的结构简式
①分子中含有四元环结构
②
 谱显示分子中有3种化学环境不同的氢原子
谱显示分子中有3种化学环境不同的氢原子③IR谱检测表明分子中无
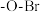 键
键(5)以2-丙醇为原料制备
 的合成路线,用流程图表示
的合成路线,用流程图表示
您最近一年使用:0次
名校
解题方法
10 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。某学习小组利用FeCO3与甘氨酸(NH2CH2COOH)制备甘氨酸亚铁,实验装置如图所示(夹持和加热、搅拌仪器已省略)。
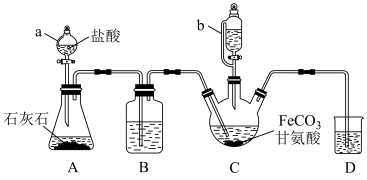
有关物质性质如下表:
实验过程:
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是_______ 。
(2)装置B中盛有的试剂是_______ ;实验过程中装置D的导管需要一直浸入液面下的必要性是_______ 。
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和_______ 。
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)可以用_______ 试剂(写化学式)检验产品中是否含有Fe3+。
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是_______ 。

有关物质性质如下表:
| 甘氨酸 | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇 | 易溶于水和乙醇 | 易溶于水,难溶于乙醇 |
| 两性化合物 | 强酸性、强还原性 |
I.合成:装置C中盛有0.1molFeCO3和200mL1.0mol·L−1甘氨酸溶液和适量柠檬酸。实验时,先打开仪器a的活塞,待装置C中空气排净后,加热C并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节pH到6左右,使反应物充分反应。
Ⅱ.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)仪器a的名称是
(2)装置B中盛有的试剂是
(3)合成过程加入柠檬酸的作用是促进FeCO3溶解和
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为
(5)过程II中加入无水乙醇的目的是
(6)可以用
(7)本实验制得16.1g甘氨酸亚铁(M=204g/mol),则其产率是
您最近一年使用:0次



