名校
1 . 下表是元素周期表的一部分,请用标出的元素回答有关问题:
⑴表中给出的化学性质最不活泼的元素,其原子结构示意图为__________________ 。
⑵表中能形成两性氢氧化物的元素是___________ (用元素符号表示),写出该元素形成的单质与⑨最高价氧化物对应的水化物反应的离子方程式:_______________________ 。
⑶用电子式表示④元素与⑦元素形成化合物的过程___________________________ 。
⑷写出②的最高价氧化物对应的水化物与其简单气态氢化物反应的生成物的化学式___________ 。
⑸③元素与⑩元素两者核电荷数之差是______________ 。
⑹为探究元素性质的递变规律,某化学兴趣小组将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由。______ ;_______________ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
⑴表中给出的化学性质最不活泼的元素,其原子结构示意图为
⑵表中能形成两性氢氧化物的元素是
⑶用电子式表示④元素与⑦元素形成化合物的过程
⑷写出②的最高价氧化物对应的水化物与其简单气态氢化物反应的生成物的化学式
⑸③元素与⑩元素两者核电荷数之差是
⑹为探究元素性质的递变规律,某化学兴趣小组将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由。
您最近一年使用:0次
2 . 下图是元素周期表的一部分。
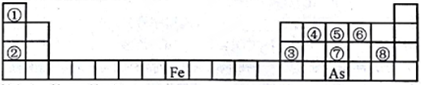
I.用化学用语回答下列问题:
(1)②、⑥、⑧的离子半径由大到小的顺序为_________ (用离子符号表示)。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。(用化学式表示)
(3)As的原子结构示意图为_______ ;其氢化物的化学式为_______ 。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_________ ,当消耗1mol还原剂时,电子转移了______ mol。
Ⅱ.A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。
(5)A与水反应的化学方程式为_______________ 。
(6)工业上常用热还原法冶炼X,写出其化学方程式___________ 。
(7)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式_______________ 。

I.用化学用语回答下列问题:
(1)②、⑥、⑧的离子半径由大到小的顺序为
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)As的原子结构示意图为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
Ⅱ.A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。
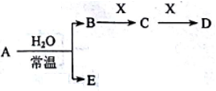
(5)A与水反应的化学方程式为
(6)工业上常用热还原法冶炼X,写出其化学方程式
(7)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式
您最近一年使用:0次
解题方法
3 . 有人推测尚未合成的第114号元素有相当稳定的同位素,恰处在不稳定核素的“海洋”中浮起的一群较稳定核素的“岛屿”的中心。114号元素是第_______ 周期第_______ 族元素,它的可能氧化态_______ 。
您最近一年使用:0次
4 . 在1—18号元素中,选择合适的选项回答下列问题
1.写出①和②的非金属性较强的是( )
2.写出④的最高价氧化物化学式( )
3.写出③和⑤的最高价氧化物对应水化物反应的离子方程式( )
4.③和④两种元素的最高价氧化物对应水化物中碱性较强的是
5.写出③的单质在②单质中燃烧的现象()
6.①元素在周期表中的位置是( )
7.②和⑤两种元素中原子半径较大的是( )
8.下列化学用语表达不正确 的是( )
9.⑤和⑥形成的气态氢化物最稳定的是( )
10.④的氧化物类型为 ( )
| ① | ② | ||||||||||||||
| ③ | ④ | ⑤ | ⑥ |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.RO | B.R2O | C.R2O3 | D.RO2 |
| A.2NaOH+H2SO4=Na2SO4+2H2O | B.H+ +OH- =H2O |
| C.NaOH+H2SO4=Na2SO4+H2O | D.2OH- +H2SO4=SO42- +2H2O |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.白色固体 | B.淡黄色固体 | C.浅紫色火焰 | D.苍白色火焰 |
| A.第二周期第四主族 | B.第二周期第IV主族 |
| C.第二周期第IVA族 | D.第二周期第VA族 |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
A.氟离子的结构示意图: | B.水分子的电子式: |
| C.二氧化碳的结构式:O=C=O | D.硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.酸性氧化物,非金属氧化物 | B.两性氧化物,金属氧化物 |
| C.碱性氧化物,金属氧化物 | D.酸性氧化物,金属氧化物 |
您最近一年使用:0次
12-13高一下·广东东莞·期中
名校
解题方法
5 . 下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答。
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是________ ,氧化性最强的单质是______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物碱性最强的是___ ,酸性最强的是____ ,呈两性的是 _______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的______________ ,
(4)在B、C、E、F、G、H中,原子半径最大的是_________ ,
(5)A和D组成化合物的电子式_____________________ ,
(6)A和E组成化合物的化学式_____________________ ,
(7)用电子式表示B和H组成化合物的形成过程______________________________ ,
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式___________________________________________ 。
| 族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、E、F、G、H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)A和E组成化合物的化学式
(7)用电子式表示B和H组成化合物的形成过程
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
1049次组卷
|
3卷引用:2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷
(已下线)2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题河北省石家庄市元氏县第四中学2019-2020学年高一下学期期中考试化学试题
解题方法
6 . 元素周期表的形式多种多样,下图是扇形元素周期表的一部分,扇面的18折相当于中学化学常见长式元素周期表的18列,1、2、3、4相当于周期,针对表中所给元素,对照中学化学常见长式元素周期表,回答下列问题:
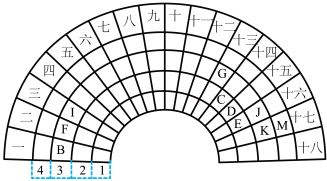
(1)表中金属性最强的元素在长式元素周期表中的位置是___________ ,该元素单质与水反应的化学方程式为______________ 。
(2)表中最高价氧化物对应的水化物酸性最强的是__________ (填酸的化学式)。
(3)元素F与K形成化合物的电子式为__________ 。
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式_________ 。
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式________ 。

(1)表中金属性最强的元素在长式元素周期表中的位置是
(2)表中最高价氧化物对应的水化物酸性最强的是
(3)元素F与K形成化合物的电子式为
(4)写出元素D最高价氧化物对应水化物的稀溶液与铜单质反应的离子方程式
(5)元素G的最高价氧化物对应水化物跟氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
7 . 下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼 的是:_______ (填具体元素符号或化学式 ,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_________ ,第三周期中碱性最强的化合物的化学式是____________________ 。
(3)最高价氧化物是两性氧化物的元素是____________ ;写出它最高价氧化物对应水化物与氢氧化钠反应的化学 方程式_______________________________________ 。
(4)用电子式表示元素④与⑥形成化合物的形成过程:________________________ ,该化合物属于__________________ (填 “共价”或“离子”)化合物。
(5)表示③与①最高价态形成的化合物电子式 ___________________ ,该化合物分子由___________ (填“极性”“非极性”)键形成。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在这些元素中,化学性质
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥形成化合物的形成过程:
(5)表示③与①最高价态形成的化合物
您最近一年使用:0次
解题方法
8 . 下表是元素周期表的一部分,针对a~k十一种元素回答下列问题(请用具体化学式回答,否则不给分):
(1)这些元素中非金属性最强的单质是_________ ,最高价氧化物对应水化物酸性最强的是_________ ,最高价氧化物对应水化物碱性最强的是_________ 。
(2)表中k的氢化物的化学式为_____ ,它的还原性比j的氢化物还原性_______ (填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性_______ (填“强”或“弱”)。
(3)e单质为________ ,其结构式为________________ 。
(4)用电子式表示h与k构成化合物的形成过程________________
(5)写出i的氧化物与强碱溶液反应的离子方程式________________
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热。将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应。下列说法正确的是____ (填写选项)。
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(1)这些元素中非金属性最强的单质是
(2)表中k的氢化物的化学式为
(3)e单质为
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热。将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应。下列说法正确的是
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡
您最近一年使用:0次
2016-12-09更新
|
434次组卷
|
2卷引用:2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷
9 . 下表列出了7种短周期元素在元素周期表中的相对位置,其中元素①的最低负化合价的绝对值与其原子最外层电子数相等,元素⑤是地壳中含量最多的金属元素。
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是_______ 。
(2)上述7中元素中,非金属性最强的是______ (填元素符号);最高价氧化物对应水化物中,碱性最强的物质的化学式是_______ 。
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是________ 。
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是_______________ 。
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是_______ 。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是_______ 。
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
请用相应的化学用语回答下列问题:
(1)元素①在元素周期表中所处的位置是
(2)上述7中元素中,非金属性最强的是
(3)③、⑥、⑦三种元素形成的简单气态氢化物的稳定性由强到弱的顺序是
(4)元素④和⑤各自的最高价氧化物对应水化物相互间发生反应的离子方程式是
(5)化合物甲是元素②形成的最简单氢化物,甲的电子式是
您最近一年使用:0次
解题方法
10 . 处于金属和非金属分界线附近的元素常作催化剂( )
您最近一年使用:0次



