名校
解题方法
1 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)②的最高价氧化物的分子式为_______ ;⑦的最高价氧化物对应水化物的分子式为_______ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
| A.在化合物中最高正化合价为+6 | B.单质可以与 气体反应并置换出单质S 气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
①铯的原子序数为
②铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
2023-11-10更新
|
882次组卷
|
2卷引用:广西柳州铁一中学2022-2023学年高一上学期期末考试化学试题
解题方法
2 . 元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
2023-01-04更新
|
726次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
名校
3 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
2021-01-20更新
|
1806次组卷
|
6卷引用:新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题
新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题
4 . 几种主族元素在周期表中的位置如表:
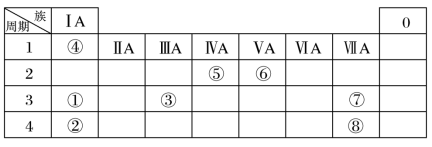
根据表回答下列问题:
(1)⑤元素的简单氢化物的电子式是_____ 、⑤的最高价氧化物结构式_____ 。
(2)①②③三种元素原子半径由大到小的顺序是____ (用元素符号表示)。
(3)表中8种元素中,最高价氧化物有两性的元素的原子结构示意图为_____ ,该元素在周期表中的位置是____ 。
(4)⑤⑥⑦三种元素最高价氧化物对应水化物酸性最强的是_____ (填化学式),②与③最高价氧化物对应水化物反应的化学方程式为_____ 。
(5)非金属性强弱比较⑦_____ ⑧(填写“大于”或“小于”)下列表述中能证明这一事实的是_____ (填字母)。
a.⑦的氢化物比⑧的氢化物水溶液酸性弱
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的简单阴离子的还原性比⑧的简单阴离子的还原性弱
(6)③与⑦形成的化合物是_____ (填“离子”或“共价”)化合物。

根据表回答下列问题:
(1)⑤元素的简单氢化物的电子式是
(2)①②③三种元素原子半径由大到小的顺序是
(3)表中8种元素中,最高价氧化物有两性的元素的原子结构示意图为
(4)⑤⑥⑦三种元素最高价氧化物对应水化物酸性最强的是
(5)非金属性强弱比较⑦
a.⑦的氢化物比⑧的氢化物水溶液酸性弱
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的简单阴离子的还原性比⑧的简单阴离子的还原性弱
(6)③与⑦形成的化合物是
您最近一年使用:0次
5 . 下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
2022-01-14更新
|
783次组卷
|
4卷引用:湖南省怀化市2021-2022学年高一上学期期末考试化学试题
湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
6 . 合成氨是人类科学技术发展史上的一项重大成就,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氮原子中,能量最高的电子的电子云在空间有_______ 个伸展方向。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为_______ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①Cr原子的价电子排布图为_______ ;第四周期ds区元素中,与基态Cr原子最外层电子数目相同的元素的元素符号为_______ 。
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有_______ (填元素符号)
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①Mn在元素周期表中的位置_______ ,基态Mn原子未成对的电子数为_______ 。
②第三电离能
_______ 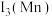 (填“>”或“<”),原因是
(填“>”或“<”),原因是_______ 。
(1)基态氮原子中,能量最高的电子的电子云在空间有
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用“
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
”表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①Cr原子的价电子排布图为
②上述氧化物所涉及的元素中,处于元素周期表中p区的元素有
(4)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①Mn在元素周期表中的位置
②第三电离能

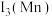 (填“>”或“<”),原因是
(填“>”或“<”),原因是
您最近一年使用:0次
2023-02-14更新
|
662次组卷
|
3卷引用:山东省泰安市2022-2023学年高二上学期期末考试化学试题
7 . 元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①~⑧分别代表一种元素。回答下列问题:
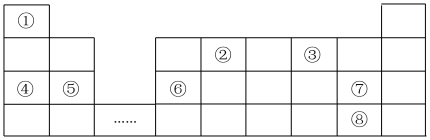
(1)元素①含2个中子的核素为_____ (填符号)。
(2)元素②、③形成的化合物_____ (填“属于”或“不属于”)电解质。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为_____ (用离子符号填空)。
(4)元素④、⑤、⑥金属性由强到弱的顺序为_____ ,元素④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为_____ ,该反应的离子方程式为_____ 。

(1)元素①含2个中子的核素为
(2)元素②、③形成的化合物
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
(4)元素④、⑤、⑥金属性由强到弱的顺序为
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为
您最近一年使用:0次
解题方法
8 . X是第四周期中未成对电子数最多的元素
(1)X是___________ (填元素符号)。
(2)它位于___________ 族,属于___________ 区。
(3)它的核外电子排布式是___________ ,价层电子的轨道表示式___________ 。
(4)它有___________ 个能层,___________ 个能级。
(5)价层电子排布式的特点是___________ 。
(1)X是
(2)它位于
(3)它的核外电子排布式是
(4)它有
(5)价层电子排布式的特点是
您最近一年使用:0次
名校
9 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
2022-03-15更新
|
800次组卷
|
4卷引用:北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
10 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为______ ,其最高价氧化物对应的水化物含有的化学键类型为______ ,⑩元素最高价氧化物对应的水化物的化学式是______ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是______ (用化学式表示,下同),②、⑧简单氢化物熔点高的是______ ,④、⑤最高价氧化物的水化物碱性更强的是______ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序______ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置______ 。
ii.关于铷的下列说法中不正确的是______ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
2021-01-07更新
|
1359次组卷
|
3卷引用:辽宁省五校联考2020-2021学年高一上学期期末考试化学试题



