名校
1 . 如图是元素周期表的一部分,表中列出了八种元素的位置:
请回答下列问题:
(1)①元素的简单氢化物的电子式为______ 。
(2)在元素①-⑧中,金属性最强的元素是______ (填元素符号),最高价含氧酸酸性最强的是_____ (填化学式)。
(3)②、③、④三种元素的原子半径由大到小的顺序是_____ (填元素符号),③和⑦的简单氢化物的稳定性较强的是_____ (填化学式)。
(4)④和⑤所形成的化合物属于_____ (填“离子”或“共价”)化合物。
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为_____ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①元素的简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)②、③、④三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
2023-04-09更新
|
479次组卷
|
2卷引用:湖南省岳阳教研联盟2022-2023学年高一下学期联考联评化学试题
名校
2 . 德米特里·伊万诺维奇·门捷列夫是著名的俄国化学家,他对化学的发展作出了卓越的贡献。请回答下列问题:
(1)门捷列夫的突出贡献是________
(2)某元素的原子L层电子数比K层电子数多3个,与该元素同一主族的短周期元素是___________ 。
(3)C、O、Na的原子半径从大到小的顺序为___________ 。
(4)请你根据原子结构示意图,分别指出这些原子所含的质子数、元素周期表中的位置。___________ ,周期表中位置:___________ 。
(5)请将短周期元素或其化合物填入下列表格
①金属性最强的元素是___________ (填元素符号);
②形成化合物种类最多的元素是___________ (填元素符号);
③第三周期中,简单气态氢化物热稳定性最好的是___________ (填写分子式)。
(1)门捷列夫的突出贡献是________
| A.提出原子学说 | B.发现元素周期律 |
| C.提出分子学说 | D.发现氧气 |
(3)C、O、Na的原子半径从大到小的顺序为
(4)请你根据原子结构示意图,分别指出这些原子所含的质子数、元素周期表中的位置。

(5)请将短周期元素或其化合物填入下列表格
①金属性最强的元素是
②形成化合物种类最多的元素是
③第三周期中,简单气态氢化物热稳定性最好的是
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
3 . 回答下列问题:
(1)根据“原子序数”推导元素
①56号元素位于第___________ 周期___________ 族。
②114号元素位于第___________ 周期___________ 族。
③35号元素位于第___________ 周期___________ 族。
(2)根据“元素符号”填空(前20号元素)
①主族序数与周期数相同的元素有___________ 。
②主族序数是周期数2倍的元素有___________ ,主族序数是周期数3倍的元素有___________ 。
③周期数是主族序数2倍的元素有___________ ,周期数是主族序数3倍的元素有___________ 。
(3)用“元素符号”填空
①最高正价与最低负价代数和为0的短周期元素是___________ 。
②最高正价是最低负价绝对值3倍的短周期元素是___________ 。
(4)①甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是___________ (填序号)。
A.x+2 B.x+4
C.x+8 D.x+18
②若甲、乙分别是同一周期的ⅡA族和ⅢA族元素,原子序数分别为m和n。则下列关于m和n的关系不正确的是___________ (填序号)。
A.n=m+1 B.n=m+18
C.n=m+25 D.n=m+11
(1)根据“原子序数”推导元素
①56号元素位于第
②114号元素位于第
③35号元素位于第
(2)根据“元素符号”填空(前20号元素)
①主族序数与周期数相同的元素有
②主族序数是周期数2倍的元素有
③周期数是主族序数2倍的元素有
(3)用“元素符号”填空
①最高正价与最低负价代数和为0的短周期元素是
②最高正价是最低负价绝对值3倍的短周期元素是
(4)①甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A.x+2 B.x+4
C.x+8 D.x+18
②若甲、乙分别是同一周期的ⅡA族和ⅢA族元素,原子序数分别为m和n。则下列关于m和n的关系不正确的是
A.n=m+1 B.n=m+18
C.n=m+25 D.n=m+11
您最近一年使用:0次
名校
解题方法
4 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
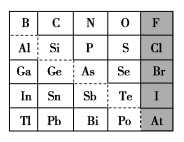
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第______ 周期第______ 族。
(2) 的最高化合价为
的最高化合价为______ , 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为______ , 的最高价氧化物为
的最高价氧化物为______ 。
(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是______ 元素(填元素符号)。
②酸性:
______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
______  。
。
④原子半径:
______  。
。
(4)可在图中分界线(虚线)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较 、
、 的非金属性强弱:
的非金属性强弱:______ 。(可供选择的药品有 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)

(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)
 的最高化合价为
的最高化合价为 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。④原子半径:

 。
。(4)可在图中分界线(虚线)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较
 、
、 的非金属性强弱:
的非金属性强弱: 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)
您最近一年使用:0次
2020-09-08更新
|
1584次组卷
|
6卷引用:人教版(2019)高一必修第一册 全书综合训练(一)
解题方法
5 . 联合国将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,下表代表元素周期表前四周期,回答下列问题:
(1)将磷的元素符号填写在上述周期表相应的空格中___________ 。
(2)Cl元素的最高价氧化物对应水化物的化学式为___________ 。
(3)下列有关性质的比较正确,且能用元素周期律解释的是___________ 。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:HF<HCl
(4)从原子结构角度解释元素的非金属性S弱于Cl的原因___________ 。
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为 。
。
①Se在元素周期表中的位置是___________ 。
②Se的气态氢化物的化学式为____________ 。
③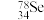 和
和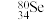 互称为
互称为___________ 。
(1)将磷的元素符号填写在上述周期表相应的空格中
(2)Cl元素的最高价氧化物对应水化物的化学式为
(3)下列有关性质的比较正确,且能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:HF<HCl
(4)从原子结构角度解释元素的非金属性S弱于Cl的原因
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为
 。
。①Se在元素周期表中的位置是
②Se的气态氢化物的化学式为
③
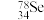 和
和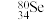 互称为
互称为
您最近一年使用:0次
2022-01-14更新
|
419次组卷
|
2卷引用:北京市石景山区2021-2022学年高一上学期期末考试化学试题
6 . 分析下列图表,回答问题。
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
则该元素是_______ (填写元素符号)。
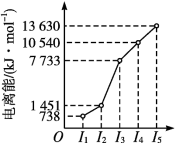
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第_______ 族。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价层电子排布式:_______ ,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______ 。
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | …… |
| In/( kJ∙mol−1) | 578 | 1 817 | 2 745 | 11 575 | …… |
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第

(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| I1 | 717 | 759 | |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
您最近一年使用:0次
名校
解题方法
7 . 下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:

(1)地壳中含量最高的金属元素是___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)用电子式表示J与C形成化合物的过程:___________ 。
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。

(1)地壳中含量最高的金属元素是
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)用电子式表示J与C形成化合物的过程:
(6)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
2023-01-11更新
|
441次组卷
|
4卷引用:河北省保定市部分高中2022-2023学年高一上学期期末考试化学试题
名校
8 . 下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)画出①和③两种元素的原子1:2组成的化合物的电子式_______ 。
(2)元素①-⑩中化学性质最不活泼的元素是_______ (填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______ (填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①-⑩中化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生的化学方程式为
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
您最近一年使用:0次
2022-04-04更新
|
400次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高一上学期期末考试化学试题
解题方法
9 . 下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素④的名称是_______ 。
(2)⑥、④、⑦中气态氢化物稳定性最强的是:_______ (写氢化物的化学式)。
(3)元素⑦的原子结构示意图是_______ 。
(4)写出元素⑤形成的单质在氧气中燃烧的化学方程式_______ 。
| ⅠA | |||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ② | ③ | ④ | ⑧ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ |
请按要求回答下列问题。
(1)元素④的名称是
(2)⑥、④、⑦中气态氢化物稳定性最强的是:
(3)元素⑦的原子结构示意图是
(4)写出元素⑤形成的单质在氧气中燃烧的化学方程式
您最近一年使用:0次
10 . 根据以下9种元素在元素周期表中的位置,回答下列问题:
(1)①的原子轨道形状是_______ ;②③④的第一电离能由大到小的顺序是_______ (填编号)。
(2)下列可以判断⑤和⑥金属性强弱的是_______ (填序号)。
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式_______ ,它的熔点高,硬度大,电绝缘性好,化学性质稳定。它的晶体类型是_______ ,试推测其可能有哪些用途_______ (填序号)。
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式
您最近一年使用:0次



