3. 元素周期表的表达形式有多种,但都能表示出元素的周期性变化规律,请回答下列问题:
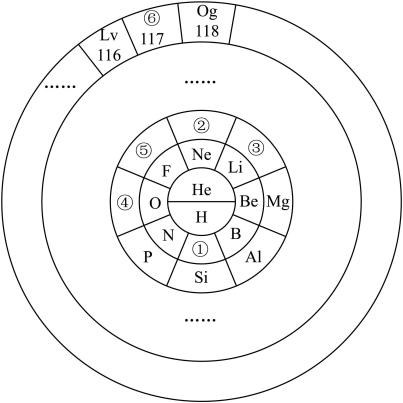
(1)①与④元素形成的化合物属于
___________晶体。
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:
__________。
(3)②号元素为
___________(填元素符号)。请写出1个与②核外电子数相同的简单离子组成的化合物的化学式:
___________。其中存在的化学键属于
___________键,该物质在熔融状态下
___________导电(填“能”或“不能”)。
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:
___________,将反应所得混合物溶于水,得到浅绿色的溶液,请写出相关的离子方程式:
___________。
(5)其中非金属性④
___________⑤(填“>”或“<”),请用一个化学方程式证明
___________。
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为
___________,根据元素的周期性规律,以下推测正确的是
________A.单质在常温下为气体
B.气态氢化物的稳定性较好
C.离子具有强还原性
D.半径大于⑤