德米特里·伊万诺维奇·门捷列夫是著名的俄国化学家,他对化学的发展作出了卓越的贡献。请回答下列问题:
(1)门捷列夫的突出贡献是________
(2)某元素的原子L层电子数比K层电子数多3个,与该元素同一主族的短周期元素是___________ 。
(3)C、O、Na的原子半径从大到小的顺序为___________ 。
(4)请你根据原子结构示意图,分别指出这些原子所含的质子数、元素周期表中的位置。

质子数:___________ ,周期表中位置:___________ 。
(5)请将短周期元素或其化合物填入下列表格
①金属性最强的元素是___________ (填元素符号);
②形成化合物种类最多的元素是___________ (填元素符号);
③第三周期中,简单气态氢化物热稳定性最好的是___________ (填写分子式)。
(1)门捷列夫的突出贡献是________
| A.提出原子学说 | B.发现元素周期律 |
| C.提出分子学说 | D.发现氧气 |
(3)C、O、Na的原子半径从大到小的顺序为
(4)请你根据原子结构示意图,分别指出这些原子所含的质子数、元素周期表中的位置。

质子数:
(5)请将短周期元素或其化合物填入下列表格
①金属性最强的元素是
②形成化合物种类最多的元素是
③第三周期中,简单气态氢化物热稳定性最好的是
22-23高一下·上海黄浦·期末 查看更多[3]
(已下线)寒假作业10 元素周期律-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)(已下线)课时2 元素周期表和元素周期律的应用上海市大同中学2022-2023学年高一下学期期末考试化学试题
更新时间:2023-07-16 16:02:29
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①〜⑩元素,填写下列空白:
(1)表中所列元素中,属于短周期金属元素的为__________ (填元素符号),其原子半径由大到小的顺序为__________ (用元素符号表示)。
(2)表中不属于主族元素的是__________ (填元素符号),该元素在周期表中的位置是__________ 。
(3)1mol④的单质与足量②的氢化物完全反应产生的气体在标准状况下的体积为__________ 。
| 族 周期 | I A | II A | … | III A | IV A | V A | VI A | VII A | 0 |
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑩ | |||
| 4 | ⑨ |
(1)表中所列元素中,属于短周期金属元素的为
(2)表中不属于主族元素的是
(3)1mol④的单质与足量②的氢化物完全反应产生的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:
(1)②表示的元素是______ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是______ (填元素符号),其非金属性较强的是 ______ (填元素符号),其最高正价氧化物水化物酸性较强的酸是_______ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______ (填化学式)。③与⑥两种元素所形成化合物所含化学键是______ (填“共价键”或“离子键”)。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:____________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ① | ② | F | Ne | ||||
| 3 | ③ | Mg | ④ | Si | ⑤ | ⑥ |
(1)②表示的元素是
(2)①与⑤两种元素相比较,原子半径较大的是
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
【推荐1】(1)基态Ti原子的核外电子排布式为__ 。
(2)H、B、N中,原子半径最大的是__ 。根据对角线规则,B的一些化学性质与元素__ 的相似。
(3)Fe、Co、Ni在周期表中的位置为__ ,基态Fe原子的电子排布式为__ 。
(2)H、B、N中,原子半径最大的是
(3)Fe、Co、Ni在周期表中的位置为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】A、B、C、D、E、F是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族.
(1)D在周期表中的位置_____________________ 。
(2)B的原子结构示意图_____________________ 。
(3)E元素形成最高价氧化物对应水化物的化学式为_____________________ 。
(4)元素C、D、E形成的原子半径大小关系是_____________________ (用元素符号表示).
(5)B、C的气态氢化物的稳定性关系为____________________ (填化学式)。
(6)C、D可形成原子个数比为1:1的化合物的电子式是_____________________ 。
(7)写出A、C、F三种元素按原子个数比1:1:1形成化合物的结构式______________ 。
(1)D在周期表中的位置
(2)B的原子结构示意图
(3)E元素形成最高价氧化物对应水化物的化学式为
(4)元素C、D、E形成的原子半径大小关系是
(5)B、C的气态氢化物的稳定性关系为
(6)C、D可形成原子个数比为1:1的化合物的电子式是
(7)写出A、C、F三种元素按原子个数比1:1:1形成化合物的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】比较下列微粒半径的大小(用“>”或“”填空):
(1)Na_____Mg_____Cl,______
(2)Li________Na_________K,______
(3)Na+______Mg2+________Al3+,______
(4)F-_____Cl-_________Br-,______
(5)Cl-______O2−______Na+____Mg2+,______
(6)Fe2+______ Fe3+
(1)Na_____Mg_____Cl,
(2)Li________Na_________K,
(3)Na+______Mg2+________Al3+,
(4)F-_____Cl-_________Br-,
(5)Cl-______O2−______Na+____Mg2+,
(6)Fe2+
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知氟、氯、溴、碘在元素周期表中位于同一纵行,都是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素。卤素单质都具有氧化性,其氧化性强弱顺序是F2>Cl2>Br2>I2,它们都能与H2、H2O等反应。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是________________________ ,其反应条件难易规律是________________________________________ 。
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式:______________________ ,离子方程式:________________________________ 。
(1)若用X2表示卤素单质,则X2与H2化合的化学方程式是
(2)氧化性强的卤素单质(如Cl2)能把氧化性弱的卤素从其卤化物(如NaBr或KI)中置换出来。请写出将氯气通入碘化钾溶液中的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表列出① ~ ⑨九种元素在周期表中的位置:
(1)这九种元素化学性质最不活泼的元素名称是___________ 。
(2) ①、②、③三种元素的高价氧化物对应的水化物,其中碱性最强的是___________ 。(填化学式)
(3) ①、③、④三种元素按原子半径由大到小的顺序排列为___________ 。(填元素符号)
(4) ③的原子序数为___________
(5)⑧在周期表中的位置___________
(6)⑦的最高价氧化物的水化物的化学式___________
(7)⑥元素氢化物的化学式是___________ ,该氢化物在常温下跟①发生反应的化学方程式是___________ 。
(8)⑤的原子结构示意图为___________
(9)其单质在常温下为液态的非金属元素是___________ (填编号)
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(1)这九种元素化学性质最不活泼的元素名称是
(2) ①、②、③三种元素的高价氧化物对应的水化物,其中碱性最强的是
(3) ①、③、④三种元素按原子半径由大到小的顺序排列为
(4) ③的原子序数为
(5)⑧在周期表中的位置
(6)⑦的最高价氧化物的水化物的化学式
(7)⑥元素氢化物的化学式是
(8)⑤的原子结构示意图为
(9)其单质在常温下为液态的非金属元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】短周期元素A、B、D、E、G、J在周期表中的位置如下:
根据上表回答问题:
(1)D在周期表中的位置是_______ 。
(2)A、B、E、G的原子半径由大到小的顺序是_______ (填元素符号)。
(3)B、D的气态氢化物的稳定性关系为_______ (填化学式)。
(4)用电子式表示A与J形成化合物的过程:_______ 。
(5)34Se与D同主族,其非金属性比D_______ (填“强”或“弱”),从原子结构的角度解释其原因_______ 。
(6)E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为:
①H++OH-=H2O;
②_______ ;
③_______ 。
(7)A和B可以形成多种化合物,下图模型表示的分子中,不可能由A和B形成的是_______ (填序号)。
a.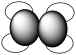 b.
b.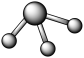 c.
c.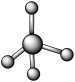 d.
d.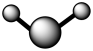
| A | |||||||
| B | D | ||||||
| E | G | J |
根据上表回答问题:
(1)D在周期表中的位置是
(2)A、B、E、G的原子半径由大到小的顺序是
(3)B、D的气态氢化物的稳定性关系为
(4)用电子式表示A与J形成化合物的过程:
(5)34Se与D同主族,其非金属性比D
(6)E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为:
①H++OH-=H2O;
②
③
(7)A和B可以形成多种化合物,下图模型表示的分子中,不可能由A和B形成的是
a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次

 (用R代表)。回答下列问题:
(用R代表)。回答下列问题: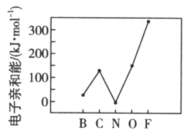
 )。第二周期部分元素的
)。第二周期部分元素的

