如图是元素周期表的一部分,表中列出了八种元素的位置:
请回答下列问题:
(1)①元素的简单氢化物的电子式为______ 。
(2)在元素①-⑧中,金属性最强的元素是______ (填元素符号),最高价含氧酸酸性最强的是_____ (填化学式)。
(3)②、③、④三种元素的原子半径由大到小的顺序是_____ (填元素符号),③和⑦的简单氢化物的稳定性较强的是_____ (填化学式)。
(4)④和⑤所形成的化合物属于_____ (填“离子”或“共价”)化合物。
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为_____ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①元素的简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)②、③、④三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
更新时间:2023-04-09 14:06:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm).
(1)C元素在元素周期表中的位置是______ ;
(2)B的原子结构示意图为______ ;
(3)D、E气态氢化物的稳定性强弱顺序为______ (填化学式);
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是______ (填化学式);
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:______ ;
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:______ ;
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.037 | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | -1 | -2 | +5、-3 |
(1)C元素在元素周期表中的位置是
(2)B的原子结构示意图为
(3)D、E气态氢化物的稳定性强弱顺序为
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是________________ ;离子半径由大到小的顺序是______________ ;阳离子中氧化性较强的是____________ ,阴离子中还原性较强的是______________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请用元素符号(或化学式)回答原子序数11-18的元素有关问题:
(1)除稀有气体外,原子半径最大的是________________________________ 。
(2)最高价氧化物的水化物中碱性最强的是____________________________ 。
(3)最高价氧化物的水化物中呈两性的是______________________________ 。
(4)最高价氧化物的水化物中酸性最强的是____________________________ 。
(5)气态氢化物中最稳定的是________________________________________ 。
(1)除稀有气体外,原子半径最大的是
(2)最高价氧化物的水化物中碱性最强的是
(3)最高价氧化物的水化物中呈两性的是
(4)最高价氧化物的水化物中酸性最强的是
(5)气态氢化物中最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中①到⑩10种元素,填写下表空白:
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的化学式是______ 。 均填化学式
均填化学式
(2)最高价氧化物对应的水化物是两性的元素是______  填元素符号
填元素符号 ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式______ 。
(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是 用离子符号表示
用离子符号表示
______ 。
列 周期 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
4 | ⑩ |
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是
 均填化学式
均填化学式
(2)最高价氧化物对应的水化物是两性的元素是
 填元素符号
填元素符号 ,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式
,写出它的氢氧化物与⑤的氢氧化物反应的离子方程式(3)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是
 用离子符号表示
用离子符号表示
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习化学的重要工具,下表是元素周期表的一部分,请回答下列问题:
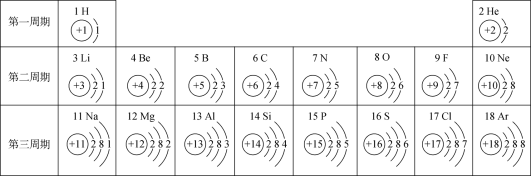
(1)不同元素之间的最本质区别是_________ 不同;
(2)表中与氧元素化学性质相似的是_______ 元素;
(3)12号元素的原子在化学反应中比较容易_____ (填“得到”或“失去”)电子;
(4)11﹣18号元素在表中处于同一周期的原因是它们原子结构中的_____ 相同。

(1)不同元素之间的最本质区别是
(2)表中与氧元素化学性质相似的是
(3)12号元素的原子在化学反应中比较容易
(4)11﹣18号元素在表中处于同一周期的原因是它们原子结构中的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(I)俄美科学家联合小组宣布合成出114号元素(FI)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置______________ ,属于金属元素还是非金属元素?____
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式___________________ 。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
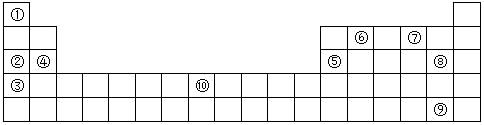
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为__________ 。
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________ 。
(3)元素Fe的单质与⑦的氢化物高温下反应的化学方程式为___________ 。
(III)判断以下叙述正确的是__________ 。
部分短周期元素的原子半径及主要化合价
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物一定具有两性
D.氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(1)元素⑦的氢化物与⑧的单质反应的离子方程式为
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为
(3)元素Fe的单质与⑦的氢化物高温下反应的化学方程式为
(III)判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物一定具有两性
D.氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是元素周期表的一部分,A~J代表对应的元素,回答下列问题:
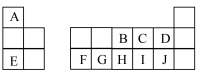
(1)F的元素符号为___________ ,元素C在周期表中的位置为___________ 。
(2)A、D和E三种元素的离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(4)A、B和J三种元素形成常见化合物所含化学键的类型是___________ 。
(5)下列说法错误的是___________ (填标号)。
a.单质的熔点:
b.简单氢化物的沸点:
c.氧化物对应水化物的酸性:
(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为___________ 。

(1)F的元素符号为
(2)A、D和E三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、B和J三种元素形成常见化合物所含化学键的类型是
(5)下列说法错误的是
a.单质的熔点:

b.简单氢化物的沸点:

c.氧化物对应水化物的酸性:

(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.自然界的硫循环对动植物和人类的生存意义重大。
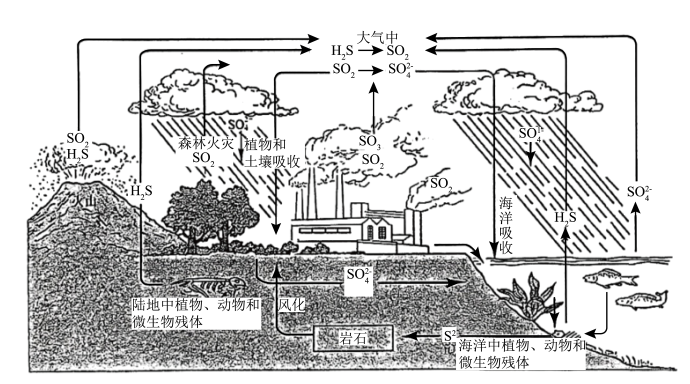
(1)生物体内多种蛋白质含有硫元素,硫与同主族的氧元素相比,非金属性S_____ O(选填“>”、“<”或“=”),写出两种能够比较说明O和S非金属性强弱的化学事实或化学反应方程式_______ 、_____ 。
(2)已知 与硫元素属于同一主族,原子序数比硫大18,写出
与硫元素属于同一主族,原子序数比硫大18,写出 在元素周期表的位置
在元素周期表的位置_______ ,写出 原子的原子结构示意图
原子的原子结构示意图_______ 。
(3)O、S和 都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
(4)硫元素在第三周期,第三周期元素的原子所形成的简单离子中:还原性最弱的阴离子是_______ ;对第三周期简单阳离子的离子半径由大到小进行排列_______ 。
II.活火山的火山口往往有硫磺矿物富集,是人类获得硫磺的主要来源之一,人们利用硫磺可以制备例如浓硫酸等许多有用的含硫化合物。
(5)下列不能由硫单质和其他单质化合生成的物质是_______。
(6)硫磺和过氧化钠都是淡黄色固体,如何鉴别某固体物质为硫磺或过氧化钠:____ 。硫单质有多种结构,例如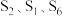 和
和 等,它们互称
等,它们互称_______ ,已知 中S原子最外层满足8电子稳定结构,且
中S原子最外层满足8电子稳定结构,且 结构中仅有硫硫单键,计算
结构中仅有硫硫单键,计算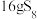 固体中共价键的数目为
固体中共价键的数目为_______ 。
III.火山喷发产生的气体中含有 ,经过一系列化学反应最终能转变为硫磺。
,经过一系列化学反应最终能转变为硫磺。
(7)写出 的结构式
的结构式_______ , 是一种具有强还原性的二元弱酸,写出
是一种具有强还原性的二元弱酸,写出 在水溶液中的电离方程式
在水溶液中的电离方程式_______ 、_______ 。
(8) 从火山口喷出后在空气中转变化
从火山口喷出后在空气中转变化 ,写出有关化学反应方程式
,写出有关化学反应方程式__ ,之后生成的 与剩余
与剩余 继续反应形成硫磺,
继续反应形成硫磺, 与
与 反应产物中氧化产物与还原产物的比例为
反应产物中氧化产物与还原产物的比例为_______ 。
IV. 是海洋中硫元素的主要存在形式之一。
是海洋中硫元素的主要存在形式之一。
(9)海水中硫酸根离子含量大约为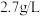 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法_______ 。
(10)粗盐提纯时,除去粗盐中的硫酸根离子,经常向溶液中加入_______ (填写试剂化学式)。该物质的固体熔点_______ (填写“大于”或“小于”) 的熔点。
的熔点。
V.人们合成的许多硫的化合物具有奇妙的性质
(11)人类合成了一系列的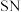 二元化合物,其中线性的
二元化合物,其中线性的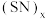 是具有类似黄铜的金属光泽和导电性,其结构片段为:
是具有类似黄铜的金属光泽和导电性,其结构片段为: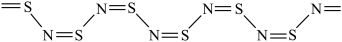 ,以下说法正确的是_______。
,以下说法正确的是_______。
(12) 与酸反应时生成
与酸反应时生成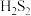 ,
,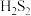 与
与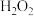 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是_______。
颗粒混合,不可能生成的物质是_______。
(13) 在酸性环境中的氧化性比
在酸性环境中的氧化性比 还要强,实验室可以用无色的酸性
还要强,实验室可以用无色的酸性 溶液来检验
溶液来检验 (溶液几乎无色),原理如下所示:
(溶液几乎无色),原理如下所示:
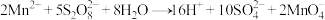
 的结构如图所示:
的结构如图所示:
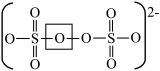
①已知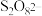 中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态
中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态_______ ,并标明上述反应的电子转移方向与数目_______ 。
②确认溶液中是否含 的现象是:
的现象是:_______ 。

(1)生物体内多种蛋白质含有硫元素,硫与同主族的氧元素相比,非金属性S
(2)已知
 与硫元素属于同一主族,原子序数比硫大18,写出
与硫元素属于同一主族,原子序数比硫大18,写出 在元素周期表的位置
在元素周期表的位置 原子的原子结构示意图
原子的原子结构示意图(3)O、S和
 都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。
都是第ⅥA族的元素,关于这三种元素原子的说法正确的是_____。A.O的原子半径>S的原子半径 的原子半径 的原子半径 | B.最外层电子数都相同 |
| C.核外电子层数都相同 | D.最外层电子数都不相同 |
II.活火山的火山口往往有硫磺矿物富集,是人类获得硫磺的主要来源之一,人们利用硫磺可以制备例如浓硫酸等许多有用的含硫化合物。
(5)下列不能由硫单质和其他单质化合生成的物质是_______。
A. | B. | C. | D. |
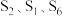 和
和 等,它们互称
等,它们互称 中S原子最外层满足8电子稳定结构,且
中S原子最外层满足8电子稳定结构,且 结构中仅有硫硫单键,计算
结构中仅有硫硫单键,计算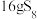 固体中共价键的数目为
固体中共价键的数目为III.火山喷发产生的气体中含有
 ,经过一系列化学反应最终能转变为硫磺。
,经过一系列化学反应最终能转变为硫磺。(7)写出
 的结构式
的结构式 是一种具有强还原性的二元弱酸,写出
是一种具有强还原性的二元弱酸,写出 在水溶液中的电离方程式
在水溶液中的电离方程式(8)
 从火山口喷出后在空气中转变化
从火山口喷出后在空气中转变化 ,写出有关化学反应方程式
,写出有关化学反应方程式 与剩余
与剩余 继续反应形成硫磺,
继续反应形成硫磺, 与
与 反应产物中氧化产物与还原产物的比例为
反应产物中氧化产物与还原产物的比例为IV.
 是海洋中硫元素的主要存在形式之一。
是海洋中硫元素的主要存在形式之一。(9)海水中硫酸根离子含量大约为
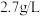 ,会干扰海水中
,会干扰海水中 的检验,写出检验海水中
的检验,写出检验海水中 的实验方法
的实验方法(10)粗盐提纯时,除去粗盐中的硫酸根离子,经常向溶液中加入
 的熔点。
的熔点。V.人们合成的许多硫的化合物具有奇妙的性质
(11)人类合成了一系列的
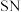 二元化合物,其中线性的
二元化合物,其中线性的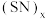 是具有类似黄铜的金属光泽和导电性,其结构片段为:
是具有类似黄铜的金属光泽和导电性,其结构片段为: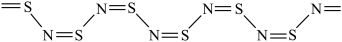 ,以下说法正确的是_______。
,以下说法正确的是_______。| A.是共价化合物 | B.酸性: ,所以非金属性 ,所以非金属性 |
| C.为离子化合物 | D.所有原子最外层都是8电子 |
 与酸反应时生成
与酸反应时生成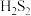 ,
,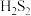 与
与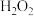 相似,易分解。实验室用过量稀硫酸与
相似,易分解。实验室用过量稀硫酸与 颗粒混合,不可能生成的物质是_______。
颗粒混合,不可能生成的物质是_______。A. | B.S | C. | D. |
 在酸性环境中的氧化性比
在酸性环境中的氧化性比 还要强,实验室可以用无色的酸性
还要强,实验室可以用无色的酸性 溶液来检验
溶液来检验 (溶液几乎无色),原理如下所示:
(溶液几乎无色),原理如下所示: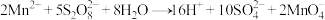
 的结构如图所示:
的结构如图所示:
①已知
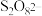 中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态
中所有氧原子均满足8电子稳定结构,写出用粗方框圈出的氧原子的价态②确认溶液中是否含
 的现象是:
的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:
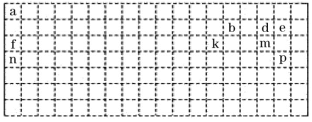
(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。_______
(2)表中最活泼的金属与最活泼的非金属形成的物质是_______ (填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:____ ,这两种化合物中所含的化学键有____ (填字母)。
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为___ (填离子符号)。
(5)e、p对应的离子还原性由强到弱顺序为_____ (填离子符号)。
(6)d、e、m的气态氢化物中,最不稳定的是_______ (填化学式)。
(7)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:________ 。

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。
(2)表中最活泼的金属与最活泼的非金属形成的物质是
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为
(5)e、p对应的离子还原性由强到弱顺序为
(6)d、e、m的气态氢化物中,最不稳定的是
(7)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】随着原子序数的递增, 种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。请用相应的化学用语回答下列问题:
种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。请用相应的化学用语回答下列问题:

(1)元素F在元素周期表中的位置是_______ ,元素C的简单气态氢化物的电子式是 _________ 。
(2)分子式为B2A6D的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是________ 。
(3)元素D、G的单质中,氧化性较强的是_______________ (填化学式),元素E、F的最高价氧化物的水化物反应的离子方程式为________________ 。
(4)化合物BD2由固态变为气态需克服的微粒间作用力是_________________ ,由D、E元素按照原子个数比为1:1组成的化合物中所含的化学键是____________________ 。
(5)写出由A、C、H三种元素形成的离子化合物的化学式_______________ 。
(6)化合物E3C遇水反应生成氨气NH3和一种强碱,反应的化学方程式为______________ 。
 种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。请用相应的化学用语回答下列问题:
种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。请用相应的化学用语回答下列问题:
(1)元素F在元素周期表中的位置是
(2)分子式为B2A6D的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是
(3)元素D、G的单质中,氧化性较强的是
(4)化合物BD2由固态变为气态需克服的微粒间作用力是
(5)写出由A、C、H三种元素形成的离子化合物的化学式
(6)化合物E3C遇水反应生成氨气NH3和一种强碱,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】①NH3 ②CO2 ③SiCl4 ④BF3 ⑤C2H4 ⑥H2O2 ⑦Cl2 ⑧P4 ⑨H2S
(1)含极性共价键的非极性分子___________ (填序号,下同)
(2)含非极性共价键的非极性分子___________
(3)含极性共价键的极性分子___________
(4)①NH3中心原子杂化方式___________ 分子的空间构型___________
(5)④BF3中心原子杂化方式___________ 分子的空间构型___________
(1)含极性共价键的非极性分子
(2)含非极性共价键的非极性分子
(3)含极性共价键的极性分子
(4)①NH3中心原子杂化方式
(5)④BF3中心原子杂化方式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有__ 种,氟原子的价电子排布图为__ .
(2)与HF2- 互为等电子体的分子有___ (写一个)。
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为__ 。
Ⅱ.下列变化中①NaCl 溶于水 ②HCl 溶于水 ③ 葡萄糖溶于水
④Na2O2溶于水 ⑤ I2升华 ⑥固体NaOH熔化。
未发生化学键破坏的是_____ ,仅发生离子键破坏的是________ ,仅发生共价键破坏的是_______ ,既发生离子键破坏,又发生共价键破坏的是____________ (填序号)。
(1)基态氟原子核外电子的运动状态有
(2)与HF2- 互为等电子体的分子有
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为
Ⅱ.下列变化中①NaCl 溶于水 ②HCl 溶于水 ③ 葡萄糖溶于水
④Na2O2溶于水 ⑤ I2升华 ⑥固体NaOH熔化。
未发生化学键破坏的是
您最近一年使用:0次



