如图是元素周期表的一部分,A~J代表对应的元素,回答下列问题:
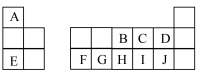
(1)F的元素符号为___________ ,元素C在周期表中的位置为___________ 。
(2)A、D和E三种元素的离子半径由大到小的顺序是___________ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(4)A、B和J三种元素形成常见化合物所含化学键的类型是___________ 。
(5)下列说法错误的是___________ (填标号)。
a.单质的熔点:
b.简单氢化物的沸点:
c.氧化物对应水化物的酸性:
(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为___________ 。

(1)F的元素符号为
(2)A、D和E三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、B和J三种元素形成常见化合物所含化学键的类型是
(5)下列说法错误的是
a.单质的熔点:

b.简单氢化物的沸点:

c.氧化物对应水化物的酸性:

(6)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
更新时间:2023-09-12 12:52:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请回答有关问题:
(1)元素⑥的原子结构示意图___________ ;写出⑤的氧化物的一种用途__________ 。
(2)表中⑤和⑥气态氢化物的稳定性顺序为______ >______ (填氢化物的化学式);
(3)表中能形成两性氢氧化物的元素是_________ (填元素符号),该元素的单质与③的氢氧化物水溶液反应的离子反应方程式_______________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第2周期 | ① | ② | ||||||
| 第3周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)元素⑥的原子结构示意图
(2)表中⑤和⑥气态氢化物的稳定性顺序为
(3)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、h分别代表某种化学元素。请依据这8种元素回答下列问题。
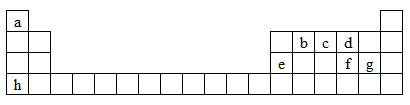
(1)上述8种元素的单质中常温下为气态,且密度最小的是______ (填化学式)。
(2)f元素的原子结构示意图为_______ 。
(3)c的最高价氧化物对应水化物的化学式为______ 。
(4)hg的电子式为_______ 。
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是______ (填化学式)。
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为__________ 。
(7)f元素的最简单氢化物的水溶液显____ 性(填“酸”或“碱”),请写出该氢化物久置在空气中变质的化学方程式________ 。
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为__________ 。

(1)上述8种元素的单质中常温下为气态,且密度最小的是
(2)f元素的原子结构示意图为
(3)c的最高价氧化物对应水化物的化学式为
(4)hg的电子式为
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为
(7)f元素的最简单氢化物的水溶液显
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表中前7周期的元素数目如表所示(假设第7周期已排满):
(1)第6、7周期比第4、5周期多了14种元素,其原因是_______ 。
(2)周期表中_______ 族所含元素最多。
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为_______ 。
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第_______ 周期第_______ 纵列。
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期比第4、5周期多了14种元素,其原因是
(2)周期表中
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素周期律
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
(2) 的电子式正确的是________
的电子式正确的是________
(3)有关N、O两种元素,下列排序错误的是________
(4)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是________
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
A. | B. | C. | D. |
 的电子式正确的是________
的电子式正确的是________A.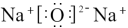 | B. |
C.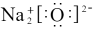 | D. |
| A.元素的最高化合价:O>N | B.简单氢化物的稳定性: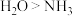 |
| C.元素的电负性:O>N | D.离子半径: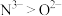 |
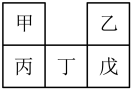
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,第一电离能最大的元素是___________ ,电负性最小的金属元素是___________ 。
(2)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是___________ 。
(3)②③④三种元素形成的离子,离子半径由大到小的顺序是___________ 。
(4)①和⑨的最高价氧化物对应水化物的化学式分别为___________ 、___________ 。
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:___________ 。
(7)⑨元素的价层电子轨道表示式为___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第二周期 | ⑥ | ⑦ | ||||||
| 第三周期 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 第四周期 | ② | ④ | ⑨ |
(2)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)②③④三种元素形成的离子,离子半径由大到小的顺序是
(4)①和⑨的最高价氧化物对应水化物的化学式分别为
(5)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的过程:
(7)⑨元素的价层电子轨道表示式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列数字①~⑨分别代表某种化学元素。请依据这9种元素回答下列问
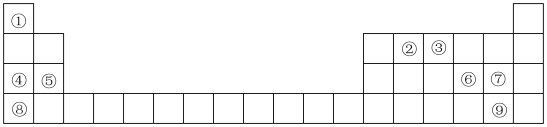
(1)非金属性最强的元素是_______ 。(填元素符号 )
(2)⑨的最高价氧化物对应水化物的化学式是_______ 。(填化学式 )
(3)表中 某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_______ (填离子符号)。
(4)任意例举一个实验事实说明金属性④>⑤:_______ 。
(5)化合物M由9种元素中2种元素甲、乙组成,M电子式可表示为 ,则M化学式为
,则M化学式为_______ 。(填元素符号 )
(6)1971年在星际空间发现一种由①、②、③三种元素组成的直线型分子X。X的摩尔质量为51g·mol-1,且X分子中共含5个原子(各原子均满足稀有气体原子的稳定结构),X分子式为_______ ,结构式为_______ 。

(1)非金属性最强的元素是
(2)⑨的最高价氧化物对应水化物的化学式是
(3)
(4)任意例举一个实验事实说明金属性④>⑤:
(5)化合物M由9种元素中2种元素甲、乙组成,M电子式可表示为
 ,则M化学式为
,则M化学式为(6)1971年在星际空间发现一种由①、②、③三种元素组成的直线型分子X。X的摩尔质量为51g·mol-1,且X分子中共含5个原子(各原子均满足稀有气体原子的稳定结构),X分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用“>”或“<”回答下列问题:
(1)酸性:H2CO3___________ H2SiO3,H2SiO3___________ H3PO4
(2)碱性:Ca(OH)2___________ Mg(OH)2,Mg(OH)2___________ Al(OH)3
(3)气态氢化物稳定性: H2O_______ H2S,H2S________ HCl。
(4)酸性:H2SO4_______ H2SO3,HClO4_______ HClO。
(5)还原性:H2O___________ H2S,H2S___________ HCl。
从以上答案中可以归纳出:
(6)元素的非金属性越强,其对应的最高价氧化物的水化物酸性越________ 。
(7)元素的金属性越强,其对应最高价氧化物水化物的碱性越_______ 。
(8)元素的_____ 性越强,其对应气态氢化物的稳定性越______ 。
(9)元素非金属性越强,其气态氢化物的还原性越_____ 。
(10)同种非金属元素形成的含氧酸,成酸元素价态越高,其酸性也越___________ 。
(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)气态氢化物稳定性: H2O
(4)酸性:H2SO4
(5)还原性:H2O
从以上答案中可以归纳出:
(6)元素的非金属性越强,其对应的最高价氧化物的水化物酸性越
(7)元素的金属性越强,其对应最高价氧化物水化物的碱性越
(8)元素的
(9)元素非金属性越强,其气态氢化物的还原性越
(10)同种非金属元素形成的含氧酸,成酸元素价态越高,其酸性也越
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列物质:①HCl、②CO2、③H2O、④NaOH、⑤Cl2、⑥NaHSO4、⑦MgCl2、⑧CaO、⑨He请回答下列问题。
(1)NaOH是以___________ 化学键结合的;不含化学键的物质是___________ (填序号)。
(2)写出CO2的电子式___________ ;用电子式表示MgCl2的形成过程___________ 。
(3)存在分子间作用力的物质有___________ (填序号)。
(4)哪些物质属于离子化合物___________ (填序号);哪些物质属于共价化合物___________ (填序号)。
(5)HCl溶于水时,断开的化学键类型是___________ ;NaHSO4加热熔化时,断开的化学键类型是___________ 。
(1)NaOH是以
(2)写出CO2的电子式
(3)存在分子间作用力的物质有
(4)哪些物质属于离子化合物
(5)HCl溶于水时,断开的化学键类型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)前四周期中的一部分如图,若B元素原子序数为x,则A、C、D、E原子序数之和为( )

(2)核内中子数为N的R2+,质量数为A,则它的n g氧化物中所含质子的物质的量是( ) mol
(3)最外层电子数为2的元素有_______ (填元素符号,下同)。
最外层电子数与次外层电子数相等的元素有________
(4)在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是____ 、 ____ 、 ____________________

(2)核内中子数为N的R2+,质量数为A,则它的n g氧化物中所含质子的物质的量是
(3)最外层电子数为2的元素有
最外层电子数与次外层电子数相等的元素有
(4)在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在1~18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
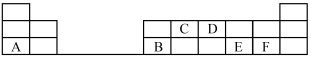
(1)写出D单质的电子式:___________ 。
(2)写出C的最高价氧化物的结构式:___________ 。
(3)E和F分别形成的气态氢化物中较稳定的是___________ (填氢化物的化学式)。
(4)A最高价氧化物的水化物所含化学键为___________ ,其水溶液与F单质反应的离子方程式为___________ 。

(1)写出D单质的电子式:
(2)写出C的最高价氧化物的结构式:
(3)E和F分别形成的气态氢化物中较稳定的是
(4)A最高价氧化物的水化物所含化学键为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______ (填序号,下同);
(2)互为同素异形体的是_____ ;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___ 种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____ ;
(2)用电子式表示二氧化碳分子的形成过程_________ ;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______ (填序号,下同);
(2)含有极性键的离子化合物是_________ ;
(3)氟化氢水溶液中存在的氢键有________ 种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____ 。
(1)互为同位素的是
(2)互为同素异形体的是
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式
(2)用电子式表示二氧化碳分子的形成过程
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是
(2)含有极性键的离子化合物是
(3)氟化氢水溶液中存在的氢键有
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】①NH3 ②CO2 ③SiCl4 ④BF3 ⑤C2H4 ⑥H2O2 ⑦Cl2 ⑧P4 ⑨H2S
(1)含极性共价键的非极性分子___________ (填序号,下同)
(2)含非极性共价键的非极性分子___________
(3)含极性共价键的极性分子___________
(4)①NH3中心原子杂化方式___________ 分子的空间构型___________
(5)④BF3中心原子杂化方式___________ 分子的空间构型___________
(1)含极性共价键的非极性分子
(2)含非极性共价键的非极性分子
(3)含极性共价键的极性分子
(4)①NH3中心原子杂化方式
(5)④BF3中心原子杂化方式
您最近一年使用:0次



