几种主族元素在周期表中的位置如表:
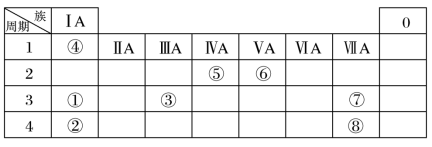
根据表回答下列问题:
(1)⑤元素的简单氢化物的电子式是_____ 、⑤的最高价氧化物结构式_____ 。
(2)①②③三种元素原子半径由大到小的顺序是____ (用元素符号表示)。
(3)表中8种元素中,最高价氧化物有两性的元素的原子结构示意图为_____ ,该元素在周期表中的位置是____ 。
(4)⑤⑥⑦三种元素最高价氧化物对应水化物酸性最强的是_____ (填化学式),②与③最高价氧化物对应水化物反应的化学方程式为_____ 。
(5)非金属性强弱比较⑦_____ ⑧(填写“大于”或“小于”)下列表述中能证明这一事实的是_____ (填字母)。
a.⑦的氢化物比⑧的氢化物水溶液酸性弱
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的简单阴离子的还原性比⑧的简单阴离子的还原性弱
(6)③与⑦形成的化合物是_____ (填“离子”或“共价”)化合物。

根据表回答下列问题:
(1)⑤元素的简单氢化物的电子式是
(2)①②③三种元素原子半径由大到小的顺序是
(3)表中8种元素中,最高价氧化物有两性的元素的原子结构示意图为
(4)⑤⑥⑦三种元素最高价氧化物对应水化物酸性最强的是
(5)非金属性强弱比较⑦
a.⑦的氢化物比⑧的氢化物水溶液酸性弱
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的简单阴离子的还原性比⑧的简单阴离子的还原性弱
(6)③与⑦形成的化合物是
更新时间:2023-03-10 02:16:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】人体必需的一些元素在周期表中的分布情况如图:
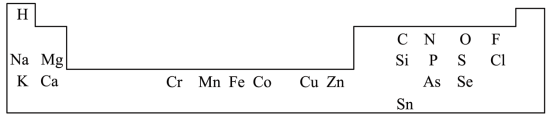
(1)请写出 Si 在周期表的位置_______
(2)S 、Cl 、K 元素对应的简单离子半径由小到大的顺序_______ (用离子符号表示)
(3)锡(Sn)与 C 为同一主族元素,Sn 原子比 C 原子多三个电子层, 则 Sn 的原子序数为_______
(4)X 射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是_______ (填字母)
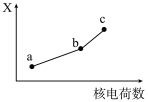
(5)前四周期同族元素的某种性质 X 随核电荷数的变化趋势如图所示, 则下列说法正确的是_______
(6)铬是胰岛素不可缺少的辅助成分,但食用不当也会带来很大的危害。六价铬的化合物有剧毒,所以要对 Cr(Ⅵ)(罗马数字表示元素的化合价, 下同)废水进行化学处理,可转化为重要产品磁性铁铬氧体(CrxFeyOz):先向含CrO 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出CrO 在酸性条件下被Fe2+还原为Cr3+的离子方程式:
在酸性条件下被Fe2+还原为Cr3+的离子方程式:_______
②若处理含 1molCrO (不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为_______

(1)请写出 Si 在周期表的位置
(2)S 、Cl 、K 元素对应的简单离子半径由小到大的顺序
(3)锡(Sn)与 C 为同一主族元素,Sn 原子比 C 原子多三个电子层, 则 Sn 的原子序数为
(4)X 射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl |  | CO2 |  |
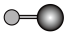 | 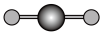 | 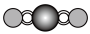 | 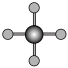 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |

| A.若 a、b 、c 表示碱金属元素, 则 X 表示对应单质的密度 |
| B.若 a 、b 、c 表示卤族元素, 则 X 表示对应简单离子的还原性 |
| C.若 a 、b 、c 表示氧族元素, 则 X 表示对应氢化物的稳定性 |
| D.若 a、b 、c 表示第ⅡA 族元素,则 X 表示最高价氧化物对应水化物的碱性 |
 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气 (氧化部分Fe2+ )并加入 NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出CrO
 在酸性条件下被Fe2+还原为Cr3+的离子方程式:
在酸性条件下被Fe2+还原为Cr3+的离子方程式:②若处理含 1molCrO
 (不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
(不考虑其他含铬微粒)的污水时恰好消耗 10molFeSO4,则当铁铬氧体中n (Fe2+):n(Fe3+ )=3:2 时,铁铬氧体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Q、R、T、W、X、Y、Z为原子序数依次增大的前四周期元素,其中R、T、W是同周期相邻元素,Q、R最外层电子排布可表示为asa,bsbbpa(a≠b):X的基态原子中占据哑铃形原子软道的电子数为10,Y与X为同周期主族元素,基态Z原子核外电子填充在7个能级中,且价层电子有3对成对电子。
(1)四种分子①RY3②TQ4③WQ3④Q2X键角由大到小排列的顺序是_____________ (填序号).
(2)微粒W3-的空间构型为_____________ 。
(3)XTW-的等电子体中属于分子的有_____________ (填化学式,写出一种即可),XTW-的电子式为_____________ ;
(4)R的某种钠盐晶体,其阴离子Mm-(含Q、R、O三种元素)的球棍模型如下图所示:在Mm-中,R原子轨道杂化类型为_____________ ,m=_____________ 。(填数字)

(5)T的某种单质的片层与层状结构如图1所示.其中层间距离为xpm,图2为从结构中取出的晶胞,若晶胞的边长为ypm,则T的该种单质的密度为_____________ g•cm-3。(1pm=10-12m)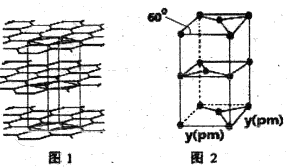
(1)四种分子①RY3②TQ4③WQ3④Q2X键角由大到小排列的顺序是
(2)微粒W3-的空间构型为
(3)XTW-的等电子体中属于分子的有
(4)R的某种钠盐晶体,其阴离子Mm-(含Q、R、O三种元素)的球棍模型如下图所示:在Mm-中,R原子轨道杂化类型为

(5)T的某种单质的片层与层状结构如图1所示.其中层间距离为xpm,图2为从结构中取出的晶胞,若晶胞的边长为ypm,则T的该种单质的密度为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下面为元素周期表的一部分,根据元素① ~⑧在表中的位置回答下列问题。

(1)元素④的原子结构示意图为___________ ,元素⑦在自然界的存在形态是__________ 。
(2)用电子式表示元素⑤、⑧形成化合物的过程_____________ 。
(3)元素①③形成的最简单氢化物化学式是__________ ,写出实验室制备此物质的化学方程式___________ 。
(4)元素⑥的单质与磁性氧化铁反应的化学方程式___________ 。
(5)由元素②形成的只有三种同分异构体的烷烃是_________ (填化学式),这三种同分异构体的结构简式分别是CH3CH2CH2CH2CH3、___________ 、___________ 。

(1)元素④的原子结构示意图为
(2)用电子式表示元素⑤、⑧形成化合物的过程
(3)元素①③形成的最简单氢化物化学式是
(4)元素⑥的单质与磁性氧化铁反应的化学方程式
(5)由元素②形成的只有三种同分异构体的烷烃是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白。
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___ 。
(2)④与⑤两种元素相比较,原子半径较大的是___ (填元素符号);在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是___ (填化学式)。在金属元素氧化物所对应的水化物中,碱性最强的化合物是___ (填化学式),具有两性的化合物是___ (填化学式)。
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为___ (填化学式)。
(4)元素①和元素⑦形成化合物属于___ 化合物(填“离子”或者“共价”)。请用电子式表示⑥和④组成化合物的形成过程:________ 。
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:______________ 。
| 主族\周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)④与⑤两种元素相比较,原子半径较大的是
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为
(4)元素①和元素⑦形成化合物属于
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化合物Q用作铝、铜和铝合金焊接助熔剂,结构如图所示, X、Y、Z、W为原子序数依次增大的主族元素,最外层电子数均为奇数且质子数之和为22。则X、Y、Z、W分别是________________ (填元素符号)。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表为元素周期表的一部分,用请化学用语回答有关问题:
(1)C和H的元素符号是______ 和_______ ;
(2)表中A与F的氢化物反应的化学方程式___________ ,E的单质与其下一周期同族元素的最高价氧化物在高温下反应的化学方程式___________ ;最不活泼的元素________ (填写元素符号)
(3)表中所列元素中最高价氧化物对应水化物碱性最强的是___________ ,酸性最强的是______ (填写化学式)
(4)表中能形成两性氢氧化物的元素是__________ (填写元素符号),写出该元素的氢氧化物与A的最高价氧化物对应水化物反应的离子方程式__________________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)C和H的元素符号是
(2)表中A与F的氢化物反应的化学方程式
(3)表中所列元素中最高价氧化物对应水化物碱性最强的是
(4)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)④、③、⑧三种元素中,离子半径由大到小的顺序为:___ (填离子符号)。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是:___ (填化学式)。
(3)⑥单质与⑨的最高价氧化物对应的水化物反应的化学方程式为:___ 。
(4)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___ 。
(5)能说明⑧的非金属性比⑨的非金属性弱的事实是:___ (用离子方程式说明)。
(6)①和③形成的18电子的化合物甲是一种应用广泛的化工原料,写出甲的结构式:___ 。实验室中可用次氯酸钠溶液与氨反应制备甲,反应的化学方程式为:___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是:
(3)⑥单质与⑨的最高价氧化物对应的水化物反应的化学方程式为:
(4)①、④、⑤、⑨四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(5)能说明⑧的非金属性比⑨的非金属性弱的事实是:
(6)①和③形成的18电子的化合物甲是一种应用广泛的化工原料,写出甲的结构式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用钴酸锂(LiCoO2) 代替锂是锂电池的巨大突破之一、工业上可用LiOH制备LiCoO2。完成下列填空:
(1)锂原子核外的3个电子_______(选填选项)
(2)请将Li、O、H的原子半径和简单离子的半径分别按由小到大的顺序排列:_______ (用元素符号表示)、_______ (用离子符号表示)。
(3)如何证明LiOH是离子化合物?_______ 。
(4)元素周期表中,钴、铁同族且都属于过渡元素,可在这一区域的元素中寻找_______(选填选项)
(5)将LiCoO2、石墨和稀硫酸构成电解池,LiCoO2可转化成Li2SO4和CoSO4,LiCoO2作_______ 极,该电极上还可能发生副反应生成某气体,该气体是_______ 。
(6)LiCoO2可转化为CoC2O4·2H2O。加热CoC2O4·2H2O,固体残留物质量变化如图所示。
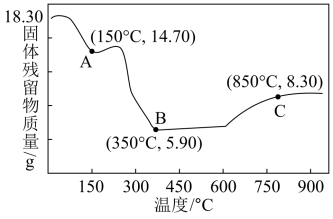
600℃之前隔绝空气加热,600℃之后在空气中加热,A、B、C三点的产物均为纯净物。已知M(CoC2O4·2H2O)=183,则B生成C的化学方程式是:_______ 。
(1)锂原子核外的3个电子_______(选填选项)
| A.具有两种能量 | B.分占三个轨道 |
| C.具有两种运动状态 | D.电子云形状相同 |
(3)如何证明LiOH是离子化合物?
(4)元素周期表中,钴、铁同族且都属于过渡元素,可在这一区域的元素中寻找_______(选填选项)
| A.半导体材料 | B.催化剂 |
| C.高效农药 | D.耐高温、耐腐蚀合金材料 |
(6)LiCoO2可转化为CoC2O4·2H2O。加热CoC2O4·2H2O,固体残留物质量变化如图所示。

600℃之前隔绝空气加热,600℃之后在空气中加热,A、B、C三点的产物均为纯净物。已知M(CoC2O4·2H2O)=183,则B生成C的化学方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知: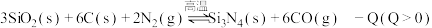 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子占有_______ 种能量不同的轨道。 属于
属于_______ 晶体。
(5)非金属性:S小于O。试用一个实验事实说明_______ 。
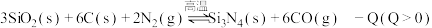 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子占有
 属于
属于(5)非金属性:S小于O。试用一个实验事实说明
您最近一年使用:0次



