名校
1 . 下列说法正确的是
| A.当L层上的电子数为奇数时,M层上不可能有电子 |
| B.同一主族中,相邻周期元素原子的核电荷数相差值一定为8或18或32 |
| C.同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大 |
| D.同一周期中,IIA与IIIA族元素原子的核电荷数都相差1 |
您最近一年使用:0次
2024-02-23更新
|
168次组卷
|
5卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
解题方法
2 . 人体必需的一些元素在周期表中的分布情况如下:
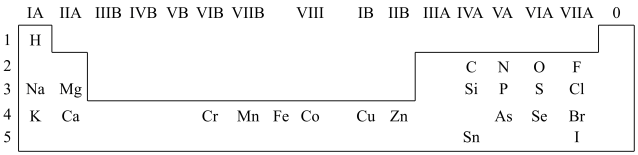
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
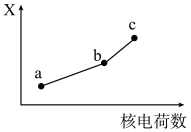
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
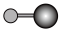 | 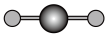 | 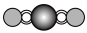 | 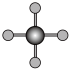 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近一年使用:0次
名校
解题方法
3 . 对于前四周期元素,下列说法正确的是
| A.基态原子的N层上只有一个电子的元素,一定是IA族元素 |
| B.原子的最外层电子排布为ns2的元素一定是主族元素 |
| C.基态原子的p能级上半充满的元素一定位于p区 |
D.基态原子的价电子排布为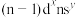 的元素的族序数一定为x+y 的元素的族序数一定为x+y |
您最近一年使用:0次
4 . 下列说法正确的是
| A.d区、ds区、s区元素全部是金属元素 |
| B.在周期表中,假设第八周期按照现有规则填满,则最后一个元素是168号元素 |
| C.第四周期元素中,未成对电子数最多的主族元素位于钾元素后面第五位 |
D.气态 再失去一个电子比气态 再失去一个电子比气态 再失去一个电子容易 再失去一个电子容易 |
您最近一年使用:0次
2024-02-18更新
|
216次组卷
|
2卷引用:广东省汕头市金山中学2023-2024学年高二上学期期末考试 化学试题
名校
5 . 下列关于原子结构及元素周期表的说法错误的是
A.第ⅡA族基态原子最外层电子排布均为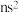 |
| B.第三、四周期同主族元素的原子序数均相差8 |
| C.元素周期表有3个短周期4个长周期 |
D.除第一周期外,其余各周期的原子核外电子排布总是从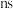 开始,以 开始,以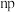 结束 结束 |
您最近一年使用:0次
名校
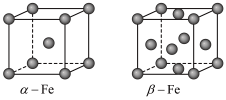
6 . 因生产金属铁的工艺和温度不同,产生的铁单质的晶体结构、密度和性质均不同,铁的晶体中铁原子有三种堆积方式,其中两种立方晶胞结构如图所示。下列关于铁或其晶胞的说法中正确的是
| A.铁在周期表中位于第四周期第VIIIB族,是过渡元素也是副族元素 |
| B.在两种晶胞中,每个Fe原子周围均有8个与之距离相等且最近的Fe原子 |
C.若ɑ-Fe晶胞边长为bpm,则Fe原子半径r= bpm bpm |
D.若β-Fe晶胞中最近的两个Fe原子核间距为apm,阿伏加德罗常数为NA,晶胞的密度表达式是 |
您最近一年使用:0次
名校
7 . 下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近一年使用:0次
8 . 处于s区、d区、ds区和f区的元素全部是金属元素。(_____)
您最近一年使用:0次
名校
解题方法
9 . 铁及其化合物在工农业生产中应用广泛,部分含铁物质的分类与相应化合价关系如图所示。下列说法错误的是
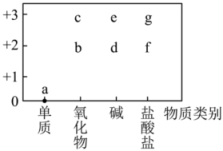

| A.g、f均可由化合反应来制备 | B. 在周期表中处在第四周期第VIIIB族 在周期表中处在第四周期第VIIIB族 |
C.a在纯氧中燃烧,可生成 | D.能用KSCN溶液鉴别g溶液和f溶液 |
您最近一年使用:0次
2023-12-23更新
|
239次组卷
|
2卷引用:湖南省长沙市南雅中学2023-2024学年高一上学期第三次12月月考化学试卷
10 . 下列说法正确的是
| A.对轨道模型贡献最大的科学家是汤姆生 |
| B.充有氖气的霓虹灯管通电时,灯管发出的红色光属于发射光谱 |
C.在基态多电子原子中, 轨道电子的能量一定高于 轨道电子的能量一定高于 轨道电子的能量 轨道电子的能量 |
D.根据原子核外电子排布的特点可知, 在元素周期表中属于 在元素周期表中属于 区元素 区元素 |
您最近一年使用:0次



