解题方法
1 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了6种元素在周期表中的位置,其中①~③代表3种元素。
(1)①的元素符号是_______ 。
(2)下列能说明 比
比 失电子能力强的事实是
失电子能力强的事实是_______ (填字母)。
 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢
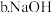 是强碱,
是强碱, 是中强碱
是中强碱
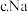 的密度比
的密度比 的小
的小
(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,_______ ,原子半径②小于③,得电子能力②强于③。
(4)依据元素周期律,预测气态氢化物的热稳定性: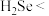
_______ (填写化学式,一种即可)。
| \ | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ||||||||
| 3 |  |  | ① | ② | ||||
| 4 |  | ③ |
(2)下列能说明
 比
比 失电子能力强的事实是
失电子能力强的事实是 比
比 更容易与水反应置换出氢
更容易与水反应置换出氢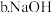 是强碱,
是强碱, 是中强碱
是中强碱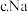 的密度比
的密度比 的小
的小(3)非金属性②强于③,用原子结构解释原因:②和③位于同一主族,最外层电子数相同,
(4)依据元素周期律,预测气态氢化物的热稳定性:
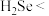
您最近一年使用:0次
2 . 下表是元素周期表中主族的一部分,其中c是地壳中含量最多的元素,回答下列问题:__________ , 的结构式为
的结构式为___________ 。
(2)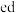 为
为__________ (填“离子”或“共价”)化合物,能证明该结论的实验依据为___________ .
(3)用电子式表示物质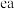 的形成过程
的形成过程__________________ ,该物质能与 反应生成
反应生成 ,反应中
,反应中 作
作________ 剂。
(4) 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为_________ (用化学式表示)。
(5)若 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: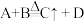 ,写出该反应的离子方程式
,写出该反应的离子方程式____________________ 。
(6)下列有关说法正确的是__________ 。
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用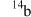 测定一些文物的年代
测定一些文物的年代
C.科学家常在 等元素区域寻找新型农药
等元素区域寻找新型农药
D.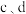 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
 的结构式为
的结构式为(2)
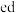 为
为(3)用电子式表示物质
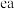 的形成过程
的形成过程 反应生成
反应生成 ,反应中
,反应中 作
作(4)
 最高价氧化物水化物的碱性由强到弱的顺序为
最高价氧化物水化物的碱性由强到弱的顺序为(5)若
 均为上述元素形成的10电子微粒,相互之间能发生离子反应:
均为上述元素形成的10电子微粒,相互之间能发生离子反应: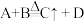 ,写出该反应的离子方程式
,写出该反应的离子方程式(6)下列有关说法正确的是
A.a和e最外层电子数相同,均为碱金属元素 B.考古时利用
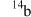 测定一些文物的年代
测定一些文物的年代C.科学家常在
 等元素区域寻找新型农药
等元素区域寻找新型农药D.
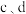 形成阴离子时,c原子得到的电子更多,所以非金属性
形成阴离子时,c原子得到的电子更多,所以非金属性
您最近一年使用:0次
3 . 下表为八种短周期主族元素的部分性质(已知铍的原子半径为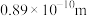 ):
):
(1)元素Z在元素周期表中的位置为___________ ,元素Y为___________ (填元素符号)。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:___________ 。
(3)R与T相比,非金属性较强的是___________ (填元素符号),下列事实能证明这一结论的是___________ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: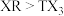
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是___________ (填元素符号),能证明这一结论的依据是___________ 。
(5)根据表中数据推测,M的原子半径的最小范围是___________ 。
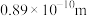 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 | r | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
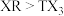
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
解题方法
4 . 下表列出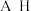 八种元素在周期表中的位置:
八种元素在周期表中的位置:
回答下列问题:
(1) 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是___________ (填元素符号,下同)。
(2)写出 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:___________ 。
(3)这八种元素中非金属性最强的元素是___________ 。
(4)写出 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:___________ 。
(5) 的氢化物属于
的氢化物属于___________ (填“离子化合物”或“共价化合物”)。
该氢化物与水反应的化学方程式为___________ 。
(6) 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
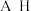 八种元素在周期表中的位置:
八种元素在周期表中的位置:| 周期 | 主族 | ||||||
Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
| 2 |  |  |  | ||||
| 3 |  |  |  |  | |||
| 4 |  | ||||||
(1)
 、
、 、
、 三种元素中,原子半径最大的是
三种元素中,原子半径最大的是(2)写出
 与
与 两元素最高价氧化物对应水化物反应的离子方程式:
两元素最高价氧化物对应水化物反应的离子方程式:(3)这八种元素中非金属性最强的元素是
(4)写出
 、
、 两元素形成的原子个数比为
两元素形成的原子个数比为 的物质的电子式:
的物质的电子式:(5)
 的氢化物属于
的氢化物属于该氢化物与水反应的化学方程式为
(6)
 和
和 两种元素形成的简单氢化物的稳定性
两种元素形成的简单氢化物的稳定性
 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近一年使用:0次
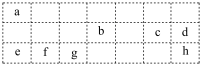
5 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
解题方法
6 . 下表为元素周期表中的一部分.
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是____________ .
(2)②③④中形成的简单离子半径由大到小的顺序是____________ .
(3)⑨的最高价氧化物对应水化物的化学式为____________ .①和⑨两元素形成化合物的化学式为____________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为____________ .
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是____________ ,三者非金属性的强弱顺序为____________ .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)①③⑤中,最高价氧化物对应水化物中碱性最强的是
(2)②③④中形成的简单离子半径由大到小的顺序是
(3)⑨的最高价氧化物对应水化物的化学式为
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
7 . X、Y、Z、W、Q是元素周期表中原子序数依次增大的五种短周期主族元素,X最外层电子数是内层电子数的2倍,Y的单质与氢气在暗处能剧烈化合并发生爆炸,Z短周期元素中原子半径最大,W其氧化物是两性氧化物,Q同周期元素中,最高价氧化物对应水化物的酸性最强。
(1)元素Y在元素周期表中的位置是___________ 。
(2)Z在氧气中完全燃烧的产物的化学式为___________ 。
(3)Y、W、Q的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。___________ 、___________ ;M为___________ (填化学式),其作用是___________ 。
②能说明X元素的非金属性比硅元素强的实验现象是___________ 。
(5)元素Z与W相比,金属性较弱的是___________ (填元素名称),请写出能证明这一结论的实验事实___________ 。(列举一条)
(1)元素Y在元素周期表中的位置是
(2)Z在氧气中完全燃烧的产物的化学式为
(3)Y、W、Q的简单离子半径由大到小的顺序是
(4)某同学为了比较X元素和硅元素非金属性的相对强弱,用如图所示装置进行实验。

②能说明X元素的非金属性比硅元素强的实验现象是
(5)元素Z与W相比,金属性较弱的是
您最近一年使用:0次
名校
8 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
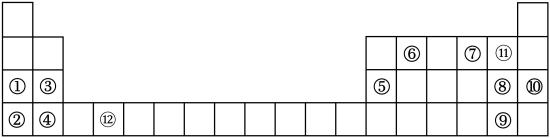
(1)在这12种元素中,化学性质最不活泼的是_______ ,原子半径最大的是_______ 。
(2)①②⑤中,最高价氧化物的水化物中碱性最强的是_______ 。
(3)⑤和⑨最高价氧化物对应的水化物反应化学方程式为_______ 。
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
(5)元素⑫在周期表中的位置是_______ 。
(6)⑤的单质和①的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(7)⑥的最高价氧化物电子式为:_______ 。
(8)查阅资料可知:③的单质可以在⑥的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:_______ 。

(1)在这12种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物中碱性最强的是
(3)⑤和⑨最高价氧化物对应的水化物反应化学方程式为
(4)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
(5)元素⑫在周期表中的位置是
(6)⑤的单质和①的最高价氧化物对应的水化物反应的离子方程式为
(7)⑥的最高价氧化物电子式为:
(8)查阅资料可知:③的单质可以在⑥的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:
您最近一年使用:0次
9 . 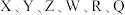 为原子序数依次增大的六种短周期主族元素。
为原子序数依次增大的六种短周期主族元素。 是原子半径最小的元素;
是原子半径最小的元素; 原子最外层电子数是核外电子层数的3倍;
原子最外层电子数是核外电子层数的3倍; 是短周期中金属性最强的元素;
是短周期中金属性最强的元素; 是地壳中含量最多的金属元素;
是地壳中含量最多的金属元素; 的最高正价与最低负价代数和为4。回答下列问题:
的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示
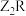 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)
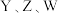 三种元素对应的简单离子半径由大到小的顺序是
三种元素对应的简单离子半径由大到小的顺序是(5)下列说法能证明非金属性
 强于
强于 的是
的是a.简单阴离子的还原性: b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性: d.
d.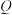 的单质能从
的单质能从 溶液中置换出
溶液中置换出 单质
单质
(6)
 的单质与
的单质与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2024-03-29更新
|
160次组卷
|
2卷引用:山西省部分学校2023-2024学年高一上学期1月期末化学试题
名校
10 . 下表为八种短周期主族元素的部分性质(已知铍的原子半径为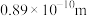 ):
):
(1)元素Z在元素周期表中的位置为_______ 。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:_______ 。
(3)R与T相比,非金属性较强的是_______ (填元素符号),下列事实能证明这一结论的是_______ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: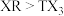
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是_______ (填元素符号),能证明这一结论的依据是_______ 。
(5)根据表中数据推测,M的原子半径的最小范围是_______ 。
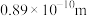 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 |  | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
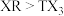
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
2024-03-20更新
|
129次组卷
|
2卷引用:江西省庐山市第一中学2023-2024学年高一上学期1月期末考试化学试题



