名校
解题方法
1 . 2021年,剑桥大学Dominic.S.Wght课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。其中X、Y、Z为原子序数依次增大的短周期主族元素,三者的核外电子数之和等于35,则下列说法正确的是


| A.简单离子半径:X>Y |
| B.Z的最高价氧化物的水化物是强酸 |
| C.工业上常采用电解Y的氧化物冶炼单质Y |
| D.该化合物阴离子中各原子均满足8电子稳定结构 |
您最近一年使用:0次
名校
2 . 2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短周期主族元素,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正确的是


| A.简单离子的半径:X>Y |
| B.Z的最高价氧化物对应水化物是强酸 |
| C.工业上常采用电解Y的氧化物冶炼单质Y |
| D.该化合物阴离子中各原子均满足8电子稳定结构 |
您最近一年使用:0次
名校
3 . 2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短周期主族元素,X的电负性为4,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正确的是
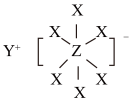

| A.简单离子的半径:X>Y |
| B.Z的最高价氧化物对应水化物是强酸 |
| C.工业上常采用电解Y的氧化物冶炼单质Y |
| D.该化合物阴离子中各原子均满足8电子稳定结构 |
您最近一年使用:0次
2022-05-30更新
|
285次组卷
|
6卷引用:山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题
山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题06物质结构元素周期律-2022年高考真题+模拟题汇编(全国卷)(已下线)专题06物质结构元素周期律-三年(2020~2022)高考真题汇编(全国卷)北京市海淀区中关村中学2022届高三下学期三模化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)
名校
4 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是____ ,用电子式表示Y的最高价氧化物的形成过程:_____ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)_______ 。
(3)在 与
与 的混合液中通入足量
的混合液中通入足量 ,是工业制取
,是工业制取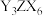 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:_______ 。
(4) 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
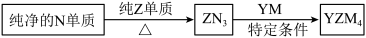
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为_______ 。
②现设计如图四种装置测定 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_______ (填编号)。
③取样品ag,若实验测得氢气的体积为 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为_______ (用代数式表示)。
(1)Y在周期表中的位置是
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示)
(3)在
 与
与 的混合液中通入足量
的混合液中通入足量 ,是工业制取
,是工业制取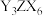 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)
 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②现设计如图四种装置测定
 样品的纯度(假设杂质不参与反应)。
样品的纯度(假设杂质不参与反应)。
从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为
 (标准状态),则
(标准状态),则 样品纯度为
样品纯度为
您最近一年使用:0次
5 . 新工艺采用金属氧化物 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:
反应①: +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)
反应②:2NH3(g)+CO2(g)
 +H2O(l)
+H2O(l)
完成下列填空:
(1)C原子核外能量最高的电子有______ 个,比较 、N、O简单离子的半径大小
、N、O简单离子的半径大小__________ 。
(2)下列事实能说明氮的非金属性比碳强的是______ (选填编号)。
a.酸性: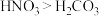 b.最高正价:氮>碳
b.最高正价:氮>碳
c.沸点: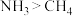 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳
(3)达到平衡时,反应①碳酸二甲酯的产率 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是__________ 反应(选填“放热”或“吸热”),
______  (选填“>”或“<”)。
(选填“>”或“<”)。

(4)某一恒温恒容 装置内,
装置内, 与
与 发生反应②,
发生反应②,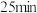 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为__________ 。
(5)传统合成DMC的方法是以光气( ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式__________ 。
(6)新工艺合成DMC的方法和传统方法相比,优点有__________ (任写两点)。
 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:反应①:
 +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)反应②:2NH3(g)+CO2(g)

 +H2O(l)
+H2O(l)完成下列填空:
(1)C原子核外能量最高的电子有
 、N、O简单离子的半径大小
、N、O简单离子的半径大小(2)下列事实能说明氮的非金属性比碳强的是
a.酸性:
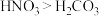 b.最高正价:氮>碳
b.最高正价:氮>碳c.沸点:
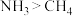 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳(3)达到平衡时,反应①碳酸二甲酯的产率
 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是
 (选填“>”或“<”)。
(选填“>”或“<”)。
(4)某一恒温恒容
 装置内,
装置内, 与
与 发生反应②,
发生反应②,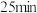 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为(5)传统合成DMC的方法是以光气(
 ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式(6)新工艺合成DMC的方法和传统方法相比,优点有
您最近一年使用:0次



