名校
1 . 短周期元素X、Y、Z、M的原子序数依次增大,它们组成一种团簇分子,结构如图所示。X、M的族序数均等于周期序数,Y原子核外最外层电子数为6,下列说法正确的是
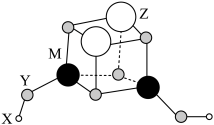
| A.简单离子半径:Z>M>Y |
| B.Y2与Y3都是由Y原子组成的,所以是同一种物质 |
| C.工业上常用电解熔融物ZY制取Z单质 |
| D.Z为镁元素 |
您最近一年使用:0次
解题方法
2 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
| 元素 |  |  |  |  |
| 最高价氧化物的水化物 | 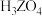 | |||
 溶液对应的pH(25℃) 溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
| A.X、W最简单氢化物的键角:X>W |
| B.简单离子半径:W<Y |
| C.元素电负性、第一电离能:Z<W |
| D.简单氢化物的沸点:X<Z |
您最近一年使用:0次
2024-02-02更新
|
76次组卷
|
4卷引用:云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷
云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)江西省上饶市广丰一中2023-2024学年高三上学期12月考试化学试卷湖南省浏阳市2023-2024学年高二上学期期末质量监测考试化学试题
名校
解题方法
3 . X、Y、Z、R、M为原子序数依次增大的五种短周期主族元素,其中X的原子半径最小,Y与Z可形成一种红棕色有刺激性气味的气体;R与X同主族;M原子最外层的电子数与Y的电子总数相同。下列叙述正确的是
| A.X与Y只能形成一种二元化合物 |
| B.简单离子半径:M>Y>Z>R |
| C.R与Z形成的化合物中只含有离子键 |
| D.Y、M的氧化物对应的水化物均为强酸 |
您最近一年使用:0次
4 . 几种短周期元素的原子半径及主要化合价见下表,下列相关叙述错误的是
| 元素代号 |  |  |  |  |  |
原子半径 |  |  | 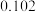 | 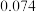 |  |
| 主要化合价 |  |  |  、 、 |  |  、 、 |
A. 、 、 最高价氧化物对应的水化物碱性: 最高价氧化物对应的水化物碱性: |
B.离子半径: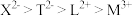 |
C. 单质能与 单质能与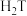 反应,置换出 反应,置换出 |
D. 的最高价氧化物是两性氧化物 的最高价氧化物是两性氧化物 |
您最近一年使用:0次
5 . 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20,W是组成有机物的必备元素,Z原子核外最外层电子数等于其最内层电子数,X2−核外电子比Z2+少一个电子层,Y有两种颜色不同的同素异形体。下列说法正确的是
| A.原子半径:Y<X | B.最简单氢化物的稳定性:X>W |
| C.X与Z组成的化合物只含离子键 | D.Y的最高价氧化物对应水化物为三元强酸 |
您最近一年使用:0次
名校
6 . 根据下表(部分短周期元素的原子半径及主要化合价)信息,下列叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A.E2-与B3+的核外电子数不可能相等 | B.离子半径:A+<D2- |
| C.最高价氧化物对应水化物的碱性:A<C | D.氢化物的稳定性:D>E |
您最近一年使用:0次
名校
解题方法
7 . 已知 、
、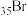 位于同一周期,下列关系正确的是
位于同一周期,下列关系正确的是
 、
、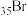 位于同一周期,下列关系正确的是
位于同一周期,下列关系正确的是A.热稳定性: |
B.原子半径: |
C.还原性: |
D.酸性: |
您最近一年使用:0次
8 . X、Y、Z、W是原子序数依次递增的短周期元素,其中X、Y、Z处于同一周期,由这四种元素组成的化合物M的结构式如图所示。下列有关说法错误的是
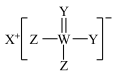
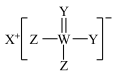
A.离子半径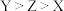 |
| B.化合物M中Y、Z、W都达到了8电子稳定结构 |
C.Y和Z的简单氢化物沸点 |
D.非金属性由强到弱的顺序是: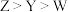 |
您最近一年使用:0次
名校
9 . 以硼砂、萤石和浓硫酸为原料可制取有机合成的原料三氟化硼。反应原理为:B2O3(s)+3CaF2(s)+3H2SO4(浓)=2BF3(g)+3CaSO4(s)+3H2O(l)。请完成下列填空:
(1)萤石的电子式___________ ,已知BF3为非极性分子,则其分子构型可能为___________ (填编号)。
A. 三角锥形 B. 平面正三角形 C. 直线形 D. 正四面体形
(2)硼原子核外电子的轨道表示式___________ ,硼原子核外有___________ 种不同形状的电子云。
(3)该反应体系中除硼元素外的其他短周期元素的简单离子的半径由小到大排列的是(用离子符号表示)___________ 。
(4)其中O与S相比,非金属性较强的是___________ ,下列能比较它们非金属性强弱的有(填编号)___________ 。
A. 相互之间的置换反应 B. 最高价氧化物对应的水化物的酸性
C. 氢化物水溶液的酸性 D. 相互形成的化合物中元素的化合价
(1)萤石的电子式
A. 三角锥形 B. 平面正三角形 C. 直线形 D. 正四面体形
(2)硼原子核外电子的轨道表示式
(3)该反应体系中除硼元素外的其他短周期元素的简单离子的半径由小到大排列的是(用离子符号表示)
(4)其中O与S相比,非金属性较强的是
A. 相互之间的置换反应 B. 最高价氧化物对应的水化物的酸性
C. 氢化物水溶液的酸性 D. 相互形成的化合物中元素的化合价
您最近一年使用:0次
名校
10 . 2019 年诺贝尔化学奖颁给研究锂电池的科学家,一种用作锂电池电解液的锂盐结构如图所示。其中,X位于第三周期,X原子的电子数为Z原子的两倍,W、Z、Y位于同一周期。下列叙述正确的是


| A.原子半径: X>Z>W | B.非金属性: Z>W>Y |
| C.Y的氢化物水溶液是弱酸 | D.X的氧化物对应的水化物均为强酸 |
您最近一年使用:0次
2023-09-30更新
|
63次组卷
|
2卷引用:上海市徐汇区徐汇中学2022-2023学年高三上学期11月期中考试化学试题



