名校
1 . 现有U、V、W、X、Y、Z共6种短周期元素,其原子序数依次增大,部分信息如下表:
请用相应的化学用语回答下列问题:
(1)第一电离能介于X和Y之间的第三周期的元素共有___________ 种。基态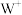 离子的电子占据最高能级的电子云轮廓图为
离子的电子占据最高能级的电子云轮廓图为___________ 形。
(2)Z原子的简化电子排布式为___________ 。
(3)根据对角线规则,与X的化学性质最相似的邻族短周期元素是___________ (填元素名称)。
(4)元素R与Y的原子序数相差18,预测R的简单氢化物分子的立体构型为___________ 其稳定性比Y的简单氢化物___________ (填“高”或“低”),其判断理由是___________ (从原子结构的角度分析)。
(5)V、W、Z的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(6)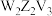 可以看成是
可以看成是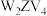 中的一个V原子被一个Z原子取代的产物,
中的一个V原子被一个Z原子取代的产物,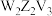 溶液与
溶液与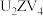 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为___________ 。
| U | 最高正价与最低负价的代数和为0,基态原子p能级上无电子 |
| V | 基态原子L层p能级电子数是L层s能级电子数的2倍 |
| W | 存在质量数为23,中子数为12的核素 |
| X | 基态原子的价电子排布为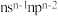 |
| Y | 单质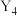 :正四面体结构,有剧毒,易自燃 :正四面体结构,有剧毒,易自燃 |
| Z |  能使品红溶液褪色,加热后品红能恢复红色 能使品红溶液褪色,加热后品红能恢复红色 |
(1)第一电离能介于X和Y之间的第三周期的元素共有
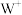 离子的电子占据最高能级的电子云轮廓图为
离子的电子占据最高能级的电子云轮廓图为(2)Z原子的简化电子排布式为
(3)根据对角线规则,与X的化学性质最相似的邻族短周期元素是
(4)元素R与Y的原子序数相差18,预测R的简单氢化物分子的立体构型为
(5)V、W、Z的简单离子半径由大到小的顺序为
(6)
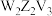 可以看成是
可以看成是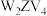 中的一个V原子被一个Z原子取代的产物,
中的一个V原子被一个Z原子取代的产物,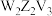 溶液与
溶液与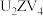 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为
您最近一年使用:0次
2 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是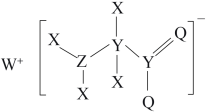
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
2024-04-08更新
|
66次组卷
|
2卷引用:云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
名校
3 . 现有四种元素,其中两种元素基态原子的电子排布式如下:①1s22s22p63s23p2②1s22s22p63s23p3,另两种元素的价电子排布式为③2s22p3④2s22p4,则下列有关比较中正确的是
| A.原子半径:①>②>④>③ | B.第一电离能:④>③>②>① |
| C.电负性: ④>③>②>① | D.最高正化合价:④>③=②>① |
您最近一年使用:0次
2024-04-08更新
|
295次组卷
|
3卷引用:四川省成都市成华区某校2023-2024学年高二下学期4月月考化学试题
4 . W、X、Y、Z、M为原子序数依次增大的短周期主族元素,其原子半径和最外层电子数的关系如图所示。下列说法正确的是
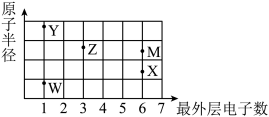

| A.简单氢化物的沸点:X<M |
| B.Z的氧化物可用作耐火材料 |
| C.X、Y、Z的简单离子半径:X<Y<Z |
| D.最高价氧化物对应水化物碱性:Y<Z |
您最近一年使用:0次
名校
解题方法
5 . 2021年6月11日国家航天局公布了“祝融号”火星车拍摄的首批科学影像图。已知:火星气体及岩石中富含X、Y、Z、W四种元素,X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与冷水反应后溶液能使酚酞试液变为红色,X、W为同一主族元素,Y地壳中含量最高的元素,火星岩石含有W的最高价化合物Z2WY3。下列判断正确的是
| A.原子半径:Z>W>Y>X |
| B.W位于元素周期表第三周期VIIA族 |
| C.最高价氧化物对应水化物的酸性:X>W |
| D.X、Y、Z三种元素组成的化合物中没有离子 |
您最近一年使用:0次
2024-01-28更新
|
103次组卷
|
3卷引用:福建省福州高级中学2022-2023学年高二上学期学段考试化学试题
6 . 四种元素基态原子的电子排布式如下:① ;②
;② ;③
;③ ;④
;④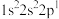 。下列有关比较中正确的是
。下列有关比较中正确的是
 ;②
;② ;③
;③ ;④
;④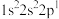 。下列有关比较中正确的是
。下列有关比较中正确的是| A.第一电离能:④>③>②>① | B.原子半径:④>③>①>② |
| C.电负性:③>④>①>② | D.最高正化合价:④=①>③=② |
您最近一年使用:0次
2024-01-24更新
|
143次组卷
|
7卷引用:第一章 本章达标检测2
名校
解题方法
7 . 下列有关性质或数据的比较正确的是
A.原子的未成对电子数: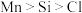 | B.第一电离能: |
C.离子半径: | D.电负性: |
您最近一年使用:0次
8 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_____ (填“吸收光谱”或“发射光谱”)。
(2)某元素的激发态原子的电子排布式为 ,则该元素基态原子的电子排布式为
,则该元素基态原子的电子排布式为_____ ;其最高价氧化物对应水化物的化学式是_____ 。
(3) 原子位于元素周期表中的
原子位于元素周期表中的_____ 区,最高能层电子的电子云轮廓形状为_____ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为_____ 。
(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
_____ (填“大于”、“小于”或“等于”) ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_____ 。
(5)下列各组多电子原子的能级能量比较不正确的是_____ (填序号)。
① ②
② ③
③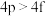 ④
④
(1)钠在火焰上灼烧的黄光是一种
(2)某元素的激发态原子的电子排布式为
 ,则该元素基态原子的电子排布式为
,则该元素基态原子的电子排布式为(3)
 原子位于元素周期表中的
原子位于元素周期表中的 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 。
。 与
与 的离子半径大小关系为
的离子半径大小关系为
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(5)下列各组多电子原子的能级能量比较不正确的是
①
 ②
② ③
③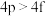 ④
④
您最近一年使用:0次
名校
解题方法
9 . 短周期元素 、
、 、
、 、
、 的原子序数依次增大,它们组成的一种分子结构如图所示,结构中只有
的原子序数依次增大,它们组成的一种分子结构如图所示,结构中只有 不满足最外层8电子的稳定结构。常温下,
不满足最外层8电子的稳定结构。常温下, 、
、 、
、 、
、 分别形成的常见单质中有2种是气体,下列说法正确的是
分别形成的常见单质中有2种是气体,下列说法正确的是

 、
、 、
、 、
、 的原子序数依次增大,它们组成的一种分子结构如图所示,结构中只有
的原子序数依次增大,它们组成的一种分子结构如图所示,结构中只有 不满足最外层8电子的稳定结构。常温下,
不满足最外层8电子的稳定结构。常温下, 、
、 、
、 、
、 分别形成的常见单质中有2种是气体,下列说法正确的是
分别形成的常见单质中有2种是气体,下列说法正确的是
A.在化合物中, 只显正价 只显正价 |
B. 形成的单质是一种廉价易得的清洁燃料 形成的单质是一种廉价易得的清洁燃料 |
C.原子半径: |
D.最高价氧化物对应水化物的酸性: |
您最近一年使用:0次
2024-01-17更新
|
133次组卷
|
2卷引用:陕西省咸阳市实验中学2022-2023学年高二上学期开学质量检测化学试题
名校
10 . 随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)g元素的离子结构示意图为___________ ;元素y的一种质子数与中子数相同的核素符号为___________ 。
(2)元素z与x元素形成一种离子zx ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是___________ 。
(3)e和f两元素相比较,金属性较强是___________ (填元素符号),可以证明该结论的实验是___________ 。
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目
(4)z、d、e、f元素分别形成的简单离子中离子半径由大到小的顺序是___________ (填离子符号)。
(5)e2g4是离子化合物,各原子均满足8电子稳定结构,则e2g4的电子式为___________ ,z2x4的结构式为___________ ,fh3溶液和e2g溶液混合反应的离子方程式为___________ 。

(1)g元素的离子结构示意图为
(2)元素z与x元素形成一种离子zx
 ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是(3)e和f两元素相比较,金属性较强是
A.比较这两种元素最高价氧化物对应的水化物的碱性
B.比较这两种元素的气态氢化物的稳定性
C.将相同大小的这两种元素单质分别放入冷水中,观察反应现象
D.比较物质的量相同的这两种元素的单质与酸反应时失电子的数目
(4)z、d、e、f元素分别形成的简单离子中离子半径由大到小的顺序是
(5)e2g4是离子化合物,各原子均满足8电子稳定结构,则e2g4的电子式为
您最近一年使用:0次



