名校
解题方法
1 . 有A、B、C、D、E五种短周期元素,A是地壳中含量最多的元素,B元素有3种同位素 B₁、B₂、B₃, B₃原子的质量数是B₁的3倍, C是非金属性最强的元素, D 和C可以形成DC型离子化合物,且离子的电子层结构相同,E元素原子的最外层电子数比内层电子总数少6个。下列说法正确的是
| A.离子半径: D⁺>C⁻ |
| B.EA₂是光导纤维的主要成分 |
| C.A和B不能形成原子个数比1∶1的化合物 |
| D.以上元素中形成的最高价氧化物对应的水化物酸性最强的是 C |
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分,请根据表标注的元素回答(用相应的化学符号作答):
(1)形成单质不含化学键的是___________ (填化学式)。
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是___________ (填化学式)。
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为___________ (用物质化学式表示)。
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有___________ 。
(6)写出由元素a、e、g组成的化合物的电子式:___________ 。
| 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 周期 | 1 | a | f | ||||||
| 2 | b | d | e | ||||||
| 3 | g | h | k | m | n | ||||
(2)元素a分别与元素e、k、m所形成的简单气态化合物中稳定性最强的是
(3)元素k、m、n最高价氧化物对应的水化物酸性由强到弱的顺序为
(4)元素g、h、m、n所形成的简单离子的半径由大到小的顺序为
(5)元素d的简单氢化物,与其最高价氧化物的水化物反应的产物,所含化学键的类型有
(6)写出由元素a、e、g组成的化合物的电子式:
您最近一年使用:0次
3 . 几种主族元素在周期表中的位置如图
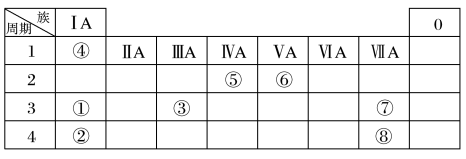
根据上表回答下列问题:
(1)写出⑤和⑧两种元素的名称:___________ 、___________ 。
(2)①和⑦两种元素的形成化合物的电子式是___________ 。
(3)①③⑦三种元素离子半径由大到小的顺序是___________ (用元素符号表示)。
(4)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是 ___________ 。
(5)②与③最高价氧化物对应水化物反应的离子方程式为___________ 。
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是___________ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱

根据上表回答下列问题:
(1)写出⑤和⑧两种元素的名称:
(2)①和⑦两种元素的形成化合物的电子式是
(3)①③⑦三种元素离子半径由大到小的顺序是
(4)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(5)②与③最高价氧化物对应水化物反应的离子方程式为
(6)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
您最近一年使用:0次
4 . X、Y、Z、W、M、R、T七种短周期元素,周期表中位置如图:
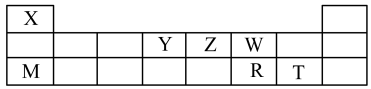
试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是______ (用元素符号表示)。
(2)W的简单氢化物的电子式为_______ 。
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为______ 。
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是______ (用化学式表示)。
(5)M和R最高价氧化物对应水化物反应的离子方程式为______ 。

试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是
(2)W的简单氢化物的电子式为
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是
(5)M和R最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
名校
5 . 几种短周期元素的原子半径及主要化合价如下表所示,下列叙述正确的是
元素代号 | X | Y | Z | W | Q |
原子半径/pm | 130 | 118 | 75 | 73 | 102 |
主要化合价 | +2 | +3 | +5、-3 | -2 | +6、-2 |
| A.简单离子半径:X<Y |
B.一定条件下,Z单质与W的常见单质直接生成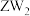 |
| C.W的简单氢化物比Q的更稳定,是因为W的简单氢化物中含有氢键 |
| D.最高价氧化物对应的水化物的碱性:X>Y |
您最近一年使用:0次
6 . 如表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素③的原子结构示意图是___________ ,以上元素的最高价氧化物形成的水化物酸性最强的是___________ (填分子式)。
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为___________ 。
(4)②和⑦按原子个数比 1:1 形成离子化合物乙的电子式为___________
(5)下列物质中,互为同素异形体的是___________ ,属于同位素的 ___________ 。
①正戊烷②白磷③ ④
④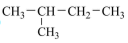 ⑤
⑤ Cl⑥红磷⑦
Cl⑥红磷⑦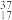 Cl
Cl
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ⑦ | ||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
(1)元素③的原子结构示意图是
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序为
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(4)②和⑦按原子个数比 1:1 形成离子化合物乙的电子式为
(5)下列物质中,互为同素异形体的是
①正戊烷②白磷③
 ④
④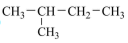 ⑤
⑤ Cl⑥红磷⑦
Cl⑥红磷⑦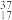 Cl
Cl
您最近一年使用:0次
名校
7 . 下列各组元素的原子随着原子序数的递增,有关递变规律不正确的是
| A.原子半径:Si>P>S>Cl | B.金属性:Na<K<Rb<Cs |
| C.最高正价:C<N<O<F | D.非金属性:P<S<Cl |
您最近一年使用:0次
2024-03-11更新
|
212次组卷
|
8卷引用:贵州省仁怀市周林高级中学2021-2022学年高一下学期入学考试化学试题
名校
解题方法
8 . 短周期元素R、X、Y、Z、M原子序数依次递增,原子最外层电子数存在关系: ,其中元素R、X、Y、M形成的化合物具有如图所示转化关系。下列说法不正确的是
,其中元素R、X、Y、M形成的化合物具有如图所示转化关系。下列说法不正确的是

 ,其中元素R、X、Y、M形成的化合物具有如图所示转化关系。下列说法不正确的是
,其中元素R、X、Y、M形成的化合物具有如图所示转化关系。下列说法不正确的是
A.原子半径: |
| B.Z和M的最高价氧化物对应的水化物能发生反应 |
| C.R、X、Y形成的化合物可能会使紫色石蕊溶液变红 |
| D.Z分别与R、M形成的化合物中均只含离子键 |
您最近一年使用:0次
解题方法
9 . 一种麻醉剂的分子结构式如下图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增大;元素E的原子比W原子多8个电子。下列说法不正确的是

A. 是一种强酸 是一种强酸 |
B.原子半径: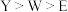 |
C.非金属性: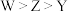 |
| D.Z元素分别与X、Y、E元素均可形成至少两种二元化合物 |
您最近一年使用:0次
2024-02-25更新
|
244次组卷
|
4卷引用:广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷
名校
解题方法
10 . 短周期元素c、d、e、f、g、h存在于某些食品添加剂中,如着色剂胭脂红中含有f、g等元素。这六种元素的最高正化合价或最低负化合价与原子序数的关系如图所示。已知c为非金属元素,d元素的最外层电子数为内层电子数的3倍。

回答下列问题:
(1)元素g在周期表中的位置是_______ 。
(2)元素c和d组成的化合物中,既含有极性共价键又含有非极性共价键的是_______ (填化学式)。元素c、e、d形成的离子化合物的电子式为_______ 。
(3)元素f形成的最高价氧化物与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(4)元素d、e、f、g形成的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(5) 可用于处理碱性工业废水中的
可用于处理碱性工业废水中的 ,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,该反应的离子方程式为
,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,该反应的离子方程式为_______ 。
(6)硒酵母是一种新型添加剂。下列判断正确的是_______(填字母)。

回答下列问题:
(1)元素g在周期表中的位置是
(2)元素c和d组成的化合物中,既含有极性共价键又含有非极性共价键的是
(3)元素f形成的最高价氧化物与
 溶液反应的离子方程式为
溶液反应的离子方程式为(4)元素d、e、f、g形成的简单离子半径由大到小的顺序为
(5)
 可用于处理碱性工业废水中的
可用于处理碱性工业废水中的 ,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,该反应的离子方程式为
,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,该反应的离子方程式为(6)硒酵母是一种新型添加剂。下列判断正确的是_______(填字母)。
A.稳定性: | B. 与 与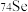 的中子数之和为58 的中子数之和为58 |
C.酸性: | D.还原性: |
您最近一年使用:0次



