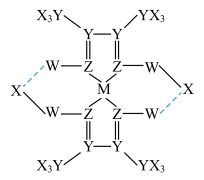
现有四种元素,其中两种元素基态原子的电子排布式如下:①1s22s22p63s23p2②1s22s22p63s23p3,另两种元素的价电子排布式为③2s22p3④2s22p4,则下列有关比较中正确的是
| A.原子半径:①>②>④>③ | B.第一电离能:④>③>②>① |
| C.电负性: ④>③>②>① | D.最高正化合价:④>③=②>① |
更新时间:2024-04-08 16:38:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、R为原子序数依次增大的短周期元素,X的一种核素无中子,Z、R为同主族元素,X、Y、Z、R可形成多种化合物,其中一种可表示为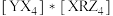 。下列说法正确的是
。下列说法正确的是
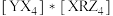 。下列说法正确的是
。下列说法正确的是| A.原子半径:R<Y<Z<X |
| B.R在周期表中位于第三周期VI族 |
| C.Y元素的气态氢化物能与其最高价含氧酸反应 |
| D.Z与R两种元素形成的化合物只有一种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】工业上电解熔融 和冰晶石
和冰晶石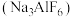 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是
 和冰晶石
和冰晶石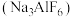 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是
A.电离能大小: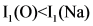 | B.电负性大小: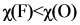 |
C.半径大小: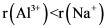 | D.碱性强弱: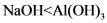 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知:四种原子最外层电子数之和为24。下列说法正确的是


| A.元素X和元素Z的最高正化合价相同 |
B.单核阴离子半径的大小顺序为 |
C.气态简单氢化物的热稳定性顺序为 |
| D.元素Y的氧化物对应水化物都是强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下图是一种综合处理含 尾气的工艺流程,下列叙述正确的是
尾气的工艺流程,下列叙述正确的是
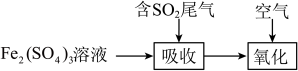
 尾气的工艺流程,下列叙述正确的是
尾气的工艺流程,下列叙述正确的是
A. 的价电子排布式为 的价电子排布式为 |
B.检验“吸收”后的溶液是否还可继续吸收 ,可用试剂 ,可用试剂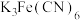 |
C.“氧化”中发生反应的离子方程式为: |
| D.“氧化”后的溶液可以循环使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化合物A可应用于清洁剂、化妆品、杀虫剂,结构简式如图所示,W、X、Y、Z分属三个短周期的主族元素且原子序数依次增大,X最高价氧化物对应的水化物为弱酸,Y是地壳中含量最多的元素,下列说法错误的是
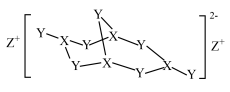

| A.Y与Z形成的两种化合物阴阳离子比均为1:2 |
| B.电负性大小关系为:Y>W>X>Z |
| C.Y基态原子核外电子有5种空间运动 |
| D.化合物A的阴离子中所有原子均满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种可用作有机化工原料的化合物Q的结构如图。已知X、Y、Z、W、M为原子序数依次增大的主族元素,其中X的核电荷数等于其主族序数,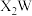 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
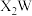 是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是
是常温下常见的液态化合物,基态Y原子核外未成对电子数与基态W原子核外未成对电子数相等,M的单质是常温下唯一的液态非金属单质。下列说法正确的是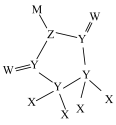
| A.原子半径:W>Z>Y | B.第一电离能:Z>W>Y |
| C.电负性:M>W>Z | D.键角: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CrSi,Ge-GaAs、聚吡咯和碳化硅都是重要的半导体化合物。下列说法正确的是
| A.基态铬原子的核外未成对电子数为6 |
| B.Ge-GaAs中元素Ge、Ga、As的第一电离能从小到大的顺序为As<Ge<Ga |
C.聚吡咯的单体为吡咯(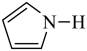 ),分子中σ键与π键的数目之比为5:2 ),分子中σ键与π键的数目之比为5:2 |
| D.碳化硅属于分子晶体,其熔、沸点均大于金刚石 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】我国科学家最近发现一种可用于制造半导体材料的新物质,其结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,Z、Y处于同一主族。下列说法正确的是
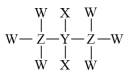
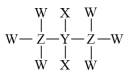
A.原子半径: |
B.电负性: |
| C.W、Z形成的化合物各原子最外层满足8电子稳定结构 |
| D.W的氧化物对应的水化物为强电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】次氟酸(又名氟氧酸)是一种强氧化剂,可用被氮气稀释的氟气在细冰上缓慢通过制得,发生反应: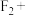
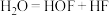 。下列关于次氟酸的说法正确的是
。下列关于次氟酸的说法正确的是
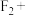
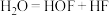 。下列关于次氟酸的说法正确的是
。下列关于次氟酸的说法正确的是| A.氟原子半径大于氧原子 | B.HOF分子中F为+1价 |
| C.第一电离能和电负性,F都大于O | D.次氟酸的强氧化性是F元素表现出来的 |
您最近一年使用:0次

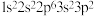 的原子
的原子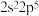 的原子
的原子 的原子
的原子 的原子
的原子 的原子
的原子 的原子
的原子