1 . 材料是人类赖以生存和发展的物质基础。下列说法错误的是
| A.硅晶片是生产芯片的基础材料 |
| B.棉花、羊毛、蚕丝、涤纶都属于天然纤维 |
| C.硫化后的橡胶适合制造轮胎,加入炭黑可提高轮胎的耐磨性 |
| D.离子液体是熔点不高的仅有离子组成的液体物质 |
您最近一年使用:0次
2024-05-16更新
|
306次组卷
|
2卷引用:重庆市第八中学校2022届高三下学期高考适应性月考(七)化学试题
名校
2 . 氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
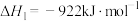
Ⅱ.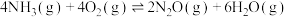
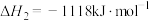
Ⅲ.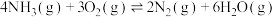

已知:298K时,相关物质的焓的数据如图。
___________  。
。
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为___________ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
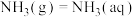

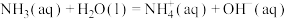

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度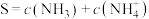 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为___________ 。
(4)由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
已知: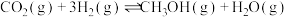 的
的 -49.5kJ/mol
-49.5kJ/mol
反应②:

反应③: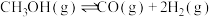
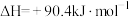
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。___________  。
。
Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入
 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在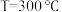 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在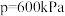 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。
ii. 点
点 的分压为
的分压为___________  ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
___________  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中 点的
点的 高于
高于 点的原因是
点的原因是___________ 。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:Ⅰ.

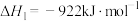
Ⅱ.
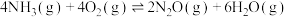
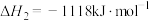
Ⅲ.
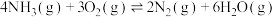

已知:298K时,相关物质的焓的数据如图。


 。
。(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。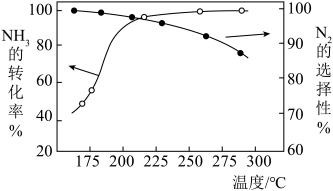
 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
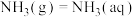

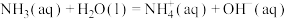

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度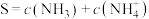 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)由
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。已知:
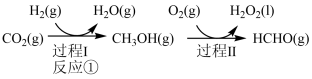
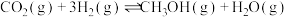 的
的 -49.5kJ/mol
-49.5kJ/mol反应②:


反应③:
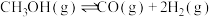
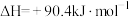
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
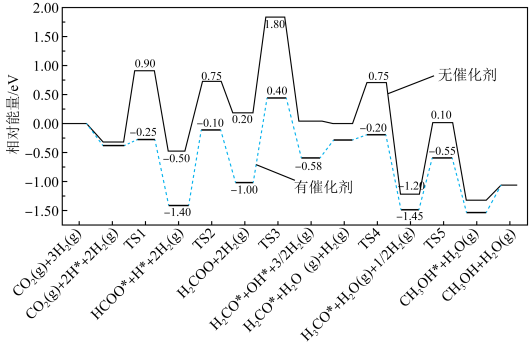
 。
。Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入

 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在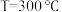 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在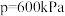 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。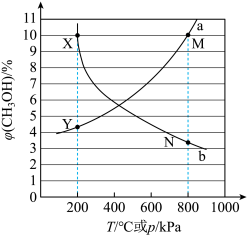
 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。ii.
 点
点 的分压为
的分压为 ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中
 点的
点的 高于
高于 点的原因是
点的原因是
您最近一年使用:0次
名校
解题方法
3 . 室温下,某同学用下图中装置在通风棚中进行如下实验:
下列说法不正确的是
| 实验 | 现象 |
| 试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应越来越剧烈,试管口上方出现红棕色气体,溶液呈蓝色 |
| 试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色,之后向溶液中持续通入N2,溶液又变为蓝色 |
| A.试管Ⅰ中浅红棕色气体为NO2,由铜还原硝酸生成 |
| B.等质量的Cu完全溶解时,Ⅰ中消耗的HNO3更少 |
| C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有NO2 |
| D.新制的Cu(OH)2悬浊液可用于检验醛基 |
您最近一年使用:0次
名校
4 . 短周期元素X、Y、Z、M的原子序数依次增大,它们组成一种团簇分子,结构如图所示。X、M的族序数均等于周期序数,Y原子核外最外层电子数为6,下列说法正确的是
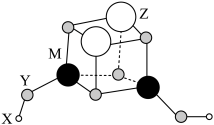
| A.简单离子半径:Z>M>Y |
| B.Y2与Y3都是由Y原子组成的,所以是同一种物质 |
| C.工业上常用电解熔融物ZY制取Z单质 |
| D.Z为镁元素 |
您最近一年使用:0次
名校
5 . List和MacMillan因开发“不对称有机催化”荣获2021年诺贝尔奖,下图是一个典型的不对称催化反应(图中“楔形”结构表示该基团不在纸张平面上)。下列说法中不正确的是
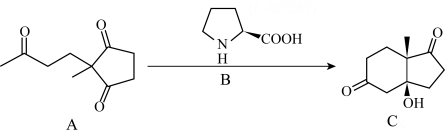
| A.化合物A的分子式为C10H12O3 | B.化合物B是一个两性分子 |
| C.化合物C含有2个手性碳原子 | D.图中反应(A→C)属于加成反应 |
您最近一年使用:0次
名校
6 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
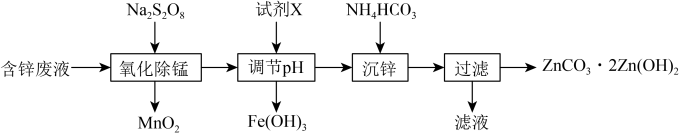
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次
名校
7 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。下列关于海洋氮循环的说法不正确的是
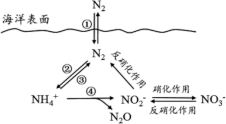
| A.海洋中的氮循环起始于氮的氧化 |
| B.氮循环中涉及氮的固定 |
C.向海洋排放含NO 的废水会影响海洋中NH 的废水会影响海洋中NH 的含量 的含量 |
| D.“硝化作用”可能有氧气的参与 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.反应2H2(g)+O2(g) =2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和-反应中断裂旧共价键的键能之和 |
| B.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应 |
| C.3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023 |
| D.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 |
您最近一年使用:0次
9 . 反应N2(g)+3H2(g)  2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
 2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是
2NH3(g) ΔH<0,若在恒压绝热的容器中发生,下列选项表明一定已达平衡状态的是| A.容器内的温度不再变化 |
| B.容器内的压强不再变化 |
| C.相同时间内,断开H-H键的数目和生成N-H键的数目之比1:1 |
| D.容器内气体的浓度c(N2):c(H2):c(NH3)=1:3:2 |
您最近一年使用:0次
10 . 已知断裂1 mol H2(g)中的H-H键需要吸收436.4 kJ的能量,断裂1 mol O2(g)中的共价键需要吸收498 kJ的能量,生成H2O(g)中的1 mol H-O键能放出462.8 kJ的能量。下列说法正确的是
| A.断裂1 mol H2O中的化学键需要吸收925.6 kJ的能量 |
B.H2(g)+ O2(g)=H2O(g) ΔH=-240.2 kJ·mol-1 O2(g)=H2O(g) ΔH=-240.2 kJ·mol-1 |
| C.2H2O(l)=2H2(g)+O2(g) ΔH=471.6 kJ·mol-1 |
D.H2(g)+ O2(g)=H2O(l) ΔH=-240.2 kJ·mol-1 O2(g)=H2O(l) ΔH=-240.2 kJ·mol-1 |
您最近一年使用:0次




