名校
解题方法
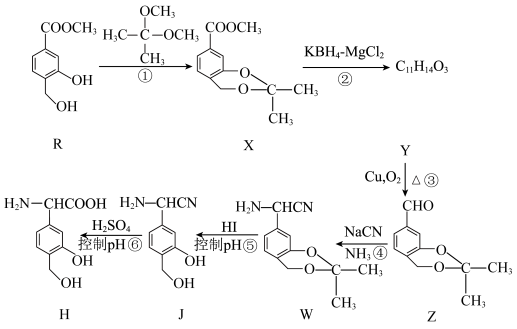
1 . H是一种免疫调节剂,其合成流程如下:
(1)H所含官能团有氨基和_______ 。
(2)X的化学式为_______ ,③的反应类型是_______ 。
(3)设计反应①和⑤的目的是_______ 。
(4)反应①为取代反应,其化学方程式为_______ 。
(5)R的同分异构体M同时满足下列条件:
①M能与氯化铁溶液发生显色反应 ②1 mol M最多能和4 mol NaOH发生反应 ③在核磁共振氢谱上有四组峰且峰的面积之为3∶3∶2∶2.则M的结构简式可能为_______ 。
(6)已知: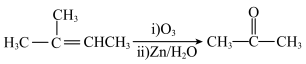 +CH3CHO,结合上述相关信息,以
+CH3CHO,结合上述相关信息,以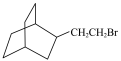 为原料设计合成路线合成
为原料设计合成路线合成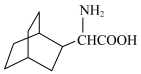 (其他试剂自选)
(其他试剂自选) _______ 。
(1)H所含官能团有氨基和
(2)X的化学式为
(3)设计反应①和⑤的目的是
(4)反应①为取代反应,其化学方程式为
(5)R的同分异构体M同时满足下列条件:
①M能与氯化铁溶液发生显色反应 ②1 mol M最多能和4 mol NaOH发生反应 ③在核磁共振氢谱上有四组峰且峰的面积之为3∶3∶2∶2.则M的结构简式可能为
(6)已知:
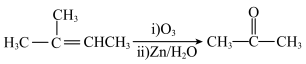 +CH3CHO,结合上述相关信息,以
+CH3CHO,结合上述相关信息,以 为原料设计合成路线合成
为原料设计合成路线合成 (其他试剂自选)
(其他试剂自选)
您最近一年使用:0次
名校
解题方法
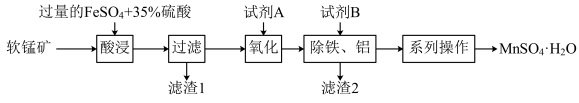
2 . 硫酸锰晶体(MnSO4•H2O)常用作动物饲料的添加剂。工业上以软锰矿(含MnO2和少量的Fe3O4、Al2O3、SiO2)为原料制备硫酸锰晶体的流程如图:
回答下列问题:
(1)“酸浸”前需要将软锰矿粉碎,粉碎的目的是_______ 。
(2)“酸浸”中"MnO2和FeSO4反应的离子方程式为_______ 。
(3)“滤渣1”的主要成分是_______ (填化学式)。“系列操作”包括_______ 、降温结晶、过滤、洗涤、干燥等。
(4)试剂B最好是_______ 。
(5)从绿色化学角度分析,试剂A宜选择_______ (填标号)。
a.HNO3 b.H2O2 c.Cl2 d.K2CrO7
如果省略“氧化”工艺,产品中可能会混有______ (填化学式)。
(6)加入硫酸后H2SO4与Fe3O4反应的离子反应方程式为_______ 。
(7)工业上常用电解硫酸锰的方式制备MnO2,请写出电解池阳极的电极反应式______ 。
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.7 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.8 |
(1)“酸浸”前需要将软锰矿粉碎,粉碎的目的是
(2)“酸浸”中"MnO2和FeSO4反应的离子方程式为
(3)“滤渣1”的主要成分是
(4)试剂B最好是
(5)从绿色化学角度分析,试剂A宜选择
a.HNO3 b.H2O2 c.Cl2 d.K2CrO7
如果省略“氧化”工艺,产品中可能会混有
(6)加入硫酸后H2SO4与Fe3O4反应的离子反应方程式为
(7)工业上常用电解硫酸锰的方式制备MnO2,请写出电解池阳极的电极反应式
您最近一年使用:0次
名校
解题方法
3 . 特定条件下制备的石墨烯具有常温超导的性质,这一发现将导致很多领域发生颠覆性的革命。镓(Ga)、硒(Se)的单质及某些化合物如砷化镓等都是常用的半导体材料,超导材料和半导体材料都广泛应用于航空航天测控、光纤通信等领域。请回答下列问题:
(1)基态硒原子的核外价电子排布式为_____ ,与硒同周期的p区元素中第一电离能大于硒的元素有_____ 种,SeO3的空间构型是_____ 。
(2)一种膦配体M在有机合成中具有较高的应用价值,M的结构简式如图所示:_____ 。
②M中磷原子的杂化轨道类型为_____ 。
③膦配体M是_____ (填“极性”或“非极性”)分子。
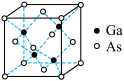
(3)CaAs为原子晶体,密度为ρg .cm-3,其晶胞结构如图所示,则As原子的配位数为_____ ,若Ga和As的原子半径分别为apm和bpm,CaAs晶胞中原子的体积占晶胞体积的百分率为A,则阿伏加德罗常数的值NA=_____ (用字母表示)。
(1)基态硒原子的核外价电子排布式为
(2)一种膦配体M在有机合成中具有较高的应用价值,M的结构简式如图所示:
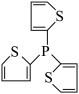
②M中磷原子的杂化轨道类型为
③膦配体M是
(3)CaAs为原子晶体,密度为ρg .cm-3,其晶胞结构如图所示,则As原子的配位数为
您最近一年使用:0次
名校
解题方法
4 . 某地以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)为原料提取氧化铝和磁性氧化铁,用直接碱溶法往往会因形成铝硅酸钠沉淀[NamAlmSinO16(OH)5]而造成铝损失。一种改进后的流程如下:_____ ;NamAlmSinO16(OH)5中的m和n之间的关系式为_____ ;
(2)写出滤渣I主要成分的一种用途:_____ ;
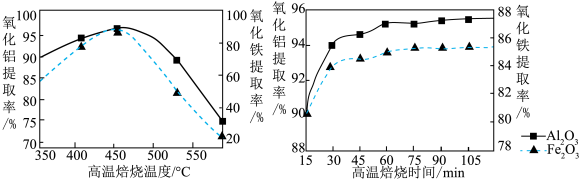
(3)“焙烧Ⅱ”的过程是由氧化铝、氧化铁制得可溶性的NH4Al(SO4) 2、NH4Fe(SO4)2.提取率随温度、时间的变化曲线如图所示,最佳的焙烧时间与温度是_____ 。若用NH4R(SO4) 2表示NH4Al(SO4) 2、NH4Fe(SO4) 2,则相关反应的化学方程式为_____ 。
(5)为了测定Wg高硫铝土矿中铝元素的含量,将流程中制取的Al2O3溶解于足量稀硫酸中,配制成250mL溶液,取出25mL,加入amLcmol·L-1EDTA标准溶液,调节溶液pH约为4.2,煮沸,冷却后用bmol·L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液VmL(已知Al3+、Cu2+与EDTA反应的化学计量数之比均为1:1)。则Wg高硫铝土矿中铝元素的质量分数为_____ (用含V、a、b、c的代数式表示)
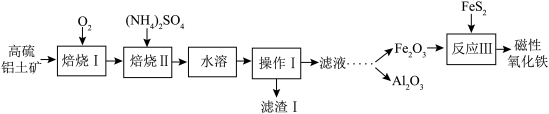
(2)写出滤渣I主要成分的一种用途:
(3)“焙烧Ⅱ”的过程是由氧化铝、氧化铁制得可溶性的NH4Al(SO4) 2、NH4Fe(SO4)2.提取率随温度、时间的变化曲线如图所示,最佳的焙烧时间与温度是
| A.因为原子半径:Na>S,所以离子半径:Na+>S2- |
| B.因为非金属性:S>Si,所以气态氢化物的稳定性:SiH4<H2S |
| C.因为非金属性:O>S,所以沸点:H2S>H2O |
| D.因为金属性:Na>Al,所以碱性:NaOH>Al(OH)3 |
(5)为了测定Wg高硫铝土矿中铝元素的含量,将流程中制取的Al2O3溶解于足量稀硫酸中,配制成250mL溶液,取出25mL,加入amLcmol·L-1EDTA标准溶液,调节溶液pH约为4.2,煮沸,冷却后用bmol·L-1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液VmL(已知Al3+、Cu2+与EDTA反应的化学计量数之比均为1:1)。则Wg高硫铝土矿中铝元素的质量分数为
您最近一年使用:0次
5 . 下列各组物质中,不能满足有图所示关系的一组是(每个箭头表示一步转化)
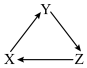
| 选项 | X | Y | Z |
| A | Si | SiO2 | Na2SiO3 |
| B | FeCl2 | Fe | FeCl3 |
| C | Al2O3 | AlCl3 | Al(OH)3 |
| D | SO2 | SO3 | H2SO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
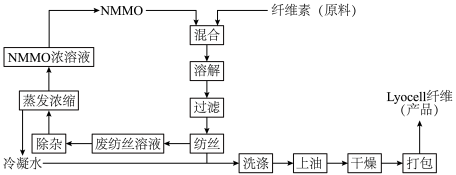
6 . Lyocell纤维是一种使用NMMO的水溶液加工纤维素所得的产品。Lyocell纤维的纺织品具有良好的吸湿透气性。NMMO是一种无毒的有机化合物。纤维素加工的工艺流程如下图所示:___________ 。
(2)Lyocell纤维被称为“绿色纤维”,从工艺流程来看,原因是___________ 。
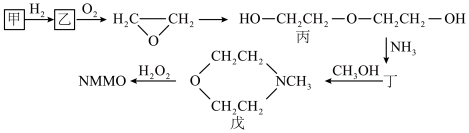
(3)NMMO的合成路线如下(各步合成条件省略):
①化合物丙所含的官能团名称是___________ 和___________ 。
②加热加压条件下,环氧乙烷合成丙的反应式是___________ 。
③化合物丁属于脂环化合物,其结构简式是___________ 。
④化合物戊的一种同分异构体无支链,且与氢氧化钠水溶液共热时生成一种无机气体,该气体能使湿润的石蕊试纸变蓝。则该同分异构体的结构简式是___________ 。
(4)Lyocell纤维制成的面料容易勾丝,不耐暴晒。而腈纶弹性优异,耐光性好。因此,将两种纤维混纺,可以实现性能互补。请写出以(3)中化合物甲为原料合成腈纶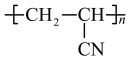 的各步反应式:
的各步反应式:___________ 。
(2)Lyocell纤维被称为“绿色纤维”,从工艺流程来看,原因是
(3)NMMO的合成路线如下(各步合成条件省略):
①化合物丙所含的官能团名称是
②加热加压条件下,环氧乙烷合成丙的反应式是
③化合物丁属于脂环化合物,其结构简式是
④化合物戊的一种同分异构体无支链,且与氢氧化钠水溶液共热时生成一种无机气体,该气体能使湿润的石蕊试纸变蓝。则该同分异构体的结构简式是
(4)Lyocell纤维制成的面料容易勾丝,不耐暴晒。而腈纶弹性优异,耐光性好。因此,将两种纤维混纺,可以实现性能互补。请写出以(3)中化合物甲为原料合成腈纶
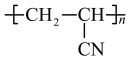 的各步反应式:
的各步反应式:
您最近一年使用:0次
名校
7 . 苯甲酸的熔点为122.13℃,微溶于水,易溶于酒精,实验室制备少量苯甲酸的流程如图:

| A.“操作1”过程中玻璃棒的作用为搅拌 | B.“操作2”为酸化过程,可使用稀硫酸 |
| C.“冷凝回流”过程中一定需要直形蒸馏管 | D.为提高苯甲酸固体的纯度,可用热水洗涤晶体 |
您最近一年使用:0次
2024-07-12更新
|
57次组卷
|
2卷引用:广西壮族自治区柳州高级中学2022-2023学年高三上学期1月考试理科综合试题-高中化学
名校
解题方法
8 . 在有机合成中,常需将官能团消除或增加,下列合成路线不简洁的是
A.乙烯→乙二醇: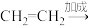 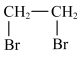  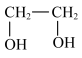 |
B.溴乙烷→乙醇: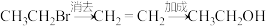 |
C.1-溴丁烷→1-丁炔: 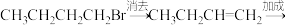 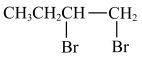  |
D.乙烯→乙炔: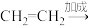 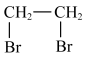  |
您最近一年使用:0次
2024-06-15更新
|
83次组卷
|
17卷引用:考点44 有机综合推断-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点44 有机综合推断-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第55练 有机合成-2023年高考化学一轮复习小题多维练(全国通用)课后-3.5.1 有机合成的主要任务-人教版2019选择性必修3(已下线)第20讲 有机合成的主要任务(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)黑龙江省七台河市勃利县高级中学2021-2022学年高二下学期期中考试化学试题第五节 有机合成陕西省延安市第一中学2021-2022学年高二下学期期中考试化学试题广东省汕头市金禧中学2023-024学年高三上学期第一次阶段考试化学试题重庆市凤鸣山中学2020-2021学年高二下学期期中考试化学试题(人教2019)选择性必修3第三章 第五节 有机合成江苏省盐城市东台创新高级中学2020-2021学年高二3月份月检测化学试题宁夏吴忠市青铜峡市高级中学2020-2021学年高二下学期期末考试化学试题(已下线)烃的衍生物——课时7有机合成河北省唐山市乐亭第一中学2022-2023学年高二下学期6月月考化学试题3.5有机合成 随堂练习(已下线)专题05 有机反应类型与有机合成 -备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)浙江省新力量联盟2023-2024学年高二下学期4月期中考试化学试题
名校
9 . 氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
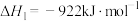
Ⅱ.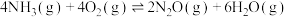
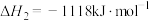
Ⅲ.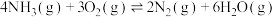

已知:298K时,相关物质的焓的数据如图。
___________  。
。
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为___________ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
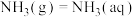

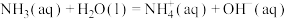

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度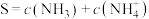 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为___________ 。
(4)由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
已知: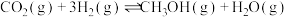 的
的 -49.5kJ/mol
-49.5kJ/mol
反应②:

反应③: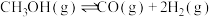
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。___________  。
。
Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入
 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在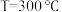 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在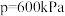 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。
ii. 点
点 的分压为
的分压为___________  ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
___________  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中 点的
点的 高于
高于 点的原因是
点的原因是___________ 。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:Ⅰ.

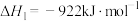
Ⅱ.
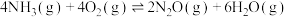
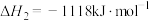
Ⅲ.
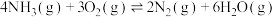

已知:298K时,相关物质的焓的数据如图。


 。
。(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。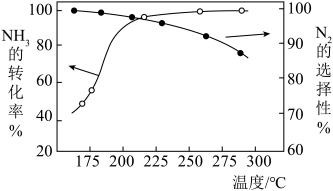
 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
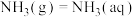

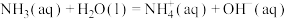

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度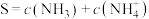 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)由
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。已知:
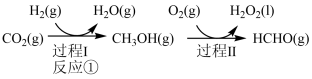
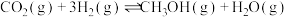 的
的 -49.5kJ/mol
-49.5kJ/mol反应②:


反应③:
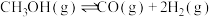
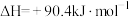
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
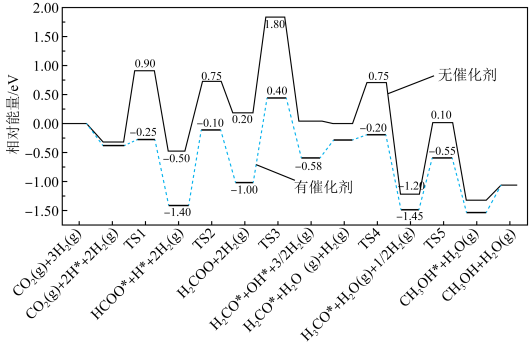
 。
。Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入

 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在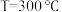 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在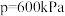 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。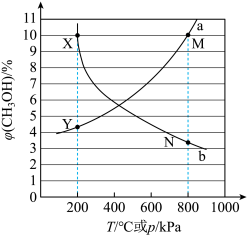
 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。ii.
 点
点 的分压为
的分压为 ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中
 点的
点的 高于
高于 点的原因是
点的原因是
您最近一年使用:0次
名校
10 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
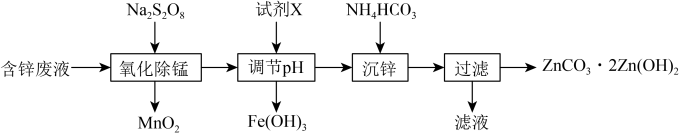
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次



