1 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>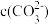 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+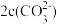 + + | D.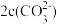 + + + +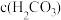 <c(Na+) <c(Na+) |
您最近一年使用:0次
名校
2 . 环境科学研究发现, 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为__________ ;在相同温度和压强下,1mol  和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:
试分析在相同温度时,催化剂2催化下 的转化率更高的原因是
的转化率更高的原因是___________ 。
(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示: 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的___________ 曲线(填“a”或“b”)。
②要缩短b曲线对应容器达到平衡的时间,但不改变 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是___________ (答出一条即可)。
③500℃该反应的化学平衡常数K=___________ (用最简分数表示)。
④实验测定该反应的反应速率 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
___________ (保留两位小数)。
 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为 和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:| 实验 | 温度/℃ | 催化剂 |  的转化率/% 的转化率/% |
| 实验1 | 400 | 催化剂1 | 9.5 |
| 400 | 催化剂2 | 10.6 | |
| 实验2 | 500 | 催化剂1 | 12.3 |
| 500 | 催化剂2 | 13.5 |
 的转化率更高的原因是
的转化率更高的原因是(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol
 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示:
 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的②要缩短b曲线对应容器达到平衡的时间,但不改变
 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是③500℃该反应的化学平衡常数K=
④实验测定该反应的反应速率
 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
您最近一年使用:0次
名校
3 . 已知反应: 。在一定压强下,按
。在一定压强下,按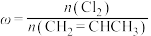 向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
 。在一定压强下,按
。在一定压强下,按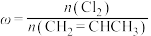 向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的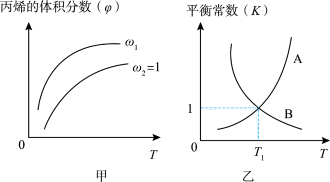
A.图甲中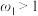 |
| B.图乙中,线A表示正反应的平衡常数 |
| C.若在恒容绝热装置中开始上述反应,达到平衡时装置内的气体压强始终不变 |
D.温度 、 、 , , 的转化率约为33.3% 的转化率约为33.3% |
您最近一年使用:0次
名校
4 . 已知: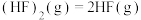 △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
△H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
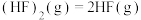 △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
△H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是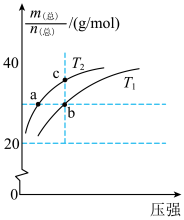
A.反应速率: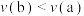 |
B.温度: |
C.当m(总)/n(总)=30g/mol时,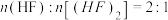 |
| D.欲测定HF的相对分子质量,宜在低温高压下进行 |
您最近一年使用:0次
名校
解题方法
5 . 在恒温恒压下,向密闭容器中充入4mol  和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是
 和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是A.若反应开始时容器体积为2L,则 |
B.若把条件“恒温恒压”改为“恒压恒容”,则平衡后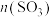 大于1.4mol 大于1.4mol |
C.2min后,向容器中再通入一定量的 气体,重新达到平衡时 气体,重新达到平衡时 的含量变小 的含量变小 |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近一年使用:0次
名校
6 . 下列关于化学反应速率和化学平衡的说法正确的是
| A.化学平衡常数K变化,平衡不一定发生移动 |
B.已知反应: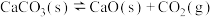 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 ,在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时 (g)的浓度将升高 (g)的浓度将升高 |
C.两个体积相同的容器中充入等量的 发生反应: 发生反应: △H<0,绝热容器中气体的颜色比铁制容器中颜色深 △H<0,绝热容器中气体的颜色比铁制容器中颜色深 |
| D.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
您最近一年使用:0次
名校
7 . 在室温下,下列四种溶液:①0.1 mol/L NH4Cl溶液,②0.1 mol/L CH3COONH4溶液,③0.1mol/L NH4HSO4溶液,④0.1 mol/L氨水。
(1)溶液①呈酸性的原因是___________ (用离子方程式表示)。
(2)溶液③的电离方程式为___________
(3)在上述①、②、 ③、④溶液中c ( )浓度由大到小的顺序是
)浓度由大到小的顺序是___________ (填序号)。
(4)25℃时,将pH=9的NaOH溶液与p=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。
(5)25℃时,向0.1mol/L FeCl3溶液中加入④溶液,若Fe(OH)3的Ksp=1×10-39,当铁离子恰好完全沉淀时[当c(Fe3+)小于10-6mol/L时,可忽略不计],溶液的pH=___________ 。
(1)溶液①呈酸性的原因是
(2)溶液③的电离方程式为
(3)在上述①、②、 ③、④溶液中c (
 )浓度由大到小的顺序是
)浓度由大到小的顺序是(4)25℃时,将pH=9的NaOH溶液与p=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(5)25℃时,向0.1mol/L FeCl3溶液中加入④溶液,若Fe(OH)3的Ksp=1×10-39,当铁离子恰好完全沉淀时[当c(Fe3+)小于10-6mol/L时,可忽略不计],溶液的pH=
您最近一年使用:0次
名校
8 . 结晶玫瑰和高分子树脂M的合成路线如下图所示:
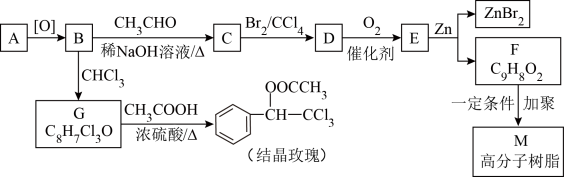
已知:①A是苯的同系物,在相同条件下,其蒸气相对于氢气的密度为46
② (-R表示烃基)
(-R表示烃基)
③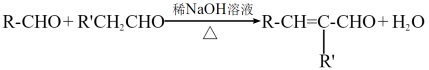 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)
④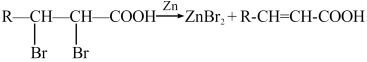
(1)C中官能团的名称为_______ ,E的结构简式为_______ 。
(2)写出由G生成结晶玫瑰的化学方程式:_______ 。
(3)上述流程中“C→D”在M的合成过程中的作用是_______ 。
(4)已知G在一定条件下水解生成H(C8H8O3),与H有相同官能团且与氯化铁溶液发生显色反应的同分异构体的数目有_______ 种。
(5)E的同分异构体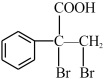 是一种重要的药物中间体,其合成路线与E相似,请以
是一种重要的药物中间体,其合成路线与E相似,请以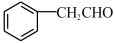 为原料设计它的合成路线
为原料设计它的合成路线_______ (其他所需原料自选)。

已知:①A是苯的同系物,在相同条件下,其蒸气相对于氢气的密度为46
②
 (-R表示烃基)
(-R表示烃基)③
 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)④
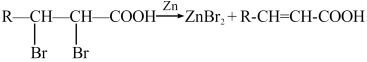
(1)C中官能团的名称为
(2)写出由G生成结晶玫瑰的化学方程式:
(3)上述流程中“C→D”在M的合成过程中的作用是
(4)已知G在一定条件下水解生成H(C8H8O3),与H有相同官能团且与氯化铁溶液发生显色反应的同分异构体的数目有
(5)E的同分异构体
 是一种重要的药物中间体,其合成路线与E相似,请以
是一种重要的药物中间体,其合成路线与E相似,请以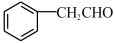 为原料设计它的合成路线
为原料设计它的合成路线
您最近一年使用:0次
名校
解题方法
9 . 有机物X完全燃烧的产物只有二氧化碳和水,元素组成分析发现,该物质中碳元素的质量分数为64.86%,氢元素的质量分数为13.51%,它的核磁共振氢谱有5组明显的吸收峰,且只含有两个甲基。下列关于有机物X的说法正确的是
A.分子式为 | B.X只可能催化氧化成醛 |
| C.与X互为官能团异构的同分异构体有3种 | D.X可能消去生成两种结构的烯烃 |
您最近一年使用:0次
10 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼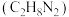 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。
已知:①

②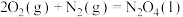

③

请写出上述反应的热化学方程式:______ 。
(2)碘蒸气存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。
下列表述正确的是______。
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中 和
和 发生反应
发生反应

 。实验测得:
。实验测得: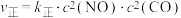 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数______ (填“大于”“小于”或“等于”) 增大的倍数
增大的倍数
②若在 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则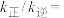
______ 。(保留小数点后两位)
(4)实验室用 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中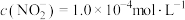 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算______ (填“能”或“不能”)产生 沉淀。
沉淀。
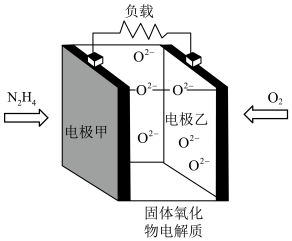
(5)一种以液态肼 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:______ 。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼
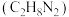 ,
, 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热。
,并放出大量热。已知:①


②
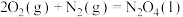

③


请写出上述反应的热化学方程式:
(2)碘蒸气存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程 (k为速率常数)。
(k为速率常数)。下列表述正确的是______。
A. 分解反应中,k值与碘蒸气浓度大小有关 分解反应中,k值与碘蒸气浓度大小有关 |
| B.第二步对总反应速率起决定作用 |
| C.第二步活化能比第三步大 |
| D.IO为反应的催化剂 |
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中
 和
和 发生反应
发生反应

 。实验测得:
。实验测得: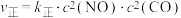 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 增大的倍数
增大的倍数②若在
 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则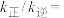
(4)实验室用
 溶液处理
溶液处理 ,已知
,已知 ,某吸收液中溶质只含
,某吸收液中溶质只含 ,溶液中
,溶液中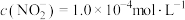 ,取该溶液
,取该溶液 ,加1滴
,加1滴 的
的 溶液混合均匀(20滴约为
溶液混合均匀(20滴约为 ),估算
),估算 沉淀。
沉淀。(5)一种以液态肼
 为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达
为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
您最近一年使用:0次



