1 . 如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
A.A、B简单离子半径大小关系为 |
B.D、E形成的简单离子的还原性: |
C.气态氢化物的稳定性: |
D.最高价氧化物对应的水化物的酸性: |
您最近一年使用:0次
名校
2 . 已知R、W、X、Y、Z均为短周期主族元素,其中R元素所在的周期数是其族序数的一半,且对应的两种常见氧化物均为酸性氧化物,W元素与Z元素在同一主族,X与其同主族另一元素单质形成的合金可用作原子反应堆导热剂,Y元素原子最外层电子数为m,次外层电子数为n,Z元素原子L层电子数为m+n,M层电子数为m-n,下列叙述中错误的是
A.R、X、Y对应的简单离子半径: |
| B.相同温度下,同浓度的R、W、Z的最高价含氧酸的酸性:R>W>Z |
C.将 与 与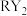 分别通入 分别通入 溶液中,现象不同 溶液中,现象不同 |
| D.因为Y的氢化物比R的氢化物稳定,所以Y的氢化物的熔、沸点比R的氢化物的熔、沸点高 |
您最近一年使用:0次
2023-02-16更新
|
1245次组卷
|
7卷引用:山西省怀仁市第一中学校北校区2022届高三高考预测猜题卷理科综合化学试题
解题方法
3 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W与X形成的某种化合物是一种红棕色有刺激性气味的气体,Y的周期数是族序数的3倍,Z核外最外层电子数与W核外电子总数相同。下列叙述错误的是
| A.X与其他三种元素均可形成两种或两种以上的二元化合物 |
| B.W、X、Y、Z的最高正化合价分别为+5、+6、+1、+7 |
| C.简单离子半径:Z>W>X>Y |
| D.单质的熔点:Y>Z |
您最近一年使用:0次
2022-11-17更新
|
146次组卷
|
2卷引用:山西省金科大联考2022-2023学年高三上学期11月质量检测化学试题
名校
解题方法
4 . 图所示的两种化合物可应用于阻燃材料和生物材料的合成,其组成元素W、X、Y、Z为原子序数依次增大的短周期元素,其中W与Z的原子序数之和等于X与Y的原子序数之和,且Z元素原子的价电子数等于W的原子序数。下列说法错误的是


A.原子半径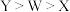 | B.简单气态氢化物的热稳定性 |
| C.W、Z元素的氧化物对应的水化物都是强酸 | D.Mg在W的单质中燃烧的产物中只含有离子键 |
您最近一年使用:0次
2022-11-16更新
|
459次组卷
|
2卷引用:山西省三晋名校联盟2022-2023学年高三上学期毕业班阶段性测试(二)化学试题
解题方法
5 . 已知短周期主族元素X、Y、Z、W的原子序数依次增大,其中W和X原子的最外层电子数之差等于Z与Y原子的最外层电子数之差。它们形成的单质和化合物之间转化的关系如图,常温下d是无色液体,液态f可用作制冷剂。下列说法不正确的是


A.简单离子半径: |
B.第一电离能: |
C.电负性: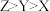 |
| D.X、Z形成的化合物中可能含有非极性键和极性键 |
您最近一年使用:0次
6 . 短周期主族元素X、Y、Z、W在元素周期表的相对位置如图所示,它们的原子序数之和为39。下列说法错误的是
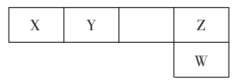
| A.常温常压下,X单质为固态 | B.Z和W的主要化合价相同 |
C.原子半径: | D.Y的氢化物与W的氢化物相遇产生白烟 |
您最近一年使用:0次
7 . 五种短周期主族元素X、Y、Z、W、R的原子序数依次增大,Z和R位于同主族,五种元素组成一种生活中常见的结晶水合物M,M的化学式为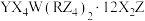 。向一定量M的水溶液中滴加烧碱溶液,沉淀的物质的量(n)与
。向一定量M的水溶液中滴加烧碱溶液,沉淀的物质的量(n)与 溶液体积(V)的关系如图所示。下列叙述错误的是
溶液体积(V)的关系如图所示。下列叙述错误的是
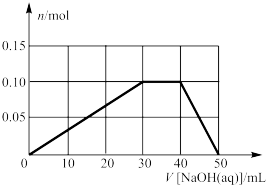
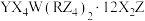 。向一定量M的水溶液中滴加烧碱溶液,沉淀的物质的量(n)与
。向一定量M的水溶液中滴加烧碱溶液,沉淀的物质的量(n)与 溶液体积(V)的关系如图所示。下列叙述错误的是
溶液体积(V)的关系如图所示。下列叙述错误的是
A.简单离子半径: | B.X、Y、Z三种元素只能组成一种离子化合物 |
C.第一电离能: | D.工业上用电解熔融的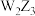 制备单质W 制备单质W |
您最近一年使用:0次
2022-10-28更新
|
96次组卷
|
2卷引用:山西省忻州市2022-2023学年高三上学期10月联考化学试题
解题方法
8 . W、X、Y、Z、M是五种位于三个不同短周期的主族元素。已知:①X、Y为同主族;②常温下, X、Y、Z、M的最高价氧化物对应水化物的pH如图所示。
X、Y、Z、M的最高价氧化物对应水化物的pH如图所示。

下列说法错误的是
 X、Y、Z、M的最高价氧化物对应水化物的pH如图所示。
X、Y、Z、M的最高价氧化物对应水化物的pH如图所示。
下列说法错误的是
| A.原子半径从大到小的顺序是Y>Z>M>X>W |
| B.W形成的阴离子核外电子排布与氦原子相同 |
| C.X、Y、Z、M的最高价含氧酸都具有强氧化性 |
D.X、Y、Z、M与W均可形成含有 的化合物 的化合物 |
您最近一年使用:0次
2022-09-08更新
|
143次组卷
|
2卷引用:山西省2022-2023学年高三上学期第一次摸底考试化学试题
名校
9 . 图为元素周期表的一部分,请参照①~⑧在表中的位置,回答下列问题:

(1)②在周期表中的位置是___________ 。
(2)①~⑧中,化学性质最稳定的是___________ (填元素符号),非金属性最强的是___________ (填元素符号),最高价氧化物对应水化物酸性最强的是___________ (填化学式)。
(3)①~⑦中,原子半径最大的是___________ (填元素符号)。
(4)元素③的非金属性比⑥___________ (填“强”或“弱”),请从原子结构的角度解释:___________ ,列举一个化学事实加以说明___________ 。
(5)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。
工业制备镓的流程如下图所示:
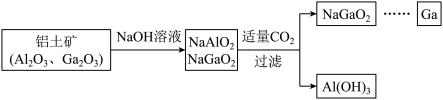
氧化镓与NaOH反应的化学方程式为___________ 。酸性:Al(OH)3___________ Ga(OH)3(填“>”或“<”),冶炼金属镓的方法是___________ (填序号)。
A.热还原法 B.热分解法 C.电解法

(1)②在周期表中的位置是
(2)①~⑧中,化学性质最稳定的是
(3)①~⑦中,原子半径最大的是
(4)元素③的非金属性比⑥
(5)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。
工业制备镓的流程如下图所示:

氧化镓与NaOH反应的化学方程式为
A.热还原法 B.热分解法 C.电解法
您最近一年使用:0次
名校
解题方法
10 . 某化合物的结构式如图所示,其中短周期元素X、Y、Z、W原子序数依次增大,且Y、W同主族。下列叙述正确的是
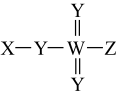
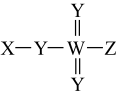
| A.原子半径:X<Y<Z<W |
| B.简单氢化物的沸点:Y>W |
| C.W的氧化物的水化物是强酸 |
D.单质与 反应的难易程度:W>Z 反应的难易程度:W>Z |
您最近一年使用:0次
2022-07-20更新
|
202次组卷
|
3卷引用:山西省大同市第二中学校2023届高三上学期开学考试化学试题



