名校
解题方法
1 . 类推的思维方法在化学学习中应用广泛,但类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论错误的是
A. 能与 能与 溶液反应,则 溶液反应,则 也能与 也能与 溶液反应 溶液反应 |
B. 是“V形”分子,则 是“V形”分子,则 是“V形”分子 是“V形”分子 |
C.第二周期元素氢化物稳定性顺序是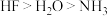 ,则第三周期元素氢化物稳定性顺序也是 ,则第三周期元素氢化物稳定性顺序也是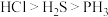 |
D.工业制 采用电解熔融 采用电解熔融 的方法,则工业制 的方法,则工业制 也可采用电解熔融 也可采用电解熔融 的方法 的方法 |
您最近一年使用:0次
2024-02-18更新
|
147次组卷
|
2卷引用:安徽省六安第一中学2023-2024学年高二上学期期末考试化学试题
名校
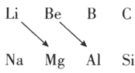
2 . 在元素周期表中的某些元素之间存在着特殊的“对角线规则”,如Li和Mg、Be和Al、B和Si的一些性质相似。下列说法不正确的是
| A.氢氧化铍是两性氢氧化物 | B.B和Si的密度相近 |
| C.Li在N2中燃烧生成Li3N | D.Li和Mg的原子半径相近,且核外电子排布相同 |
您最近一年使用:0次
3 . 镁、锂在元素周期表中具有特殊的“对角线”关系,它们的性质相似。下列有关锂的性质的叙述,不正确的是
| A.Li2SO4易溶于水 | B.LiOH是受热不易分解的强碱 |
| C.Li遇浓硫酸不产生“钝化”现象 | D.Li2CO3受热分解,生成Li2O和CO2 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
4 . 下列各组离子中,可能能在所处环境中大量共存的是
A.在室温环境下c(OH-)=1×10-11的溶液中:Cr2+,SO ,NO ,NO ,Na+ ,Na+ |
B.在4℃的水溶液中:Be2+,K+,PO ,OH- ,OH- |
C.在漂白液中:OH-,Rb+,SO ,CO ,CO |
| D.在水玻璃中:H+,SCN-,Cl-,Cs+ |
您最近一年使用:0次
名校
5 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:___________ B:___________ G___________ ,写出元素B的基态原子的轨道表示式:___________ 。
(2)C、D、E三种元素的原子半径由大到小的顺序___________ 。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:___________ ,___________ ,___________ ,其中C的简单气态氢化物的键角为:___________ 。
(4)已知元素A、B形成的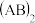 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为___________ 。
(5)F元素的简单阴离子结构示意图___________ 。电解D与F形成的化合物的水溶液在工业上有着重要应用,试写出其电解的总的化学反应方程式:___________ 。
(6)元素G位于周期表的___________ 区,其价电子的排布式为:___________ ,该元素可形成 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”)。推测M的最高价氧化物对应水化物___________ (填“能”或“不能”)与D的最高价氧化物对应水化物发生反应。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属 |
(2)C、D、E三种元素的原子半径由大到小的顺序
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
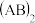 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为(5)F元素的简单阴离子结构示意图
(6)元素G位于周期表的
 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
2022-03-03更新
|
652次组卷
|
2卷引用:安徽省蚌埠市蚌埠铁路中学2023-2024学年高二下学期期中考试化学试题
6 . (1)观察Li、Be、Mg、Al在元素周期表中的位置回答下列问题:______ (填“酸性”“碱性”或“两性”)化合物,证明这一结论的有关的离子方程式是______ 。
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为______ (用化学式表示)。
(2)现有核电荷数小于20的元素A,其电离能数据如表:( 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: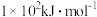 )
)
①外层电子离核越远,能量越高,电离能越______ (填“大”或“小”);阳离子所带电荷数越大,失去电子时,电离能越______ (填“大”或“小”)。
②表中11个电子分属______ 个电子层;失去了11个电子后,该元素原子还有______ 个电子。
③该元素最高价氧化物对应的水化物的化学式是______ 。
②根据Mg在空气中的燃烧情况可知,Li在空气中燃烧,生成的产物为
(2)现有核电荷数小于20的元素A,其电离能数据如表:(
 表示原子失去第n个电子的电离能,单位:
表示原子失去第n个电子的电离能,单位: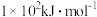 )
)| 序号 |  |  |  |  | 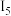 |  | 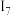 | 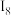 | 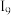 |  |  | … |
| 电离能 | 7.644 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 | 224.9 | 266.0 | 327.9 | 367.4 | 1761 | … |
②表中11个电子分属
③该元素最高价氧化物对应的水化物的化学式是
您最近一年使用:0次
2021-02-06更新
|
477次组卷
|
2卷引用:安徽省安庆市怀宁二中2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
7 . 已知下列四组短周期元素的电离能数据(kJ·mol-1), 下列判断不正确的是
| 电离能 | W | X | Y | Z |
| I1 | 496 | 573 | 738 | 899 |
| I2 | 4562 | 1817 | 1451 | 1751 |
| I3 | 6912 | 2745 | 7733 | 14848 |
| I4 | 9543 | 11575 | 10540 | 21006 |
| A.W单质的还原性最强 | B.Y和Z可能位于同一族 |
| C.X、Z的氢氧化物都具有两性 | D.W、X、Y原子半径依次减小 |
您最近一年使用:0次
2020-09-04更新
|
135次组卷
|
2卷引用:安徽省阜阳市2020-2021学年高二下学期段考化学试题
名校
8 . 运用元素周期律分析下面的推断,其中错误的是( )
①硒化氢(H2Se)是无色,有毒,比H2S稳定的气体
②铊(T既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气
③砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸
④锂在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤硫酸锶(SrSO4)是难溶于水的白色固体
①硒化氢(H2Se)是无色,有毒,比H2S稳定的气体
②铊(T既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气
③砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于稀酸
④锂在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤硫酸锶(SrSO4)是难溶于水的白色固体
| A.①②③④ | B.①②④ | C.①③⑤ | D.②④⑤ |
您最近一年使用:0次
2020-02-16更新
|
112次组卷
|
2卷引用:安徽省合肥市第一中学2019-2020学年高二上学期开学考试化学试题
13-14高一下·四川成都·期中
名校
9 . 锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物叙述正确的是( )
| A.Li2SO4难溶于水 |
| B.Li与N2反应的产物是Li3N |
| C.LiOH易溶于水 |
| D.LiOH与Li2CO3受热都很难分解 |
您最近一年使用:0次
2016-12-09更新
|
511次组卷
|
14卷引用:安徽省滁州市九校2021-2022学年高二下学期3月月考化学试题
安徽省滁州市九校2021-2022学年高二下学期3月月考化学试题2014-2015黑龙江省哈尔滨六中高二上期末化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时贵州省遵义育新高级中学2018-2019学年高二上学期11月月考化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题湖北省武汉市钢城四中2018-2019学年高二下学期期中考试化学试题辽宁省抚顺市第一中学2019-2020高二下学期期中考试化学试题甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(普通班)吉林省汪清四中2020-2021学年高二下学期第二阶段考试化学试题云南省通海县第一中学2021-2022学年高二下学期3月月考化学试题内蒙古赤峰市元宝山区第一中学2021-2022学年高二下学期期中考试化学试题(已下线)BBWYhjhx1113.pdf(已下线)2013-2014四川省成都市五校高一下学期期中联考化学试卷(已下线)专题09 常见金属元素的性质及应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)



