名校
1 . “芯片”决定手机的发展,芯片中的主要材质是硅。如图所示是硅原子的构成示意图,下列说法错误的是

| A.硅元素属于金属元素 |
B.硅原子的结构示意图为 |
| C.硅在元素周期表内位列第三周期 |
| D.硅原子不带电的原因是其质子数与核外电子数目相同,电性相反 |
您最近一年使用:0次
名校
解题方法
2 . 在我国“两弹一星”试验中,许多科学家都做出了突出贡献。我国科学家研制“两弹”所涉及的基本核反应方程式有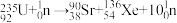 ,下列说法正确的是
,下列说法正确的是
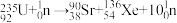 ,下列说法正确的是
,下列说法正确的是| A.Xe位于第四周期 | B.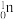 代表的是质子 代表的是质子 |
C.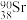 中有52个中子 中有52个中子 | D.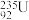 与 与 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
2024-03-04更新
|
214次组卷
|
3卷引用:安徽省灵璧中学名校联考2023-2024学年高一上学期1月阶段性考试化学试题
名校
解题方法
3 . 近年来,氮化镓以其直接带隙宽、热导率高、化学稳定性好以及抗辐射能力强等优势,成为第三代半导体材料中的佼佼者,目前我国雷达已采用氮化镓,技术世界领先。下列说法错误的是
| A.氮化镓属于新型材料 |
| B.氮化镓化学式为GaN |
| C.镓元素在周期表的第四周期第IVA族 |
| D.镓既能与盐酸反应,又能与NaOH溶液反应 |
您最近一年使用:0次
名校
4 . 已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol 丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件已略去)。
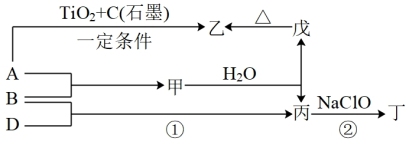
请回答:
(1)单质B的组成元素在周期表中的位置是___________ 。
(2)写出戊与强碱反应的离子方程式:___________ 。
(3)丁中所包含的化学键类型有___________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为___________ 。
(5)反应②中,0.5molNaClO参加反应时,转移1mol电子,其化学方程式为___________ 。
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为___________ 。

请回答:
(1)单质B的组成元素在周期表中的位置是
(2)写出戊与强碱反应的离子方程式:
(3)丁中所包含的化学键类型有
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为
(5)反应②中,0.5molNaClO参加反应时,转移1mol电子,其化学方程式为
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为
您最近一年使用:0次
5 . 科学院院士张青莲教授曾主持测定了铟(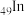 )等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(
)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(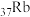 )同周期,下列说法不正确的是
)同周期,下列说法不正确的是
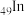 )等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(
)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷(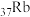 )同周期,下列说法不正确的是
)同周期,下列说法不正确的是A. 是第五周期IVA元素 是第五周期IVA元素 | B.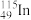 的中子数与电子数的差值为17 的中子数与电子数的差值为17 |
C.碱性: | D.原子半径: |
您最近一年使用:0次
名校
6 . 科学家利用回旋加速器,用钙原子轰击钚原子得到了鈇元素,半衰期达30秒。下列有关说法错误的是
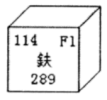

| A.鈇元素的质子数为114 | B.鈇元素属于第七周期IVA族 |
| C.鈇元素的主要化合价有+4、+2 | D.鈇元素是过渡元素 |
您最近一年使用:0次
2021-04-21更新
|
193次组卷
|
2卷引用:安徽省宿州市十三所重点中学2020-2021学年高一下学期期中质量检测化学试题
解题方法
7 . 下表是元素周期表的一部分,根据表中8种元素,用元素符号等化学用语填空。
(1)①~⑧元素中,金属性最强的是___________  写元素符号
写元素符号 。
。
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图___________ 。
(3)②、③、⑥所形成的简单离子,其半径由大到小的顺序是___________  写离子符号
写离子符号 。
。
(4)将 铁粉和氧化铁的混合物中加入
铁粉和氧化铁的混合物中加入 的稀硫酸,恰好完全反应,放出氢气
的稀硫酸,恰好完全反应,放出氢气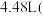 标准状况
标准状况 反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
①发生的化学反应中有一个属于化合反应,写出其离子方程式___________ 。
②混合物中氧化铁是___________ g。
③原稀硫酸的物质的量浓度___________  。
。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 写元素符号
写元素符号 。
。(2)①~⑧元素中,画出最稳定的元素的原子结构示意图
(3)②、③、⑥所形成的简单离子,其半径由大到小的顺序是
 写离子符号
写离子符号 。
。(4)将
 铁粉和氧化铁的混合物中加入
铁粉和氧化铁的混合物中加入 的稀硫酸,恰好完全反应,放出氢气
的稀硫酸,恰好完全反应,放出氢气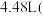 标准状况
标准状况 反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:
反应后的溶液中滴加KSCN不显红色,且无固体剩余物。求:①发生的化学反应中有一个属于化合反应,写出其离子方程式
②混合物中氧化铁是
③原稀硫酸的物质的量浓度
 。
。
您最近一年使用:0次
解题方法
8 . 2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据元素性质、相对原子质量等进行排列,预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法错误的是


| A.乙元素位于现行元素周期表第四周期第ⅥA族 |
B.原子序数:乙>甲> |
C.乙的简单气态氢化物的稳定性弱于 |
| D.推测乙的单质可以用作半导体材料 |
您最近一年使用:0次
2021-02-01更新
|
322次组卷
|
2卷引用:安徽省滁州市定远县民族中学2021-2022学年高二下学期期中考试化学试题
名校
9 . 2019年是门捷列夫提出元素周期表150周年。根据元素周期律和元素周期表,下列推断合理的是
| A.卤族元素的原子最外层都排7个电子,在反应中只能做氧化剂得到电子 |
| B.位于第三周期第13列的元素为非金属元素 |
| C.位于ⅠA族的元素都是活泼的金属元素 |
| D.第七周期0族元素的原子序数为118 |
您最近一年使用:0次
2021-01-09更新
|
241次组卷
|
4卷引用:安徽省涡阳一中2020-2021年高一上学期期末考试化学试题
安徽省涡阳一中2020-2021年高一上学期期末考试化学试题浙江省建德市严州中学新安江校区2020-2021学年高一上学期1月月考化学试题(已下线)练习10 元素的性质与原子结构-2020-2021学年【补习教材·寒假作业】高一化学(人教版)(已下线)【浙江新东方】高中化学20210304-017
10 . 下列根据元素周期表和元素周期律得出的推断中正确的是
| A.金属元素原子最外层电子数越少,该金属失电子能力越强 |
| B.若存在简单阴离子R2-,则R一定位于ⅥA族 |
| C.aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b |
| D.铅位于周期表中金属和非金属的交界处,可做半导体材料 |
您最近一年使用:0次



