名校
解题方法
1 . 四种短周期元素W、X、Y、Z的原子序数依次增大,W元素的最外层电子数是其电子层数的二倍;X的原子半径是短周期主族元素原子中最大的;Y是地壳中含量最多的金属元素;X与Z形成的离子化合物的水溶液呈中性。下列叙述中,不正确 的是
| A.将W的最高价氧化物通入到Na2SiO3溶液中,生成白色沉淀,得出非金属性:W>Si |
| B.将X单质投入到CuSO4溶液中,生成紫红色固体 |
| C.工业上用电解熔融Y的氧化物的方法冶炼金属Y |
| D.Z的气态氢化物的沸点在同主族中最低 |
您最近一年使用:0次
2018-04-01更新
|
495次组卷
|
7卷引用:专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-测试
名校
2 . 短周期主族元素X、Y、Z、W原子序数依次增大,X 与Y、Z、W不在同一周期,Y最外层电子数是次外层电子数的3倍,W与Y同主族,Z是地壳中含量最多的金属元素。下列说法正确的是( )
| A.Y的单质的氧化性比W的弱 |
| B.原子半径:r(X)< r(Y)< r(W)< r(Z) |
| C.化合物X2Y和Z2Y3,含有相同类型的化学键 |
| D.元素Y、Z形成的化合物熔点高,不能用电解法制备其中的金属单质 |
您最近一年使用:0次
2018-01-13更新
|
443次组卷
|
5卷引用:河南省实验中学2021-2022学年高三上学期期末考试化学试题
名校
解题方法
3 . 元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________ ;Z3+的离子结构示意图是____________ 。
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式__________ ;M和N气态氢化物的稳定性大小比较为________ (用化学式和“>”“<”或“=”表示)。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________ .
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_____________________________ 。
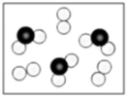
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是__________ (填化学式),示意图中转移电子的数目为______ 。


(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______________________ 。
(1)R在元素周期表中的位置是
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是



(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
2017-12-08更新
|
236次组卷
|
3卷引用: 安徽省舒城中学2021-2022学年高一下学期第一次月考化学试题
名校
4 . 已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素。下列说法正确的是
| A.B的单质在自然界只有一种核素 |
| B.元素C、D、E的简单离子的半径依次减小 |
| C.A、E分别与C形成的化合物中含有一种相同类型的化学键 |
| D.这几种元素可能形成的简单离子中E的简单离子的还原性最强 |
您最近一年使用:0次
2017-11-10更新
|
350次组卷
|
5卷引用:天津市崇化中学2022-2023学年高二 上学期阶段性质量监测化学试卷
名校
5 . 短周期主族元素X、Y、Z、W原子序数和族序数均依次增大,其中只有Y、Z处于同一周期,Z是空气中含量最多的元素。下列说法正确的是
| A.Y—定是非金属元素 |
| B.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| C.W的最高价氧化物对应的水化物一定是强酸 |
| D.若Y、Z、W位于相邻的三个主族,Y的氢化物沸点一定低于W |
您最近一年使用:0次
2017-09-07更新
|
463次组卷
|
3卷引用:广西桂林市2021-2022学年高二上学期期末考试化学试题
13-14高三·全国·课时练习
名校
解题方法
6 . 短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13;B的化合物种类繁多,数目庞大;C、D 是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1:1的原子个数比形成的化合物的电子式:_______ ,F的原子结构示意图为_______ 。
(2)B、D形成的化合物 BD2中存在的化学键为_______ 键(填“离子”或“共价”,下同),A、C、F三种元素形成的化合物CA4F为_______ 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性,则甲、乙反应的离子方程式为_______ 。
(4)A、C、D、E的原子半径由大到小的顺序是_______ (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性_______ 于F(填“强”或“弱”),并用化学方程式证明上述结论_______ 。
(1)写出D与E以1:1的原子个数比形成的化合物的电子式:
(2)B、D形成的化合物 BD2中存在的化学键为
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性,则甲、乙反应的离子方程式为
(4)A、C、D、E的原子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次
2016-12-09更新
|
1823次组卷
|
8卷引用:云南省开远市第一中学校2021-2022学年高三下学期开学考试理综化学试题



