1 . 短周期主族元素X、Y、Z、W原子序数依次增大,其中X与Y同周期且相邻,Y与W均可形成18个电子的氢化物,且两者可反应生成一种有刺激性气味的气体,Z是地壳中含量最高的金属元素。下列说法正确的是( )
| A.原子半径:r(X)< r(Y)< r(Z)< r(W) |
| B.简单氢化物的沸点:Y>W |
| C.Y分别与Z和W形成的化合物中化学键的类型相同 |
| D.常温下Z的单质与X的最高价氧化物对应水化物的浓溶液不反应 |
您最近一年使用:0次
名校
2 . 三个相邻周期的主族元素X、Y、Z、W,原子序数依次增大,其中X、Y分别是地壳中含量最高的非金属元素和金属元素,Z原子的最外层电子数是最内层电子数的2倍,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。则下列判断正确的是
| A.原子半径: W>Y>Z>X | B.气态氢化物的稳定性:Z>X |
| C.Y、Z的氧化物都有两性 | D.最高价氧化物对应水化物的碱性:Y>W |
您最近一年使用:0次
2018-05-14更新
|
477次组卷
|
5卷引用:【全国市级联考】山东省烟台市2018届高三高考适应性练习(一)理综化学试题
3 . W、X、Y、Z是原子序数依次增大的短周期主族元素。X的单质经常作为保护气,这四种元素可以组成阴阳离子个数比是1:1的离子化合物甲,由Y、Z形成的一种化合物乙和W、Z 形成的化合物丙反应生成淡黄色固体。下列说法中不正确的是
| A.化合物甲一定能与NaOH溶液反应 |
| B.原子半径大小顺序是Z>X>Y>W |
| C.W、X组成的化合物X2W4是共价化合物 |
| D.W、X、Y组成的化合物水溶液一定呈酸性 |
您最近一年使用:0次
2017-10-31更新
|
202次组卷
|
2卷引用:广西柳州市2018届高三毕业班上学期摸底联考理综化学试题
4 . 短周期元素W、X、Y、Z的原子序数依次增加。W、X、Y简单离子的电子层结构相同,X元素在短周期主族元素中原子半径最大;W的简单氢化物常温下呈液态,Y的氧化物和氯化物熔融时都能导电,X、Y和Z原子的最外层电子数之和为10。下列说法正确的是
| A.单质沸点:W<Z |
| B.原子半径:W<Y<Z |
| C.工业上采用电解Y的氧化物冶炼单质Y |
| D.W、X、Z三种元素组成的化合物水溶液一定显碱性 |
您最近一年使用:0次
2017-10-10更新
|
239次组卷
|
2卷引用:河南省鹤壁市2018届高三毕业班调研化学试题
5 . X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。 其中只有Z是金属,W的单质是黄色晶体,X、Y、W 在周期表中的相对位置关系如图所示。 下列说法不正确的是
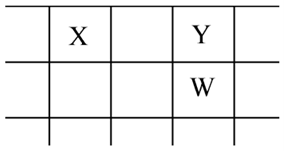

| A.5种元素中,原子半径最大的是Z |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Z与Q形成的化合物水溶液一定显酸性 |
| D.W的简单阴离子比Q的简单阴离子还原性强 |
您最近一年使用:0次
名校
解题方法
6 . 已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素,B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中含量位于金属元素的第二位。试回答下列问题:
(1)F元素价层电子排布式为___________________ 。
(2)关于B2A2的下列说法中正确的是________________ 。
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是________________ 。
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因__________ 。
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有____________ 键(填“极性键”“非极性键”),A与C组成的两种化合物M和N所含的电子数分别与X、Y相 等,N的 结构式为________ 。
(6) E的氢化物的价层电子对互斥理论模型为________ ,E 原子的杂化方式为________ 杂化。
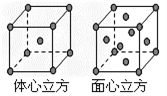
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为_________ ,F原子配位数之比为__________________ 。
(1)F元素价层电子排布式为
(2)关于B2A2的下列说法中正确的是
A.B2A2中的所有原子都满足8电子结构
B.每个B2A2分子中σ键和π键数目比为1∶1
C.B2A2是由极性键和非极性键形成的非极性分子
D.B2A2分子中的B-A键属于s—spσ键
(3) B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的空间构型是
(4) C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因
(5) A与D可以形成原子个数比分别为2∶1,1∶1的两种化合物X和Y,其中 Y含有
(6) E的氢化物的价层电子对互斥理论模型为
(7) F单质的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞的棱边长分别为acm、bcm,则F单质的面心立方晶胞和体心立方晶胞的密度之比为

您最近一年使用:0次
2017-05-18更新
|
512次组卷
|
2卷引用:黑龙江省大庆实验中学2017届高三考前得分训练(一)理科综合化学试题2
名校
7 . 现有甲、乙、丙、丁四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法不正确的是
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法不正确的是
| A.乙元素的最外层有5个电子,其氢化物含有极性键 |
| B.四种元素中丙的非金属性最强,其最高价氧化物对应的含氧酸酸性最强 |
| C.丁元素的氧化物对应的水化物与乙元素最高价氧化物对应水化物恰好完全反应形成的盐溶液显酸性 |
| D.乙、丙两元素形成的简单氢化物稳定性丙的强于乙 |
您最近一年使用:0次
2016-12-09更新
|
731次组卷
|
4卷引用:2015届甘肃省兰州市高三下学期诊断考试理综化学试卷
9-10高二下·河北·期末
名校
解题方法
8 . A、B、C三种短周期元素在元素周期表中的位置如图所示,已知A、C元素可分别与B元素形成化合物X和Y,A与B的质子数之和等于C的质子数。现有以下说法,其中判断正确的组合是
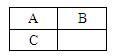 ( )
( )
①B与C均存在同素异形体
②X的种类比Y的多
③沸点:A的最简单氢化物低于C的最简单氢化物
④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
 ( )
( )①B与C均存在同素异形体
②X的种类比Y的多
③沸点:A的最简单氢化物低于C的最简单氢化物
④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
| A.①②③④ | B.②③ | C.①②④ | D.①④ |
您最近一年使用:0次
2016-12-09更新
|
1165次组卷
|
9卷引用:2011届山西省太原市高三模拟(二)(理综)化学部分
(已下线)2011届山西省太原市高三模拟(二)(理综)化学部分(已下线)2009-2010学年正定中学高二下学期期末考试化学(已下线)2012届河南省三门峡市高三上学期调研考试化学试卷(已下线)2011-2012学年河北省衡水中学高二下学期期中考试化学试卷(已下线)2013-2014山东省济宁市梁山一中3月质量检测高一化学试卷2015-2016学年江西省玉山一中高一下第一次月考化学试卷2(已下线)同步君 必修2 第1章 第2节 元素周期表和元素周期律的应用2016-2017学年辽宁省实验中学北校高一3月月考化学试卷高中化学人教版 必修2 第一章 物质结构 元素周期律 第二节 元素周期律 元素周期表和元素周期律的应用



