名校
解题方法
1 . 下列叙述中,正确的是
| A.某负离子和某正离子,其质子数和电子数都可能分别相同 |
| B.金属正离子一定具有稀有气体元素原子的电子层结构 |
| C.两种微粒的电子层结构相同,则化学性质一定相同 |
| D.两种原子的电子层结构相同,则一定属于同种元素 |
您最近一年使用:0次
2 . 科学家研究发现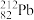 具有杀死癌细胞的功效。下列关于
具有杀死癌细胞的功效。下列关于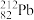 的说法正确的是
的说法正确的是
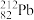 具有杀死癌细胞的功效。下列关于
具有杀死癌细胞的功效。下列关于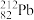 的说法正确的是
的说法正确的是A.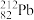 质子数是212 质子数是212 | B.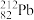 中子数是130 中子数是130 |
C.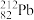 电子数是194 电子数是194 | D.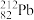 质量数是82 质量数是82 |
您最近一年使用:0次
2022-11-12更新
|
254次组卷
|
3卷引用:江苏省新海高级中学2021-2022学年高一上学期期中考试化学试题
名校
3 . 根据原子结构及元素周期律的知识,下列推断正确的是
| A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B.核外电子排布相同的微粒化学性质也相同 |
| C.热稳定性:H2O>H2S>PH3 |
D.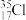 与 与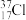 得电子能力不同 得电子能力不同 |
您最近一年使用:0次
2022-11-12更新
|
229次组卷
|
2卷引用:天津市五校2022-2023学年高三上学期期中联考化学试题
解题方法
4 . 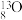 、
、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
的半衰期很短,自然界中不能稳定存在。人工合成反应如下: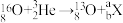 ;
;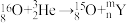 。下列说法正确的是
。下列说法正确的是
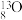 、
、 的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
的半衰期很短,自然界中不能稳定存在。人工合成反应如下: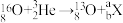 ;
; 。下列说法正确的是
。下列说法正确的是| A.X的中子数为3 |
| B.X、Y互为同位素 |
C.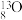 、 、 可用作示踪原子研究化学反应历程 可用作示踪原子研究化学反应历程 |
D.自然界不存在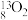 、 、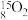 分子是因其化学键不稳定 分子是因其化学键不稳定 |
您最近一年使用:0次
2022-11-12更新
|
400次组卷
|
3卷引用:天津市五校2022-2023学年高三上学期期中联考化学试题
名校
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1L 1mol/L氯化铵溶液中 与 与 离子数之和大于 离子数之和大于 |
B.22.4L(标准状况) 所含的质子数为40 所含的质子数为40 |
C. 的 的 溶液中含有 溶液中含有 离子数目为0.1 离子数目为0.1 |
D.4.6g乙醇中含有的极性共价键数目为0.8 |
您最近一年使用:0次
名校
解题方法
6 . 已知:X、Y、Z三种元素的质子数依次增大,且均小于18。X元素的原子最外层电子数是电子层数的2倍,且X的单质为固体;Y元素的原子的最外层电子数与其K层的电子数相等;Z元素的原子次外层电子数比最外层电子数多1.下列说法正确的是
| A.0.1mol Z的单质中含3.4mol质子 | B.Y的单质不能与 反应 反应 |
| C.X元素的氧化物都是酸性氧化物 | D.化合物 属于非电解质 属于非电解质 |
您最近一年使用:0次
2022-11-10更新
|
148次组卷
|
2卷引用:河北省部分学校2022-2023学年高一上学期期中考试化学试题
7 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为_______ ,Si原子的电子式为_______ 。Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(2)如图中,“28.09”的含义是指_______ 。
(3)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。0.1mol的硅酸根离子( )中含有质子
)中含有质子_______ mol,电子_______ 个。
(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”)。
iii.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为(2)如图中,“28.09”的含义是指
| 14 Si 硅 28.09 |
 )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 )中含有质子
)中含有质子(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为
ii.流程①焦炭体现了
iii.流程④的化学反应为置换反应,写出其化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 2021年日本将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。下列有关氚的说法正确的是


| A.卡通形象中标+号的小球表示中子 |
B.氚的核素符号为 |
| C.氚和及其同位素性质完全相同 |
D.11g氚水(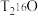 )所含中子数为6NA )所含中子数为6NA |
您最近一年使用:0次
9 . 对于1mol  和CO的混合气体,下列说法错误的是
和CO的混合气体,下列说法错误的是
 和CO的混合气体,下列说法错误的是
和CO的混合气体,下列说法错误的是| A.密度为1.25g/L | B.含有14mol质子 | C.质量为28g | D.共有NA个分子 |
您最近一年使用:0次
10 . 发现了电子的科学家是
| A.道尔顿 | B.卢瑟福 | C.汤姆孙 | D.玻尔 |
您最近一年使用:0次



