名校
解题方法
1 . 人们为了揭示原子结构的奥秘,经历了漫长的探究过程。以下是英国科学家卢瑟福进行的探究。1911 年英国科学家卢瑟福进行了著名的α粒子(即氦原子核)轰击金属箔实验。结果发现:发现绝大多数的α粒子都照直穿过薄金箔,偏转很小,但有少数α粒子发生角度比汤姆森模型所预言的大得多的偏转,大约有极少数的阿尔法粒子偏转角大于 90°,甚至观察到偏转角等于 150°的散射,称大角散射,无法用汤姆森模型说明。1911 年卢瑟福提出原子的有核模型(又称原子的核式结构模型),与正电荷联系的质量集中在中心形成原子核,电子绕着核在核外运动,由此导出α粒子散射公式,说明了 α粒子的大角散射。人类对原子结构的认识永无止境。

(1)根据上文中的表达。绝大多数α粒子是按照上图中类似_______ (填写路径编号)路径穿越金箔的;
(2)上图中所示的线条中,不可能是α粒子在该实验中的运动轨迹的是_______ (填写路径编号);
(3)正电子、负质子都属于反粒子,它们与普通的电子、质子的质量与电量均相等,而电性相反,科学家设想在宇宙的某些部分可能存在完全由反粒子构成的反物质。请你推测反氢原子的结构:
①反氢原子中含有一个带_______ 电荷的质子和一个带_______ 电荷的电子;
②反氢原子失去一个电子后所形成的离子符号_______ 。(元素符号不变)

(1)根据上文中的表达。绝大多数α粒子是按照上图中类似
(2)上图中所示的线条中,不可能是α粒子在该实验中的运动轨迹的是
(3)正电子、负质子都属于反粒子,它们与普通的电子、质子的质量与电量均相等,而电性相反,科学家设想在宇宙的某些部分可能存在完全由反粒子构成的反物质。请你推测反氢原子的结构:
①反氢原子中含有一个带
②反氢原子失去一个电子后所形成的离子符号
您最近一年使用:0次
名校
2 . 根据要求填空
(1)画出硫原子的结构示意图:_____________ 。
(2)中子数为2的氢原子:__________________________ 。
(3)写出氯化镁的电离方程式:__________________________ 。
(4)用双线桥表示出反应中电子转移的方向和数目__________________________

该反应的氧化剂是_____________ 还原剂是_____________
(5)工业利用氯气和石灰乳反应可制得漂白粉,其化学方程式为__________________________ 。
(6)碳达峰的意思是:我国承诺在2030年前 的排放量不再增长,实现碳达峰,那么
的排放量不再增长,实现碳达峰,那么 属于
属于_____________ (填字母)。
A.酸 B.碱 C.盐 D.碱性氧化物 E.酸性氧化物
(1)画出硫原子的结构示意图:
(2)中子数为2的氢原子:
(3)写出氯化镁的电离方程式:
(4)用双线桥表示出反应中电子转移的方向和数目

该反应的氧化剂是
(5)工业利用氯气和石灰乳反应可制得漂白粉,其化学方程式为
(6)碳达峰的意思是:我国承诺在2030年前
 的排放量不再增长,实现碳达峰,那么
的排放量不再增长,实现碳达峰,那么 属于
属于A.酸 B.碱 C.盐 D.碱性氧化物 E.酸性氧化物
您最近一年使用:0次
3 . 在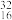 S2-中,质子数为
S2-中,质子数为____ ,中子数为____ ,电子数为____ ,该元素在元素周期表中的位置是第____ 周期____ 族,该元素的最高价氧化物对应水化物的化学式是____ 。
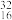 S2-中,质子数为
S2-中,质子数为
您最近一年使用:0次
名校
解题方法
4 . 联合国将2019年定为“国际化学元素周期表年”,以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索新元素、新物质提供了有效思路。
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素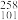 Md的质量数为
Md的质量数为( )
A. 101 B. 157 C. 258 D. 359
2. Mg和Si都属于元素周期表第3周期元素,它们原子结构中相同的是( )
A. 质子数 B. 电子层数 C. 核外电子数 D. 最外层电子数
3. 判断Cl的非金属性比S的强,可依据的事实是( )
A. HCl的热稳定性比H2S的强 B. 氯气能溶于水,硫难溶于水
C. 常温下,氯单质呈气态,硫单质呈固态 D. AgCl是白色固体,Ag2S是黑色固体
4. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是( )
A. 最高化合价为+2 B. 原子半径比钠的大
C. 单质与水的反应比钠更剧烈 D. 最高价氧化物对应的水化物碱性比钠的弱
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素
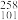 Md的质量数为
Md的质量数为A. 101 B. 157 C. 258 D. 359
2. Mg和Si都属于元素周期表第3周期元素,它们原子结构中相同的是
A. 质子数 B. 电子层数 C. 核外电子数 D. 最外层电子数
3. 判断Cl的非金属性比S的强,可依据的事实是
A. HCl的热稳定性比H2S的强 B. 氯气能溶于水,硫难溶于水
C. 常温下,氯单质呈气态,硫单质呈固态 D. AgCl是白色固体,Ag2S是黑色固体
4. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是
A. 最高化合价为+2 B. 原子半径比钠的大
C. 单质与水的反应比钠更剧烈 D. 最高价氧化物对应的水化物碱性比钠的弱
您最近一年使用:0次



