解题方法
1 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)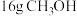 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
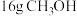 的物质的量是
的物质的量是
您最近一年使用:0次
名校
2 .  粒子是带有2个单位正电荷、质量数为4的
粒子是带有2个单位正电荷、质量数为4的 离子,由此推断
离子,由此推断 粒子含有
粒子含有___________ 个质子和___________ 中子。  粒子是
粒子是___________ (填正或负)离子。
 粒子是带有2个单位正电荷、质量数为4的
粒子是带有2个单位正电荷、质量数为4的 离子,由此推断
离子,由此推断 粒子含有
粒子含有 粒子是
粒子是
您最近一年使用:0次
3 . 物质结构决定物质性质。已知氢元素原子的核电荷数为1。试分析:
(1) 是一种离子化合物,应读作
是一种离子化合物,应读作_______ 。它与盐酸反应生成一种盐和一种可燃性气体,其化学方程式为_______ 。已知反应物中具有氧化性的物质,发生还原反应后,元素化合价降低。请判断上述反应中,反应物_______ (填化学式)具有氧化性。
(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:_______ ;也请写出氢原子与其他一种原子形成的六核(六个原子)18电子微粒的分子式:_______ 。
(1)
 是一种离子化合物,应读作
是一种离子化合物,应读作(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:
您最近一年使用:0次
名校
4 . 日本决定于2023年8月23日将福岛核电站的核污水排入大海,引起了国际上的关注和担忧。其中含有大量的放射性元素如角( ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。
(1)碘( )的质量数是
)的质量数是___________ ,中子数是___________ 。在生活中,我们也会摄入含碘( )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为___________ 。
(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
(3)碳( )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式___________ 。
(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图___________ ,___________ ,___________ 。
 ),碘(
),碘( ),碳(
),碳( )等对人体能够造成一定的危害。
)等对人体能够造成一定的危害。(1)碘(
 )的质量数是
)的质量数是 )的食品来补充人体所需的甲状腺激素,(
)的食品来补充人体所需的甲状腺激素,( )与(
)与( )互为
)互为(2)从元素周期表查得氢元素的某一数值为1.008,该数值表示___________。
| A.一种氢原子的质量数 | B.氢元素的近似相对原子质量 |
| C.三种氢原子的平均相对原子质量 | D.氢元素的相对原子质量 |
 )由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式
)由于其半衰期长达5730年,在考古发现中起到了一定的作用,请画出其电子式(4)前20号元素中,有A,B,C,D四种元素,它们的质子数依次增大,C的原子序数是另外三种元素的K层电子数之和的两倍。A的负离子和B的正离子电子层数相同,A和D的原子的最外层电子数相同,D需要得一个电子才能达到稳定结构。请依次写出A.C原子,D离子的结构示意图
您最近一年使用:0次
名校
解题方法
5 . 人们为了揭示原子结构的奥秘,经历了漫长的探究过程。以下是英国科学家卢瑟福进行的探究。1911 年英国科学家卢瑟福进行了著名的α粒子(即氦原子核)轰击金属箔实验。结果发现:发现绝大多数的α粒子都照直穿过薄金箔,偏转很小,但有少数α粒子发生角度比汤姆森模型所预言的大得多的偏转,大约有极少数的阿尔法粒子偏转角大于 90°,甚至观察到偏转角等于 150°的散射,称大角散射,无法用汤姆森模型说明。1911 年卢瑟福提出原子的有核模型(又称原子的核式结构模型),与正电荷联系的质量集中在中心形成原子核,电子绕着核在核外运动,由此导出α粒子散射公式,说明了 α粒子的大角散射。人类对原子结构的认识永无止境。

(1)根据上文中的表达。绝大多数α粒子是按照上图中类似_______ (填写路径编号)路径穿越金箔的;
(2)上图中所示的线条中,不可能是α粒子在该实验中的运动轨迹的是_______ (填写路径编号);
(3)正电子、负质子都属于反粒子,它们与普通的电子、质子的质量与电量均相等,而电性相反,科学家设想在宇宙的某些部分可能存在完全由反粒子构成的反物质。请你推测反氢原子的结构:
①反氢原子中含有一个带_______ 电荷的质子和一个带_______ 电荷的电子;
②反氢原子失去一个电子后所形成的离子符号_______ 。(元素符号不变)

(1)根据上文中的表达。绝大多数α粒子是按照上图中类似
(2)上图中所示的线条中,不可能是α粒子在该实验中的运动轨迹的是
(3)正电子、负质子都属于反粒子,它们与普通的电子、质子的质量与电量均相等,而电性相反,科学家设想在宇宙的某些部分可能存在完全由反粒子构成的反物质。请你推测反氢原子的结构:
①反氢原子中含有一个带
②反氢原子失去一个电子后所形成的离子符号
您最近一年使用:0次
6 . 原子是由什么构成的?________
您最近一年使用:0次
7 . 原子中各粒子的作用
(1)___________ 数决定元素种类,同种元素的不同___________ ,其___________ 数相同,___________ 数不同。
(2)___________ 数和___________ 数共同决定了原子(核素)的种类。
(3)元素的化学性质决定于___________ ,特别是___________ 是决定元素化学性质的主要因素。
(1)
(2)
(3)元素的化学性质决定于
您最近一年使用:0次
8 . 原子可分为___________ 和___________ 两部分,其中原子核又是由___________ 和___________ 构成的。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . NA为阿伏加德罗常数的值。下列说法正确的是___________ 。
A.1.8g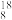 O中含有的中子数为NA
O中含有的中子数为NA
B.8gCH4含有中子数为3NA
C.2.8g56Fe含有的中子数为1.3NA
D.180g葡萄糖中,C原子的数目为6NA
E.23gNa与足量H2O反应生成的H2分子数目为NA
F.22.4L(标准状况)氟气所含的质子数为18NA
G.23gCH3CH2OH中sp3杂化的原子数为NA
H.0.5molXeF4中氙的价层电子对数为3NA
I.18gH218O含有的中子数为10NA
J.0.1mol27Al3+中含有的电子数为1.3NA
K.0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
L.18g重水(D2O)中含有的质子数为10NA
M.22.4L(标准状况)氮气中含有7NA个中子
N.1mol重水比1mol水多NA个质子
A.1.8g
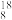 O中含有的中子数为NA
O中含有的中子数为NAB.8gCH4含有中子数为3NA
C.2.8g56Fe含有的中子数为1.3NA
D.180g葡萄糖中,C原子的数目为6NA
E.23gNa与足量H2O反应生成的H2分子数目为NA
F.22.4L(标准状况)氟气所含的质子数为18NA
G.23gCH3CH2OH中sp3杂化的原子数为NA
H.0.5molXeF4中氙的价层电子对数为3NA
I.18gH218O含有的中子数为10NA
J.0.1mol27Al3+中含有的电子数为1.3NA
K.0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
L.18g重水(D2O)中含有的质子数为10NA
M.22.4L(标准状况)氮气中含有7NA个中子
N.1mol重水比1mol水多NA个质子
您最近一年使用:0次
10 . 按要求写出下列微粒的化学符号。
(1)3个镁离子_______ 。
(2)质量数为35的氯离子_______ 。
(3)铝离子的结构示意图_______ 。
(4)硫离子的电子式_______ 。
(5)写一个含有10个电子的阳离子:_______ (化学符号)。
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:_______
(1)3个镁离子
(2)质量数为35的氯离子
(3)铝离子的结构示意图
(4)硫离子的电子式
(5)写一个含有10个电子的阳离子:
(6)写出氯酸钾的化学式,并标出其中氯元素的化合价:
您最近一年使用:0次



