名校
1 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的元素周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构。性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
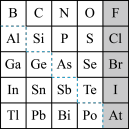
(1) 的结构示意图是
的结构示意图是___________ 。
(2)元素In在元素周期表中的位置是___________ 。
(3)P的最高价氧化物的化学式为___________ ,Al元素的最高价氧化物对应的水化物与S元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(4) 的中子数与电子数的差值是
的中子数与电子数的差值是___________ ;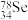 和
和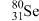 的物理性质
的物理性质___________ (填“相同”或“不同”),化学性质___________ (填“相同”或“不同”)。
(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是___________ 。
A.
B.
C.
②氢化物的还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)
 的结构示意图是
的结构示意图是(2)元素In在元素周期表中的位置是
(3)P的最高价氧化物的化学式为
(4)
 的中子数与电子数的差值是
的中子数与电子数的差值是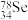 和
和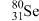 的物理性质
的物理性质(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是
A.

B.

C.

②氢化物的还原性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
2 . 请按要求填空:
(1)简单原子的原子结构如图:
①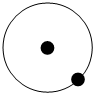 ②
② ③
③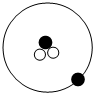
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
(2)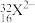 的质子数为
的质子数为___________ ,中子数为___________ ,电子数为___________ ,该元素在元素周期表中的位置是第___________ 周期___________ 族,该元素的最高价氧化物对应水化物的化学式是___________
(3)1828年,德国化学家维勒通过蒸发氰酸铵( )水溶液得到尿素[
)水溶液得到尿素[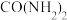 ]。
]。
①氰酸铵和尿素之间的关系是___________ (填标号)。
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为___________ 。
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为___________ 。
(1)简单原子的原子结构如图:
①
 ②
② ③
③
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
| A.①②③是三种不同的核素 | B.①②③具有相同的质量数 |
| C.①②③互为同位素 | D.①②③是三种化学性质不同的粒子 |
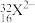 的质子数为
的质子数为(3)1828年,德国化学家维勒通过蒸发氰酸铵(
 )水溶液得到尿素[
)水溶液得到尿素[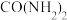 ]。
]。①氰酸铵和尿素之间的关系是
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 在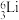 、
、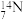 、
、 、
、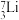 、
、 、
、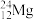 中
中
(1)互为同位素的是_______ 和_______ 。
(2)质量数相等,但不能互称同位素的是_______ 和_______ 。
(3)中子数相等,但质子数不相等的是_______ 和_______ 。
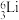 、
、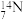 、
、 、
、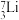 、
、 、
、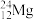 中
中(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
您最近一年使用:0次
名校
解题方法
4 . 化学计量和化学用语在化学中占有重要地位,请回答下列问题。
(1)含0.4 mol·L-1 Al3+的Al2(SO4)3溶液,取10 mL该溶液,加水稀释为100 mL溶液,稀释后的溶液中c(SO )=
)=___________ mol·L-1。
(2)标准状况下,6.72LNH3分子中所含原子数与___________ mol H2O分子中所含原子数相等。
(3)9.8 g硫酸溶解在___________ g水中,使H+与H2O个数比为1∶50(忽略水的电离)。
(4)中子数为14的铝原子,其微粒符号可表示为___________ 。
(5)质量数为35,中子数为18的原子,其原子结构示意图可表示为___________ 。
(6)已知KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。反应中氧化剂与还原剂的物质的量之比为___________ 。
(1)含0.4 mol·L-1 Al3+的Al2(SO4)3溶液,取10 mL该溶液,加水稀释为100 mL溶液,稀释后的溶液中c(SO
 )=
)=(2)标准状况下,6.72LNH3分子中所含原子数与
(3)9.8 g硫酸溶解在
(4)中子数为14的铝原子,其微粒符号可表示为
(5)质量数为35,中子数为18的原子,其原子结构示意图可表示为
(6)已知KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
2020-12-09更新
|
226次组卷
|
2卷引用:河北省唐山市迁西县职教中心2021-2022学年高二(普职融通二部)下学期4月月考化学试题
名校
解题方法
5 . 元素、原子、核素、同位素都是重要的化学基本概念,原子的构成是重要的化学基本理论。根据下列8种化学符号: H2、
H2、 H2、
H2、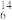 C、
C、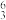 Li、
Li、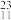 Na、
Na、 N、
N、 Li、
Li、 Mg。回答下列问题:
Mg。回答下列问题:
(1)表示核素的符号共___ 种。
(2)互为同位素的是___ 和___ 。
(3)质量数相等,但不能互称为同位素的是___ 和___ 。
(4)中子数相等,但质子数不相等的是___ 和___ 。
 H2、
H2、 H2、
H2、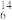 C、
C、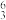 Li、
Li、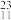 Na、
Na、 N、
N、 Li、
Li、 Mg。回答下列问题:
Mg。回答下列问题:(1)表示核素的符号共
(2)互为同位素的是
(3)质量数相等,但不能互称为同位素的是
(4)中子数相等,但质子数不相等的是
您最近一年使用:0次
2020-10-27更新
|
304次组卷
|
3卷引用:河北省辛集中学2020-2021学年高一上学期12月阶段检测化学试题
解题方法
6 . 由以下一些微粒: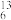 C、
C、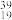 K、
K、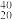 Ca、
Ca、 C、
C、 N、
N、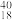 Ar。
Ar。
其中:(1)互为同位素的是___ 和___ ;
(2)质量数相等,但不能互称同位素的是___ 和___ ;
(3)中子数相等,但质子数不相等的是___ 和___ 、___ 和___ .
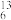 C、
C、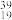 K、
K、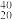 Ca、
Ca、 C、
C、 N、
N、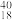 Ar。
Ar。其中:(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
您最近一年使用:0次
名校
7 . 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应: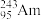 +
+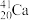 ===
===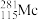 +3
+3 得到。该元素的质子数为
得到。该元素的质子数为________________ ,287Mc与288Mc互为_________________ 。
(2)Mc位于元素周期表中第VA族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式______________ ,该分子内存在的共价键类型有_________________ 。(极性键、非极性键)
(3)该族中的另一元素P能呈现多种化合价,其中氢化物的分子式为________________ ,最高价含氧酸的分子式为_________________ 。
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应:
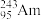 +
+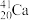 ===
===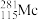 +3
+3 得到。该元素的质子数为
得到。该元素的质子数为(2)Mc位于元素周期表中第VA族,同族元素N的一种氢化物为NH2NH2,写出该化合物分子的电子式
(3)该族中的另一元素P能呈现多种化合价,其中氢化物的分子式为
您最近一年使用:0次
名校
8 . 某原子的结构示意图为: ,该原子中所含的质子数为
,该原子中所含的质子数为___ ,该原子是___ 元素的原子,该原子的核外电子数为___ 。
 ,该原子中所含的质子数为
,该原子中所含的质子数为
您最近一年使用:0次
13-14高一·全国·课时练习
名校
9 . 用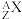 表示原子:
表示原子:
(1)中性原子的中子数:N=________ 。
(2)阳离子的中子数: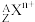 共有x个电子,则N=
共有x个电子,则N=________ 。
(3)阴离子的中子数: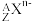 共有x个电子,则N=
共有x个电子,则N=________ 。
(4)中性分子或原子团的中子数: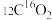 分子中,N=
分子中,N=________ 。
(5)A2-原子核内有x个中子,其质量数为m,则ng A2-所含电子的物质的量为______ 。
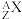 表示原子:
表示原子:(1)中性原子的中子数:N=
(2)阳离子的中子数:
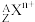 共有x个电子,则N=
共有x个电子,则N=(3)阴离子的中子数:
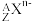 共有x个电子,则N=
共有x个电子,则N=(4)中性分子或原子团的中子数:
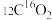 分子中,N=
分子中,N=(5)A2-原子核内有x个中子,其质量数为m,则ng A2-所含电子的物质的量为
您最近一年使用:0次
2020-02-14更新
|
155次组卷
|
8卷引用:河北省承德一中2017-2018学年高一上学期第三次月考化学试卷
河北省承德一中2017-2018学年高一上学期第三次月考化学试卷(已下线)2014学年高一化学人教版必修2 1.1.3核素练习卷安徽省铜陵一中、阜阳一中2017-2018学年高一下学期第一次联考化学试题苏教版高一化学必修2专题一第一单元第一课时《原子核外电子的排布》课时训练(夯基提能)【百强校】山东省枣庄市第八中学高中化学人教选修三课后练习1.1 原子结构 第1课时(已下线)【南昌新东方】2019-2020 南大附中 高一下 第三次月考(已下线)4.1.3 核素(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.1.3 核素-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
10 . 用 X表示原子:
X表示原子:
(1)中性原子的中子数:N=________ 。
(2)阴离子的中子数:AXn-共有x个电子,则N=________ 。
(3)中性分子中子数:12C18O2分子中,N=________ 。
(4)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为________ mol。
(5)某元素的同位素 X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置
X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置_____________________________ 。
 X表示原子:
X表示原子:(1)中性原子的中子数:N=
(2)阴离子的中子数:AXn-共有x个电子,则N=
(3)中性分子中子数:12C18O2分子中,N=
(4)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为
(5)某元素的同位素
 X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置
X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:X元素在周期表中的位置
您最近一年使用:0次
2018-06-23更新
|
127次组卷
|
2卷引用:河北省衡水市景县梁集中学2017-2018学年高一下学期期中考试化学试题



