名校
1 . 根据下列微粒回答问题: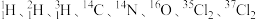 。
。
(1)以上8种微粒共有_______ 种核素,共_______ 种元素。
(2)互为同位素的是_______ 。
(3)中子数相等的是_______ 。
(4)氯有两种天然同位素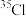 和
和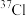 ,氯元素的近似相对原子质量为35.5,则自然界中
,氯元素的近似相对原子质量为35.5,则自然界中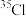 的原子百分比为
的原子百分比为_______ 。
(5)标况下2.24L14C18O分子中,中子数为_______ 。
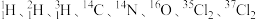 。
。(1)以上8种微粒共有
(2)互为同位素的是
(3)中子数相等的是
(4)氯有两种天然同位素
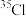 和
和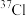 ,氯元素的近似相对原子质量为35.5,则自然界中
,氯元素的近似相对原子质量为35.5,则自然界中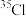 的原子百分比为
的原子百分比为(5)标况下2.24L14C18O分子中,中子数为
您最近一年使用:0次
名校
2 . 有下列粒子: 、
、 、
、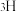 、
、 、
、 、
、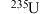 、
、 、
、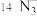 、
、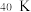 、
、 、
、 、
、 、
、 ,请回答下列问题:
,请回答下列问题:
(1)其中,含有_______ 种元素,属于氢元素的核素有_______ 种。
(2)氢的同位素 、
、 、
、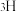 与氧的同位素
与氧的同位素 、
、 、
、 相互结合为水,可得水分子的种数为
相互结合为水,可得水分子的种数为_______ ,可得_______ 种不同的相对分子质量。
(3)0.1mol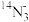 中共含
中共含_______ mol中子,含_______ 个电子。
(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的 为标准,则
为标准,则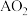 的相对分子质量为
的相对分子质量为_______ 。
 、
、 、
、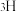 、
、 、
、 、
、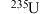 、
、 、
、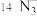 、
、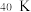 、
、 、
、 、
、 、
、 ,请回答下列问题:
,请回答下列问题:(1)其中,含有
(2)氢的同位素
 、
、 、
、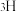 与氧的同位素
与氧的同位素 、
、 、
、 相互结合为水,可得水分子的种数为
相互结合为水,可得水分子的种数为(3)0.1mol
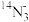 中共含
中共含(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的
 为标准,则
为标准,则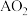 的相对分子质量为
的相对分子质量为
您最近一年使用:0次
2022-05-06更新
|
194次组卷
|
2卷引用:四川省内江市第六中学2021-2022学年高一下学期第一次月考化学试卷
名校
3 . 自然界中的铀和钴都有同位素。铀主要以三种同位素的形式存在,三种同位素的原子百分含量分别为 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式___________ 。(不必算出具体数值)。
 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式
您最近一年使用:0次
名校
解题方法
4 . (1)第ⅢB族有___________ 种元素;
(2)第5周期第ⅤA族元素的元素名称为___________ ,原子序数为___________ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为___________ ;
(4) 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为___________ ,元素X的近似相对原子质量为___________ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
(4)
 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为
您最近一年使用:0次
名校
解题方法
5 . 第ⅣA族元素R,在它的化合物R(OH)n中,其质量分数为0.778,在它的另一种化合物R(OH)m中,其质量分数为0.636.
(1)试求n和m的值:n=______ ,m=______ 。
(2)试求R的相对原子质量Ar=______ 。
(1)试求n和m的值:n=
(2)试求R的相对原子质量Ar=
您最近一年使用:0次
2024-01-12更新
|
68次组卷
|
2卷引用:海南省海口市长流中学2023-2024学年高一上学期第3次月考化学试题A卷
解题方法
6 . 某废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。
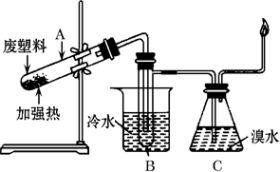
加热聚丙烯废塑料得到的产物如下表:
(1)试管A 中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A 中残留物 电石
电石 乙炔
乙炔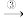 聚乙炔
聚乙炔
写出反应③的化学方程式______
(2)试管B 收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,其一氯代物有___________ 种。
(3)经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为___________ 。

加热聚丙烯废塑料得到的产物如下表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A 中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A 中残留物
 电石
电石 乙炔
乙炔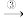 聚乙炔
聚乙炔写出反应③的化学方程式
(2)试管B 收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,其一氯代物有
(3)经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为
您最近一年使用:0次
7 . Ⅰ.现有下列基本粒子:1H、2H、3H、1H+、230Th、232Th、24Na、24Mg、O2、O3、14N、14C,请回答下列问题:
(1)这些粒子分属________ 种元素,有________ 种不同的核素。互为同素异形体的粒子为__________ 。
(2)质量数相等的粒子为____________________________ (可写多组)。
(3)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为__________ ;可得相对分子质量不同的二氧化碳分子种数为______ 。
Ⅱ.现有下列10中物质:①CaCl2 ②NH4Cl ③K2O2 ④Ba(OH)2 ⑤N2 ⑥HBr ⑦AlCl3⑧MgO⑨HNO3⑩CH4。试用以上编号填空:
(1)只有非极性键的是___________________ 。
(2)既有离子键又有极性键的是____________________ 。
(3)属于共价化合物的是__________________ 。
(1)这些粒子分属
(2)质量数相等的粒子为
(3)碳的同位素12C、13C、14C与氧的同位素16O、17O、18O可化合生成二氧化碳,可得二氧化碳分子的种数为
Ⅱ.现有下列10中物质:①CaCl2 ②NH4Cl ③K2O2 ④Ba(OH)2 ⑤N2 ⑥HBr ⑦AlCl3⑧MgO⑨HNO3⑩CH4。试用以上编号填空:
(1)只有非极性键的是
(2)既有离子键又有极性键的是
(3)属于共价化合物的是
您最近一年使用:0次
名校
解题方法
8 . 现有下列基本粒子:1H、2H、3H、1H+、234U、235U、238U、14N3-、40K、40Ca、Cl2、14N、14C,请回答下列问题:
(1)其中,含有__ 种元素,属于氢元素的核素有__ 种,属于铀元素的核素有__ 种,互为同位素的原子分别是__ ,__ 。
(2)质量数相等的粒子为__ ,__ ,__ (可不填满,也可补充)。
(3)氢元素的同位素1H、2H、3H与氧元素的同位素16O、17O、18O相互结合为水,可得水分子的种数为__ ,可得__ 种不同的相对分子质量。
(4)0.1mol14N3-中共含__ mol中子,含__ 个电子。
(1)其中,含有
(2)质量数相等的粒子为
(3)氢元素的同位素1H、2H、3H与氧元素的同位素16O、17O、18O相互结合为水,可得水分子的种数为
(4)0.1mol14N3-中共含
您最近一年使用:0次
名校
9 . (1)第ⅢB族有_____ 种元素,第117号元素属于_________ 元素(填“金属”或“非金属”);
(2)第5周期第ⅤA族元素的元素名称为_________ ,原子序数为_______ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为_______ ;
(4)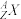 和
和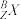 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则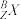 的相对原子质量为
的相对原子质量为___________ ,元素X的近似相对原子质量为______________________ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
(4)
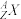 和
和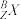 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则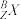 的相对原子质量为
的相对原子质量为
您最近一年使用:0次
名校
10 . 根据下列微粒回答问题: ;
; 、
、 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。
(1) 以上8种微粒共有____ 种核素,共____ 种元素;
(2) 互为同位素的是____ ;
(3) 中子数相等的是____ ;
(4) Cl2分子的结构式是____
(5) 氯有两种天然同位素35C1和37Cl,氯元素的近似相刑原子质量为35 .5,则自然界中35Cl的原子百分比为_____________________ 。
 ;
; 、
、 、14C、14N、16O、35Cl2、37Cl2。
、14C、14N、16O、35Cl2、37Cl2。(1) 以上8种微粒共有
(2) 互为同位素的是
(3) 中子数相等的是
(4) Cl2分子的结构式是
(5) 氯有两种天然同位素35C1和37Cl,氯元素的近似相刑原子质量为35 .5,则自然界中35Cl的原子百分比为
您最近一年使用:0次



