名校
1 . 2022年诺贝尔化学奖授予了三位在“点击化学”及其应用方面做出了重大贡献的三位化学家——卡罗琳贝尔托西、莫滕桦尔达和巴里·夏普莱斯。
I.卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。
(1)在很多研究糖类的实验中,会选用具有放射性的 进行示踪研究。以下有关同位素的说法正确的是
进行示踪研究。以下有关同位素的说法正确的是_______ 。(填写编号)
①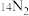 、
、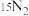 互为同位素
互为同位素
②D、T发生核聚变成为其它元素,属于化学反应
③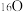 、
、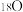 的质子数相同,电子数不同
的质子数相同,电子数不同
④ 粒子的核组成符号为
粒子的核组成符号为
⑤同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
(2)除 (丰度为
(丰度为 )外,自然界中还有两种碳的稳定核素
)外,自然界中还有两种碳的稳定核素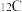 和
和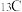 ,已知碳元素的近似相对原子质量为12.0111,则
,已知碳元素的近似相对原子质量为12.0111,则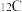 的丰度约为
的丰度约为_______ %。(填入的数字保留2位小数)
II.卡罗琳·贝尔托西在小鼠脾细胞上引入叠氮基团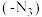 ,一段时间后注射荧光标记物
,一段时间后注射荧光标记物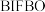 ,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。
,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。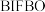 的结构如图所示,分子式为
的结构如图所示,分子式为 。
。

(3)一个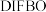 分子含有的电子数为
分子含有的电子数为_______ 个,其摩尔质量为_______ 。
(4)某次实验使用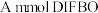 进行标记(
进行标记( ),若
),若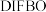 与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有
与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有_______  能被标记出。(用含A的代数式表示)
能被标记出。(用含A的代数式表示)
I.卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。
(1)在很多研究糖类的实验中,会选用具有放射性的
 进行示踪研究。以下有关同位素的说法正确的是
进行示踪研究。以下有关同位素的说法正确的是①
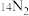 、
、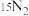 互为同位素
互为同位素 ②D、T发生核聚变成为其它元素,属于化学反应
③
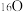 、
、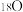 的质子数相同,电子数不同
的质子数相同,电子数不同 ④
 粒子的核组成符号为
粒子的核组成符号为
⑤同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
(2)除
 (丰度为
(丰度为 )外,自然界中还有两种碳的稳定核素
)外,自然界中还有两种碳的稳定核素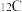 和
和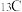 ,已知碳元素的近似相对原子质量为12.0111,则
,已知碳元素的近似相对原子质量为12.0111,则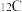 的丰度约为
的丰度约为II.卡罗琳·贝尔托西在小鼠脾细胞上引入叠氮基团
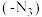 ,一段时间后注射荧光标记物
,一段时间后注射荧光标记物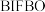 ,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。
,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。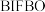 的结构如图所示,分子式为
的结构如图所示,分子式为 。
。
(3)一个
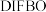 分子含有的电子数为
分子含有的电子数为(4)某次实验使用
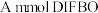 进行标记(
进行标记( ),若
),若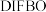 与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有
与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有 能被标记出。(用含A的代数式表示)
能被标记出。(用含A的代数式表示)
您最近一年使用:0次
名校
2 . 氯元素有两种核素 Cl、
Cl、 Cl。
Cl。
(1)关于 Cl原子说法正确的是
Cl原子说法正确的是_______ 。
(2) Cl、
Cl、 Cl具有
Cl具有_______ 。
(3) Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:_______ 决定元素种类,_______ 决定核素种类。
(4) Cl、
Cl、 Cl互为何种关系
Cl互为何种关系_______ ?
(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:_______ 、_______ 、_______ 。
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→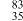 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是_______ 。
(7)已知:氯元素的近似相对原子质量为35.5。STP下,11.2LHCl气体中含H35Cl_______ mol。
 Cl、
Cl、 Cl。
Cl。(1)关于
 Cl原子说法正确的是
Cl原子说法正确的是| A.中子数等于质子数 | B.质子数等于电子数 |
| C.质子数等于质量数 | D.电子数等于中子数 |
 Cl、
Cl、 Cl具有
Cl具有| A.相同质量数 | B.不同质子数 | C.相同中子数 | D.相同电子数 |
 Cl、
Cl、 Cl都属于氯元素,由此可知:
Cl都属于氯元素,由此可知:(4)
 Cl、
Cl、 Cl互为何种关系
Cl互为何种关系(5)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:
(6)Br、Cl都属于卤族元素。某教材中有下面一段话:
For many years chemists were unsuccessfully tried to prepare the perbromateion,BrO
 。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing:
。The first successful synthesis of perbromate involved an isoelectronic species as thestarting material。The process is described asfollowing: SeO
SeO →
→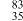 BrO
BrO +e-。以下说法正确的是
+e-。以下说法正确的是| A.该过程发生了化学变化 | B.Br元素的质量数为83 |
C. SeO SeO 中含有68个电子 中含有68个电子 | D. Se与 Se与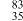 Br互为同位素 Br互为同位素 |
您最近一年使用:0次
名校
3 . 根据下列微粒回答问题: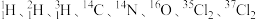 。
。
(1)以上8种微粒共有_______ 种核素,共_______ 种元素。
(2)互为同位素的是_______ 。
(3)中子数相等的是_______ 。
(4)氯有两种天然同位素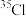 和
和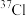 ,氯元素的近似相对原子质量为35.5,则自然界中
,氯元素的近似相对原子质量为35.5,则自然界中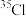 的原子百分比为
的原子百分比为_______ 。
(5)标况下2.24L14C18O分子中,中子数为_______ 。
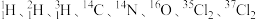 。
。(1)以上8种微粒共有
(2)互为同位素的是
(3)中子数相等的是
(4)氯有两种天然同位素
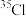 和
和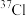 ,氯元素的近似相对原子质量为35.5,则自然界中
,氯元素的近似相对原子质量为35.5,则自然界中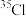 的原子百分比为
的原子百分比为(5)标况下2.24L14C18O分子中,中子数为
您最近一年使用:0次
名校
4 . 有下列粒子: 、
、 、
、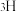 、
、 、
、 、
、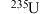 、
、 、
、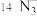 、
、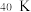 、
、 、
、 、
、 、
、 ,请回答下列问题:
,请回答下列问题:
(1)其中,含有_______ 种元素,属于氢元素的核素有_______ 种。
(2)氢的同位素 、
、 、
、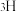 与氧的同位素
与氧的同位素 、
、 、
、 相互结合为水,可得水分子的种数为
相互结合为水,可得水分子的种数为_______ ,可得_______ 种不同的相对分子质量。
(3)0.1mol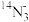 中共含
中共含_______ mol中子,含_______ 个电子。
(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的 为标准,则
为标准,则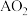 的相对分子质量为
的相对分子质量为_______ 。
 、
、 、
、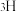 、
、 、
、 、
、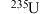 、
、 、
、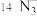 、
、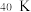 、
、 、
、 、
、 、
、 ,请回答下列问题:
,请回答下列问题:(1)其中,含有
(2)氢的同位素
 、
、 、
、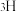 与氧的同位素
与氧的同位素 、
、 、
、 相互结合为水,可得水分子的种数为
相互结合为水,可得水分子的种数为(3)0.1mol
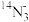 中共含
中共含(4)一个A原子的质量为a克,一个氧原子的质量为b克,现以氧原子质量的
 为标准,则
为标准,则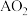 的相对分子质量为
的相对分子质量为
您最近一年使用:0次
2022-05-06更新
|
194次组卷
|
2卷引用:四川省内江市第六中学2021-2022学年高一下学期第一次月考化学试卷
名校
5 . 某文献资料上记载的相对原子质量数据摘录如表所示:
(1)则65Cu的相对原子质量=____ (保留三位小数)。
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:____ ;B:____ ;C:____ 。
(3)溶液处于____ 点时的导电性最弱,写出该处发生的化学反应的离子方程式:____ 。
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。
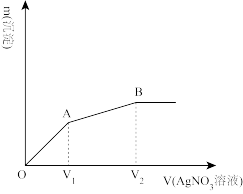
(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:____ 。
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:____ 。
(6)原溶液中c(I-):c(Cl-)的比值为:____ (用V1、V2表示)。
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
| 63Cu | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
| 65Cu | 65 | 30.85% |
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:
(3)溶液处于
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。

(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:
(6)原溶液中c(I-):c(Cl-)的比值为:
您最近一年使用:0次
6 . 某元素X构成的气态单质分子(双原子分子)有三种,其相对分子质量分别为70、72、74,标背状况下,V升该气体中此三种分子的物质的量之比为9∶6∶1.完成下列问题:
(1)X元素有_______ 种核素。
(2)各种核素的质量数分别为_______ 。
(3)X2的平均相对分子质量为_______ 。
(4)质量数较小的X原子的物质的量分数为_______ 。
(1)X元素有
(2)各种核素的质量数分别为
(3)X2的平均相对分子质量为
(4)质量数较小的X原子的物质的量分数为
您最近一年使用:0次
名校
解题方法
7 . 按要求填空
(1)写出溴原子的核外电子排布式_______
(2)写出氮原子的轨道表示式_________
(3)请解释Fe3+比Fe2+稳定的原因________
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为_______
(1)写出溴原子的核外电子排布式
(2)写出氮原子的轨道表示式
(3)请解释Fe3+比Fe2+稳定的原因
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为
您最近一年使用:0次
名校
解题方法
8 . 按要求填空
(1) 中有
中有_______  质子,
质子,_______  中子,
中子,_______ 个电子。
(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为_______ 。
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是_______ ;同质量的氨气和硫化氢气体的体积比是_______ ;若两者所含氢原子个数相同,它们的物质的量之比为_______ 。
(4)某混合气体中,各气体的体积分数为: 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为_______ ,其对于氢气的密度为_______ 。
(5)在 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_______  。
。
(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
则 的相对原子质量=
的相对原子质量=_______ (保留三位小数)。
(7)在 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是_______ ;只存在共价键的是_______ ;既存在离子键又存在共价键的是_______ ;不存在化学键的是_______ 。
(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是_______ ;仅发生离子键破坏的是_______ ;仅发生共价键破坏的是_______ ;既发生离子键又发生共价键破坏的是_______ 。
(1)
 中有
中有 质子,
质子, 中子,
中子,(2)同温同压下,两种气体A和B的体积比为2∶1,质量比为8∶5,摩尔质量之比为
(3)同温同压下,同体积的氨气和硫化氢气体的质量比是
(4)某混合气体中,各气体的体积分数为:
 、
、 、
、 、
、 ,则此混合气体的平均相对分子质量为
,则此混合气体的平均相对分子质量为(5)在
 、
、 下,有
下,有 和
和 混合气体共
混合气体共 ,经点燃后恢复到原状态时,混合气体的体积减少为
,经点燃后恢复到原状态时,混合气体的体积减少为 ,则原混合气体中
,则原混合气体中 的体积为
的体积为 。
。(6)将某文献资料上记载的相对原子质量数据摘录如表所示:
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
 | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
 | _______ | 65 | 30.85% |
则
 的相对原子质量=
的相对原子质量=(7)在
 、
、 、
、 、
、 、
、 等物质中,只存在离子键的是
等物质中,只存在离子键的是(8)下列变化中:①碘的升华;②烧碱熔化;③氯化钠溶于水;④氧气溶于水;⑤氯化氢溶于水;⑥氯化铵受热分解为氯化氢和氨气。(填序号)。化学键没有被破坏的是
您最近一年使用:0次
名校
9 . 自然界中的铀和钴都有同位素。铀主要以三种同位素的形式存在,三种同位素的原子百分含量分别为 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式___________ 。(不必算出具体数值)。
 U 0.005%、
U 0.005%、 U 0.72%、
U 0.72%、 U 99.275%。请写出计算U元素近似相对原子质量的计算式
U 99.275%。请写出计算U元素近似相对原子质量的计算式
您最近一年使用:0次
名校
解题方法
10 . (1)第ⅢB族有___________ 种元素;
(2)第5周期第ⅤA族元素的元素名称为___________ ,原子序数为___________ ;
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为___________ ;
(4) 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为___________ ,元素X的近似相对原子质量为___________ 。
(2)第5周期第ⅤA族元素的元素名称为
(3)第4周期元素硒的某一核素含有46个中子,该元素的原子符号为
(4)
 和
和 是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则
是元素X的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为W g,则 的相对原子质量为
的相对原子质量为
您最近一年使用:0次



