名校
解题方法
1 . 第ⅣA族元素R,在它的化合物R(OH)n中,其质量分数为0.778,在它的另一种化合物R(OH)m中,其质量分数为0.636.
(1)试求n和m的值:n=______ ,m=______ 。
(2)试求R的相对原子质量Ar=______ 。
(1)试求n和m的值:n=
(2)试求R的相对原子质量Ar=
您最近一年使用:0次
2024-01-12更新
|
68次组卷
|
2卷引用:海南省海口市长流中学2023-2024学年高一上学期第3次月考化学试题A卷
名校
2 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
名校
解题方法
3 . 读表,回答问题:
 和
和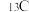 互为
互为______ 关系,请列出碳元素近似相对原子质量的计算表达式______ 。
| 核素 | 相对原子质量 | 丰度(原子分数) |
 | 12(整数,相对原子质量的基准) | 0.9893 |
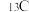 | 13.003354826 | 0.0107 |
 和
和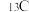 互为
互为
您最近一年使用:0次
名校
解题方法
4 . 原子是化学反应中不可再分的基本微粒,自古以来人们对于原子的研究从未停止过。了解了原子的结构,能够帮助人们更好地从微观角度认识物质并推断它们的性质。
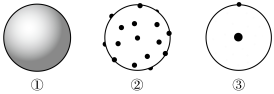
(1)下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆孙的观点的是___________。
(2)一种元素有质量数分别为35,37的两种核素,该元素的近似相对原子质量为35.5,则两种核素的丰度之比为___________ 。
(3)下列微粒中,具有相同的电子层数与最外层电子数的是___________。
(1)下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆孙的观点的是___________。

| A.①②③ | B.③①② | C.③②① | D.②①③ |
(2)一种元素有质量数分别为35,37的两种核素,该元素的近似相对原子质量为35.5,则两种核素的丰度之比为
(3)下列微粒中,具有相同的电子层数与最外层电子数的是___________。
| A.He与Li | B. 与 与 | C. 与 与 | D. 与Ar 与Ar |
您最近一年使用:0次
名校
5 . 根据2023年最新数据,中国钢铁产量占全球总产量的53.9%,铁及其化合物在人类生活中有着极其重要的作用。完成下列填空:
(1)铁的原子结构示意图为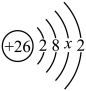 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是___________ ,铁原子核外 轨道上共填充了
轨道上共填充了___________ 个电子。
(2)铁原子中有___________ 种能量不同的电子,铁原子次外层的电子云有_种不同的伸展方向。
(3)自然界一共存在四种稳定的铁原子,分别是 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为___________ 。计算铁元素的近似相对质量的计算式为: ,其中
,其中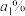 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的___________ 。
(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
(5) 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是___________ (用离子方程式表示)。
(6)向新配制的 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:
___ +___
+___ +____
+____ =____
=____ +____
+____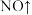 +____
+____
①配平上述反应__________ 。
②每生成0.5moI 气体,转移的电子数为
气体,转移的电子数为___________ 。
③要检验该反应后的溶液中是否还含有 ,实验方案是
,实验方案是___________ 。
(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式___________ 。
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:___________ 。
(1)铁的原子结构示意图为
 。由此可知,铁在周期表中的位置是
。由此可知,铁在周期表中的位置是 轨道上共填充了
轨道上共填充了(2)铁原子中有
(3)自然界一共存在四种稳定的铁原子,分别是
 、
、 、
、 和
和 ,其中
,其中 原子中子数与质子数之差为
原子中子数与质子数之差为 ,其中
,其中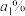 、
、 ∙∙∙∙∙∙是指各同位素的
∙∙∙∙∙∙是指各同位素的(4)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是___________(选填编号)。
A. | B. | C. | D. |
(5)
 可以用来净水、治疗缺铁性贫血等,实验室在配制
可以用来净水、治疗缺铁性贫血等,实验室在配制 溶液时,为了防止
溶液时,为了防止 变质,经常向溶液中加入铁粉,其原因是
变质,经常向溶液中加入铁粉,其原因是(6)向新配制的
 溶液中,加入一定量的稀硝酸,发生如下反应:
溶液中,加入一定量的稀硝酸,发生如下反应:___
 +___
+___ +____
+____ =____
=____ +____
+____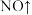 +____
+____
①配平上述反应
②每生成0.5moI
 气体,转移的电子数为
气体,转移的电子数为③要检验该反应后的溶液中是否还含有
 ,实验方案是
,实验方案是(7)现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:

①写出反应III的平衡常数表达式
②写出铁氧化物循环裂解水制氢的总反应的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 观察下列表格,回答相关问题:
(1)其中属于离子化合物的物质有___________ 。
(2)试比较F-、Cl-、Br-的离子半径大小___________ (用元素符号表示);推测离子半径与离子晶体熔点的关系___________ ;猜想KCl的熔点___________ (高于/低于)NaCl的熔点。
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为___________ g(保留2位小数)。
| 物质 | NaF | NaCl | NaBr | KCl | AlCl3 | CH4 | CCl4 |
| 熔点/℃ | 995 | 801 | 755 | 190 | -182.5 | -23 |
(2)试比较F-、Cl-、Br-的离子半径大小
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为
您最近一年使用:0次
名校
解题方法
7 . 自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。
(1)Si原子的结构示意图为_______ 。
(2)28Si是硅的一种同位素,其原子核内质子数为________ ,Si原子的电子式为_______ ,Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素_______ 。
(1)Si原子的结构示意图为
(2)28Si是硅的一种同位素,其原子核内质子数为
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素
您最近一年使用:0次
名校
8 . 安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:


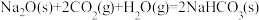
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素的名称是_______ ,原子结构示意图为_______ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为_______ ,能量最高的电子为_______ 层上的电子。
(2)已知天然氢元素中:气,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%,写出氢元素的相对原子质量计算表达式_______ ;(氕、氘、氚原子的质量用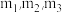 表示,
表示,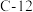 原子质量用
原子质量用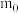 表示);
表示);
(3)碳也有一种放射性核素 ,举出一种该核素的应用
,举出一种该核素的应用_______ ;
(4)汽车行驶过程中,能保护司机不受伤害的气囊需要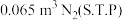 ,其中约含有
,其中约含有_______ 个氮原子(保留三个有效数字);已知获得上述 需要
需要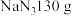 ,反应生成
,反应生成 的产率是
的产率是_______  (
( )
)


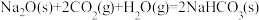
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素的名称是
(2)已知天然氢元素中:气,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%,写出氢元素的相对原子质量计算表达式
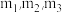 表示,
表示,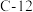 原子质量用
原子质量用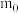 表示);
表示);(3)碳也有一种放射性核素
 ,举出一种该核素的应用
,举出一种该核素的应用(4)汽车行驶过程中,能保护司机不受伤害的气囊需要
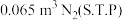 ,其中约含有
,其中约含有 需要
需要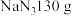 ,反应生成
,反应生成 的产率是
的产率是 (
( )
)
您最近一年使用:0次
名校
9 . 2022年诺贝尔化学奖授予了三位在“点击化学”及其应用方面做出了重大贡献的三位化学家——卡罗琳贝尔托西、莫滕桦尔达和巴里·夏普莱斯。
I.卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。
(1)在很多研究糖类的实验中,会选用具有放射性的 进行示踪研究。以下有关同位素的说法正确的是
进行示踪研究。以下有关同位素的说法正确的是_______ 。(填写编号)
①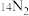 、
、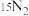 互为同位素
互为同位素
②D、T发生核聚变成为其它元素,属于化学反应
③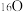 、
、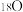 的质子数相同,电子数不同
的质子数相同,电子数不同
④ 粒子的核组成符号为
粒子的核组成符号为
⑤同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
(2)除 (丰度为
(丰度为 )外,自然界中还有两种碳的稳定核素
)外,自然界中还有两种碳的稳定核素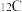 和
和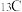 ,已知碳元素的近似相对原子质量为12.0111,则
,已知碳元素的近似相对原子质量为12.0111,则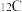 的丰度约为
的丰度约为_______ %。(填入的数字保留2位小数)
II.卡罗琳·贝尔托西在小鼠脾细胞上引入叠氮基团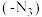 ,一段时间后注射荧光标记物
,一段时间后注射荧光标记物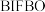 ,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。
,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。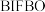 的结构如图所示,分子式为
的结构如图所示,分子式为 。
。

(3)一个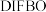 分子含有的电子数为
分子含有的电子数为_______ 个,其摩尔质量为_______ 。
(4)某次实验使用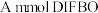 进行标记(
进行标记( ),若
),若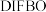 与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有
与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有_______  能被标记出。(用含A的代数式表示)
能被标记出。(用含A的代数式表示)
I.卡罗琳·贝尔托西将“点击化学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。
(1)在很多研究糖类的实验中,会选用具有放射性的
 进行示踪研究。以下有关同位素的说法正确的是
进行示踪研究。以下有关同位素的说法正确的是①
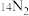 、
、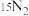 互为同位素
互为同位素 ②D、T发生核聚变成为其它元素,属于化学反应
③
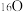 、
、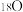 的质子数相同,电子数不同
的质子数相同,电子数不同 ④
 粒子的核组成符号为
粒子的核组成符号为
⑤同一元素各核素的近似相对原子质量不同,但它们的化学性质几乎完全相同
(2)除
 (丰度为
(丰度为 )外,自然界中还有两种碳的稳定核素
)外,自然界中还有两种碳的稳定核素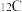 和
和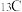 ,已知碳元素的近似相对原子质量为12.0111,则
,已知碳元素的近似相对原子质量为12.0111,则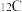 的丰度约为
的丰度约为II.卡罗琳·贝尔托西在小鼠脾细胞上引入叠氮基团
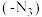 ,一段时间后注射荧光标记物
,一段时间后注射荧光标记物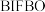 ,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。
,两者1∶1发生“点击化学”反应,以此标记引入了叠氮基团的细胞分布情况。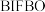 的结构如图所示,分子式为
的结构如图所示,分子式为 。
。
(3)一个
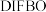 分子含有的电子数为
分子含有的电子数为(4)某次实验使用
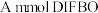 进行标记(
进行标记( ),若
),若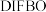 与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有
与叠氮基团的反应效率为10%,则小鼠脾细胞上引入的叠氮基团有 能被标记出。(用含A的代数式表示)
能被标记出。(用含A的代数式表示)
您最近一年使用:0次
名校
10 . 某文献资料上记载的相对原子质量数据摘录如表所示:
(1)则65Cu的相对原子质量=____ (保留三位小数)。
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:____ ;B:____ ;C:____ 。
(3)溶液处于____ 点时的导电性最弱,写出该处发生的化学反应的离子方程式:____ 。
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。
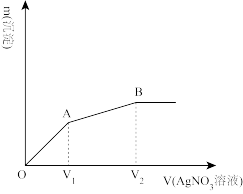
(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:____ 。
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:____ 。
(6)原溶液中c(I-):c(Cl-)的比值为:____ (用V1、V2表示)。
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
| 63Cu | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
| 65Cu | 65 | 30.85% |
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:
(3)溶液处于
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。

(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:
(6)原溶液中c(I-):c(Cl-)的比值为:
您最近一年使用:0次



