名校
1 . 下列关于含氮微粒的表述正确的是
| A.N3-离子质子数为20 |
| B.N3-离子最外层电子数为6 |
| C.N2分子和CO分子含有相同的电子数 |
| D.N原子未成对电子的电子云伸展方向相同 |
您最近一年使用:0次
2022-10-31更新
|
75次组卷
|
2卷引用:上海市格致中学2020-2021学年高一上学期期中考试化学试题
2 . 有关氮原子核外p亚层中的电子的说法错误的是
| A.能量相同 | B.电子云形状相同 |
| C.电子云伸展方向相同 | D.自旋方向相同 |
您最近一年使用:0次
2021-12-27更新
|
368次组卷
|
4卷引用:上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题
上海外国语大学附属大境中学2019-2020学年高三上学期期中考化学试题上海市嘉定区2022届高三一模化学试题(已下线)第37练 原子结构-2023年高考化学一轮复习小题多维练(全国通用)福建省漳平第二中学2021-2022学年高二下学期第一次月考化学试题
3 . 下列对化学用语的叙述正确的是
| A.碳原子最外层电子云有三种不同的伸展方向 | B.CCl4的比例模型: |
C.氮分子的结构式: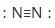 | D.溴化铵的电子式: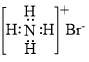 |
您最近一年使用:0次
2021-10-03更新
|
363次组卷
|
3卷引用:上海交通大学附属中学2020-2021学年高三上学期第一次月考化学试题
名校
解题方法
4 . 常温时,通过NaOH溶液或硫酸改变饱和氯水的pH,溶液中含氯微粒的物质的量分数与pH的关系如图所示。回答下列问题:
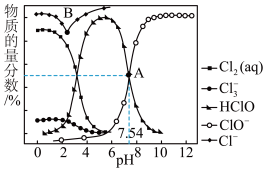
(1)Cl-的核外电子占有______ 个原子轨道, 中的化学键类型是
中的化学键类型是______ ,HClO的电子式是______ 。
(2)解释A点溶液pH=7.54的主要原因:______ 。
(3)结合图象,从平衡移动的角度解释B点向右Cl-物质的量分数增大的主要原因:
①______ ;
②______ 。
(4)估算图象中Cl-物质的量分数的上限______ 。

(1)Cl-的核外电子占有
 中的化学键类型是
中的化学键类型是(2)解释A点溶液pH=7.54的主要原因:
(3)结合图象,从平衡移动的角度解释B点向右Cl-物质的量分数增大的主要原因:
①
②
(4)估算图象中Cl-物质的量分数的上限
您最近一年使用:0次
5 . 比较结构示意图(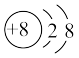 )和电子排布式(1s22s22p6),仅能由后者判断出的结论是
)和电子排布式(1s22s22p6),仅能由后者判断出的结论是
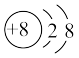 )和电子排布式(1s22s22p6),仅能由后者判断出的结论是
)和电子排布式(1s22s22p6),仅能由后者判断出的结论是| A.每个电子的自旋方向 | B.电子的能量种类 |
| C.每个电子层的电子数 | D.核电荷数 |
您最近一年使用:0次
解题方法
6 . 下列描述碳原子结构的化学用语正确的是
A.碳-12原子: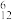 C C |
B.原子结构示意图: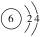 |
C.原子核外能量最高的电子云图: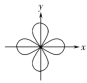 |
D.原子的轨道表示式: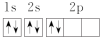 |
您最近一年使用:0次
2022-07-31更新
|
671次组卷
|
8卷引用:2015届上海市普陀区高三一模化学试卷
2015届上海市普陀区高三一模化学试卷(已下线)上海市普陀区2015届高三12月质量调研(一模)化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)(已下线)【知识图鉴】单元讲练测选择性必修2第1章01讲核心(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
7 . 氮是生命物质的重要组成元素之一,含氮物质与人类的生活密切相关。氮原子最外层电子轨道表示式为:_____________ ;N4分子的空间结构如图: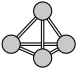 ,它是一种
,它是一种___________ 分子(填“极性”或“非极性”)。
 ,它是一种
,它是一种
您最近一年使用:0次
名校
8 . 铋(83Bi)为第V A族元素,常见化合价为+3和+5。化合物NaBiO3为黄色固体,常温下微溶于水,在空气中逐渐分解产生Bi2O3、NaOH等物质。
(1)铋元素最外层电子分布在_____ 种能级中,共有_____ 种运动状态。
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为_________ 。
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:_______ 。
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是______ 。
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
______ NaBiO3+______ MnSO4+______ H2SO4→______ Na2SO4+______ Bi2(SO4)3+______ NaMnO4+______ H2O
②若有2mol氧化剂在该反应中被还原,则生成的MnO 被还原为Mn2+时,能将
被还原为Mn2+时,能将____ mol HCl氧化成Cl2。
(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:_________ 。
(1)铋元素最外层电子分布在
(2)铋酸钠NaBiO3中属于短周期元素的离子半径大小关系为
(3)元素Na、Bi、O的金属性依次减弱,非金属性依次增强,请列举判断依据:
(4)铋酸钠NaBiO3在空气中分解所得到产物中,化学键类型是
A.金属键 B.离子键 C.极性键 D.非极性键
(5)将NaBiO3加入MnSO4和H2SO4的混合溶液里加热,发生如下反应:
[ ]NaBiO3+[ ]MnSO4+[ ]H2SO4→[ ]Na2SO4+[ ]Bi2(SO4)3+[ ]NaMnO4+[ ]H2O
①配平该化学方程式,将系数填写在对应位置上。
②若有2mol氧化剂在该反应中被还原,则生成的MnO
 被还原为Mn2+时,能将
被还原为Mn2+时,能将(6)写出NaBiO3固体溶于HCl时发生反应的离子方程式:
您最近一年使用:0次
9 . 描述硅原子核外电子运动说法错误的是
| A.有4种不同的伸展方向 |
| B.有14种不同运动状态的电子 |
| C.有5种不同能量的电子 |
| D.有5种不同的空间运动状态 |
您最近一年使用:0次
2021-10-30更新
|
653次组卷
|
8卷引用:2015届上海市十三校高三第二次联考化学试卷
2015届上海市十三校高三第二次联考化学试卷2017-2018学年上海复旦附中高三化学第一次月考测试题河北省邢台市第二中学2018-2019学年高二下学期第四次月考化学试题河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.1.2 构造原理与电子排布式-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)吉林省长春市十一高中2021-2022学年高二下学期第二学程考试化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题
解题方法
10 . 下列有关化学表达正确的是( )
A.CS2的比例模型: |
B.铍原子最外层的电子云图: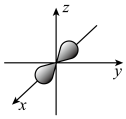 |
C.乙醇的球棍模型: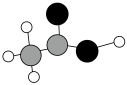 |
D.氮原子最外层轨道表示式: |
您最近一年使用:0次
2020-02-24更新
|
251次组卷
|
3卷引用:上海市八校2015届高三上学期期中联考化学试题



