解题方法
1 . W、X、Y、Z、M是原子序数依次增大的前四周期元素,其元素性质或结构如下:
回答下列问题:
(1)写出X元素的名称______ ;Y元素的元素符号______ 。
(2)写出M元素+2价离子的价层电子排布式______ 。
(3)基态Z元素原子核外电子占据的最高能层包含的原子轨道数为______ 。
(4)W、X、Z可形成强还原性物质ZXW4,W、X、Z三种元素电负性由大到小的顺序是______ (用元素符号表示)。
(5)中国的稀土储量世界第一、稀土元素是周期系ⅢB族中原子序数为21(Sc)、39(Y)和镧系元素共17种化学元素的统称。其中钪(Sc)元素有______ 种运动状态不同的电子,最高能层符号是______ ;稀土元素分组方法之一是两分法[轻稀土和重稀土]。两分法分组以Gd(钆)划界的原因是:从Gd之后在4f亚层上新增加电子的自旋方向改变了,则Gd的4f能级价层电子排布图为______ 。
元素 | 元素性质或原子结构 |
W | 电子只有一种自旋取向 |
X | 核外只有一个未成对电子,且电子有三种空间运动状态 |
Y | s轨道电子数比p轨道多一个,且第一电离能大于同周期相邻元素 |
Z | 电负性是短周期中最小的 |
M | +3价基态离子最高能级处于半满状态 |
(1)写出X元素的名称
(2)写出M元素+2价离子的价层电子排布式
(3)基态Z元素原子核外电子占据的最高能层包含的原子轨道数为
(4)W、X、Z可形成强还原性物质ZXW4,W、X、Z三种元素电负性由大到小的顺序是
(5)中国的稀土储量世界第一、稀土元素是周期系ⅢB族中原子序数为21(Sc)、39(Y)和镧系元素共17种化学元素的统称。其中钪(Sc)元素有
您最近一年使用:0次
2 . 现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。基态A元素原子的价电子排布式为 ;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能
(2)基态D元素原子的价电子排布式为
(3)基态C元素原子的电子排布图为
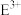 的离子符号为
的离子符号为(4)F元素位于元素周期表的
(5)G元素可能的性质是______(填字母)。
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
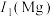
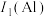 ,其原因是
,其原因是
您最近一年使用:0次
2024-03-26更新
|
74次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
3 . 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述,正确的是
| X | |||
| W | Y | R | |
| Z |
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.p能级未成对电子最多的是W元素 |
| D.X元素是电负性最大的元素 |
您最近一年使用:0次
2024-03-26更新
|
29次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
名校
解题方法
4 . 现有四种元素的基态原子的电子排布式如下:①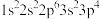 ;②
;②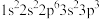 ;③
;③ ;④
;④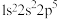 。则下列有关比较中正确的是
。则下列有关比较中正确的是
| A.第一电离能:④>③>①>② | B.原子半径:④>③>②>① |
| C.电负性:④>③>①>② | D.最高正化合价:④>①>③=② |
您最近一年使用:0次
5 . 现有四种元素基态原子的电子排布式如下。则下列有关比较中正确的是
①1s22s22p63s23p4;②ls22s22p63s23p3;③1s22s22p3;④1s22s22p5
①1s22s22p63s23p4;②ls22s22p63s23p3;③1s22s22p3;④1s22s22p5
| A.第一电离能:④>③>②>① | B.原子半径:①>②>③>④ |
| C.未成对电子数:④>③=②>① | D.电负性:④>③>②>① |
您最近一年使用:0次
2024-03-15更新
|
198次组卷
|
2卷引用:山东省潍坊市临朐县第一中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 短周期元素X、Y、Z、W原子序数依次增大。基态X原子有两个单电子,Z的简单离子在同周期离子中半径最小,基态W原子的价电子排布式为 ,且Y、W同主族。下列说法错误的是
,且Y、W同主族。下列说法错误的是
 ,且Y、W同主族。下列说法错误的是
,且Y、W同主族。下列说法错误的是| A.电负性:Y>W>X>Z | B.四种元素均位于元素周期表的p区 |
| C.简单氢化物稳定性:X<Y<W | D.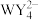 、 、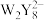 中W的化合价相同 中W的化合价相同 |
您最近一年使用:0次
2024-03-13更新
|
107次组卷
|
2卷引用:山东省青岛第一中学2023-2024学年高二上学期第二次月考化学试卷
7 . 一种新型漂白剂(结构如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,Z电子只有一种自旋取向;W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。

回答下列问题:
(1)写出元素Y在周期表中的位置是:_______ ,所属分区是:_____ 。
(2)写出元素X简单离子的核外电子排布式:________ 。
(3)元素X基态原子核外电子的运动状态有_____ 种,占据的原子轨道有____ 个。
(4)W、X、Y电负性由大到小的顺序是_______ (用元素符号表示)。
(5)试解释W的第一电离能大于 的第一电离能的原因:
的第一电离能的原因:___________ 。

回答下列问题:
(1)写出元素Y在周期表中的位置是:
(2)写出元素X简单离子的核外电子排布式:
(3)元素X基态原子核外电子的运动状态有
(4)W、X、Y电负性由大到小的顺序是
(5)试解释W的第一电离能大于
 的第一电离能的原因:
的第一电离能的原因:
您最近一年使用:0次
8 . 我国自主设计生产的长征系列运载火箭使用偏二甲肼( )作燃料,(
)作燃料,( )作氧化剂。下列相关说法正确的是
)作氧化剂。下列相关说法正确的是
 )作燃料,(
)作燃料,( )作氧化剂。下列相关说法正确的是
)作氧化剂。下列相关说法正确的是| A.N、O、C的电负性依次减小 |
B.基态N原子的轨道表示式为 |
| C.O原子有5种空间运动状态不同的电子 |
| D.C、N、O三种基态原子的第一电离能依次增大 |
您最近一年使用:0次
9 . 我国科学家近年来发现的一种重要的铁系超导材料Fe-Sm-As-F-O是由多种元素组成的化合物,下列说法正确的是
A. 的价层电子排布式为 的价层电子排布式为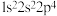 |
B.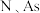 同主族,第一电离能 同主族,第一电离能 |
C.电负性 |
D. 的价层电子轨道表示式 的价层电子轨道表示式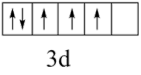 违背了泡利不相容原理 违背了泡利不相容原理 |
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z、W、R为原子序数依次增大的前四周期元素。基态X原子的价电子排布式为nsnnpn+1;Y的+2价阳离子核外电子排布与氖原子相同;Z元素的第一至第四电离能分别是:I1=578kJ∙mol-1、I2=1817kJ∙mol-1、I3=2745kJ∙mol-1、I4=11575kJ∙mol-1;W的最高正价与最低负价的代数和为6:基态R2+的M层有5个未成对电子。
回答下列问题:
(1)R元素在元素周期表中的位置为___________ ,原子序数比R少1的元素原子基态核外排布式为:___________ 。
(2)元素的气态原子得到一个电子所放出的能量称为第一电子亲合能。气态原子结合电子越容易,电子亲合能越大。X和W的第一电子亲合能X___________ W(填“>”或“<”),利用原子结构知识解释原因___________ 。
(3)X、Z、W的简单离子半径由大到小的顺序是___________ (填离子符号)。
(4)Z单质与NaOH反应的离子反应方程式为___________ 。
回答下列问题:
(1)R元素在元素周期表中的位置为
(2)元素的气态原子得到一个电子所放出的能量称为第一电子亲合能。气态原子结合电子越容易,电子亲合能越大。X和W的第一电子亲合能X
(3)X、Z、W的简单离子半径由大到小的顺序是
(4)Z单质与NaOH反应的离子反应方程式为
您最近一年使用:0次



