1 . 2017年Chem.Mater报导了某金属锂的硼氢化物不仅具有通常的高储氮密度,还有一些其它应用的性质。该化合物属立方晶系,晶胞参数为a=959.3pm,其晶胞图如下(提示:有一个Li+掩在晶胞上部阴离子中):

(1)试写出该金属硼化物的化学式(最简单正整数比)_______ 和阴离子化学式_______ 。
(2)试计算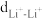 与Li+到(BxHy)n-多面体中心的距离
与Li+到(BxHy)n-多面体中心的距离_______ ,并计算晶体的密度_______ 。
(3)如果把Li+作为晶胞的原点,试写出新晶胞中Li+到(BxHy)n-的坐标_______ 。
(4)若把晶体的结构基元围成一个平行六面体,写出该平行六面体中Li+到(BxHy)n-的原子坐标_______ 。
(5)从晶体结构分析,该晶体可能作为何种功能材料?给出理由_______ 。

(1)试写出该金属硼化物的化学式(最简单正整数比)
(2)试计算
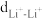 与Li+到(BxHy)n-多面体中心的距离
与Li+到(BxHy)n-多面体中心的距离(3)如果把Li+作为晶胞的原点,试写出新晶胞中Li+到(BxHy)n-的坐标
(4)若把晶体的结构基元围成一个平行六面体,写出该平行六面体中Li+到(BxHy)n-的原子坐标
(5)从晶体结构分析,该晶体可能作为何种功能材料?给出理由
您最近一年使用:0次
解题方法
2 . 鉴定NO 离子的方法之一是利用“棕色环”现象:将含有NO
离子的方法之一是利用“棕色环”现象:将含有NO 的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
(1)写出形成“棕色环”的反应方程式____ 。
(2)推出中心离子的价电子组态____ 、自旋态____ (高或低)和氧化态____ 。
(3)棕色物质中NO的键长与自由NO分子中N-O键长相比,变长还是变短____ ?简述理由____ 。
 离子的方法之一是利用“棕色环”现象:将含有NO
离子的方法之一是利用“棕色环”现象:将含有NO 的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。
的溶液放入试管,加入FeSO4,混匀,然后顺着管壁加入浓H2SO4, 在溶液的界面上出现“棕色环”。分离出棕色物质,研究发现其化学式为[Fe(NO)H2O)5]SO4.该物质显顺磁性,磁矩为3.8μB (玻尔磁子),未成对电子分布在中心离子周围。(1)写出形成“棕色环”的反应方程式
(2)推出中心离子的价电子组态
(3)棕色物质中NO的键长与自由NO分子中N-O键长相比,变长还是变短
您最近一年使用:0次



