名校
解题方法
1 . 氨基甲酸铵(H2NCOONH4)为尿素生产过程的中间产物,易分解。
已知:
Ⅰ.N2(g)+3H2(g) 2NH3(g) ΔH1=-92kJ•mol-1
2NH3(g) ΔH1=-92kJ•mol-1
Ⅱ.C(s)+O2(g) CO2(g) ΔH2=-394kJ•mo1-1
CO2(g) ΔH2=-394kJ•mo1-1
Ⅲ.N2(g)+3H2(g)+C(s)+O2(g) H2NCOONH4(s) ΔH3=-646kJ•mol-1
H2NCOONH4(s) ΔH3=-646kJ•mol-1
Ⅳ.H2NCOONH4(s) 2NH3(g)+CO2(g) ΔH4
2NH3(g)+CO2(g) ΔH4
回答下列问题:
(1)NH3的空间构型为________ ,NH3的键角大于PH3,分析原因为________ 。
(2)ΔH4=________ ;T℃下在某密闭容器中加入H2NCOONH4(s),假设只发生反应Ⅳ,达平衡时测得NH3的浓度为c1,保持温度不变,加压(缩小容器的体积),测得新的平衡条件下NH3的浓度为c2,则c1________ c2(填“>”“<”或“=”)。反应Ⅳ在________ (填“高温”“低温”或“任意温度”)条件下能够自发进行。
(3)某温度下在一刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,起始压强为1MPa,10min末达平衡,测得平衡时压强为0.8MPa,则10min内v(N2)=________ MPa/min,此时平衡常数Kp=________ 。对于该条件下的反应,下列说法错误的是________ 。
A.当H2的体积分数不变时,说明反应已经达到化学平衡状态
B.温度升高化学反应速率加快,化学平衡常数增大
C.其他条件不变时,若适当增加N2的用量,可以提高H2的平衡转化率
D.使用合适的催化剂可以加快化学反应速率,但ΔH1不变
(4)在一定的条件下,将AmolN2和BmolH2充入某体积固定的密闭容器中合成NH3,在不同的催化剂(甲或乙)下发生反应,反应相同时间后H2的转化率与温度的关系如图:
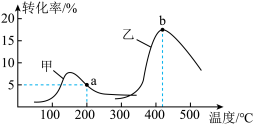
某学习小组的同学通过讨论得出结论:200℃时,a点对应的转化率(5%)不是使用催化剂甲、下H2的平衡转化率,判断依据是________ 。
已知:
Ⅰ.N2(g)+3H2(g)
 2NH3(g) ΔH1=-92kJ•mol-1
2NH3(g) ΔH1=-92kJ•mol-1Ⅱ.C(s)+O2(g)
 CO2(g) ΔH2=-394kJ•mo1-1
CO2(g) ΔH2=-394kJ•mo1-1Ⅲ.N2(g)+3H2(g)+C(s)+O2(g)
 H2NCOONH4(s) ΔH3=-646kJ•mol-1
H2NCOONH4(s) ΔH3=-646kJ•mol-1Ⅳ.H2NCOONH4(s)
 2NH3(g)+CO2(g) ΔH4
2NH3(g)+CO2(g) ΔH4回答下列问题:
(1)NH3的空间构型为
(2)ΔH4=
(3)某温度下在一刚性的密闭容器中,充入等物质的量N2和H2发生反应Ⅰ,起始压强为1MPa,10min末达平衡,测得平衡时压强为0.8MPa,则10min内v(N2)=
A.当H2的体积分数不变时,说明反应已经达到化学平衡状态
B.温度升高化学反应速率加快,化学平衡常数增大
C.其他条件不变时,若适当增加N2的用量,可以提高H2的平衡转化率
D.使用合适的催化剂可以加快化学反应速率,但ΔH1不变
(4)在一定的条件下,将AmolN2和BmolH2充入某体积固定的密闭容器中合成NH3,在不同的催化剂(甲或乙)下发生反应,反应相同时间后H2的转化率与温度的关系如图:

某学习小组的同学通过讨论得出结论:200℃时,a点对应的转化率(5%)不是使用催化剂甲、下H2的平衡转化率,判断依据是
您最近一年使用:0次



