名校
解题方法
1 . 下列设计的实验方案不能达到实验目的的是
| 选项 | 实验操作和现象 | 实验目的 |
| A. | 向0.1mol·L-1CuSO4溶液里逐滴加入1mol·L-1氨水至过量,先形成蓝色沉淀,后溶解得到深蓝色溶液 | 沉淀溶解时主要反应: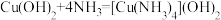 |
| B. | 向乙醇中加入一小粒金属钠,观察现象 | 检验乙醇中是否含有水 |
| C. | 以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极法 |
| D. | 用pH计分别测定等体积等浓度的CH3COOH溶液和ClCH2COOH溶液的pH,氯乙酸溶液的pH小于乙酸溶液 | 探究键的极性对羧酸酸性的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 盐酸羟胺 是一种还原剂和显像剂,其化学性质与
是一种还原剂和显像剂,其化学性质与 类似。
类似。
(1) 被
被 取代可形成羟胺
取代可形成羟胺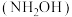 ,羟胺水溶液显碱性,用相关离子方程式解释原因
,羟胺水溶液显碱性,用相关离子方程式解释原因___________ 。
(2)已知氮原子上电子云密度越大则碱性越强,实验测得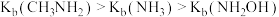 ,请解释原因:
,请解释原因:___________ 。
(3)采用原电池原理制备盐酸羟胺的装置如下图所示:

①含铁催化电极发生的电极反应式为___________ 。
②盐酸初始浓度相同,假设两侧溶液体积均为 且保持不变,理论上电路中通过
且保持不变,理论上电路中通过 电子时,左右两侧
电子时,左右两侧 浓度相差
浓度相差___________  。
。
 是一种还原剂和显像剂,其化学性质与
是一种还原剂和显像剂,其化学性质与 类似。
类似。(1)
 被
被 取代可形成羟胺
取代可形成羟胺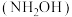 ,羟胺水溶液显碱性,用相关离子方程式解释原因
,羟胺水溶液显碱性,用相关离子方程式解释原因(2)已知氮原子上电子云密度越大则碱性越强,实验测得
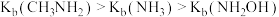 ,请解释原因:
,请解释原因:(3)采用原电池原理制备盐酸羟胺的装置如下图所示:

①含铁催化电极发生的电极反应式为
②盐酸初始浓度相同,假设两侧溶液体积均为
 且保持不变,理论上电路中通过
且保持不变,理论上电路中通过 电子时,左右两侧
电子时,左右两侧 浓度相差
浓度相差 。
。
您最近一年使用:0次
名校
解题方法
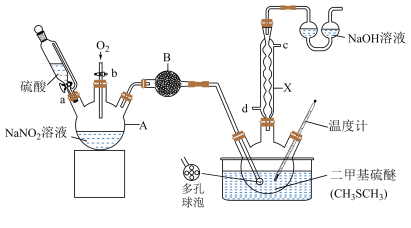
3 . 常温下,二甲基亚砜(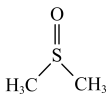 )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“NO2氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“NO2氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
已知:①制备二甲基亚砜的反应原理为: 。
。
②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为0.85g/cm3和1.10g/cm3。
③HNO2遇微热易分解为NO、NO2和水。
实验过程:将A仪器中制得的气体通入20.00mL二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到14.80mL二甲基亚砜纯品。回答下列问题:
(1)A的名称为___________ ;仪器x的进水口为___________ (填“d”或“c”)口;B中盛放的试剂的目的是干燥NO2,则B中盛放的试剂可能是___________ (填名称)。
(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是___________ 。
(3)实验中O2需过量的原因是___________ 。
(4)二甲基亚砜易溶于水的原因可能为___________ 。
(5)NaOH溶液吸收尾气中NO和NO2的化学方程式为___________ 。
(6)本实验的产率是___________ %(保留2位小数)。
 )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“NO2氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“NO2氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
已知:①制备二甲基亚砜的反应原理为:
 。
。②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为0.85g/cm3和1.10g/cm3。
③HNO2遇微热易分解为NO、NO2和水。
实验过程:将A仪器中制得的气体通入20.00mL二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到14.80mL二甲基亚砜纯品。回答下列问题:
(1)A的名称为
(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是
(3)实验中O2需过量的原因是
(4)二甲基亚砜易溶于水的原因可能为
(5)NaOH溶液吸收尾气中NO和NO2的化学方程式为
(6)本实验的产率是
您最近一年使用:0次



