名校
解题方法
1 . 下列“类比”合理的是
| A.NH3的沸点高于PH3,则CH4的沸点也高于SiH4 |
| B.AlCl3溶液中滴加NaOH溶液先生成白色沉淀后溶解,则滴加氨水也能出现相同的现象 |
| C.Fe3O4可改写成FeO·Fe2O3,则Pb3O4也可改写成PbO·Pb2O3(Pb为IVA族元素) |
| D.MnO2与浓HCl共热可制备Cl2,则MnO2与浓HBr共热可制备Br2 |
您最近一年使用:0次
2022-03-15更新
|
317次组卷
|
4卷引用:浙江省杭州第二中学2021届高三上学期期中考试化学试题
名校
2 . 下列有关物质结构和性质的表述正确的是
A.某微粒的结构示意图为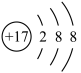 ,该元素位于周期表第三周期零族 ,该元素位于周期表第三周期零族 |
B.工业上用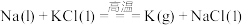 的反应来制备钾,是因为钠比钾更活泼 的反应来制备钾,是因为钠比钾更活泼 |
C. 的沸点高于 的沸点高于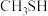 的沸点,原因与 的沸点,原因与 分子间存在氢键有关 分子间存在氢键有关 |
| D.糖类物质溶液中,蛋白质溶液中加硫酸铵都会产生盐析现象 |
您最近一年使用:0次
2019-09-12更新
|
189次组卷
|
2卷引用:浙江省杭州市2018-2019学年高二下学前期末考试化学试题
19-20高二·浙江·期中
3 . I.请回答下列问题:
(1)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1 mol 硼酸(H3BO3)晶体中含有___ mol 氢键。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:__________________ 。

(2)比较酸性的相对强弱:H2SO4__ HClO4 (填“>”“=”或“<”),已知能发生反应:H2SO4(浓)+NaClO4 HClO4+NaHSO4,说明该反应能发生的理由
HClO4+NaHSO4,说明该反应能发生的理由_______________ 。
Ⅱ.氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝。查阅资料:①实验室用饱和NaNO2溶液与NH4Cl溶液共热制N2:NaNO2+NH4Cl NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2
NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。
(1)氮化铝的制备

①实验中使用的装置如上图所示,请按照氮气流方向将各仪器接口连接:c→_____________ 。 (根据实验需要,上述装置可使用多次)
②D装置内氯化钯溶液的作用可能是_________________ 。
(2) AlN粉末会缓慢发生水解反应,粒径为100 nm的AlN粉末水解时溶液pH的变化如下图所示。

①AlN粉末水解的化学方程式是________________________ 。
②相同条件下,请在图中画出粒径为40 nm的AlN粉末水解的变化曲线__________ 。
(1)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1 mol 硼酸(H3BO3)晶体中含有

(2)比较酸性的相对强弱:H2SO4
 HClO4+NaHSO4,说明该反应能发生的理由
HClO4+NaHSO4,说明该反应能发生的理由Ⅱ.氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝。查阅资料:①实验室用饱和NaNO2溶液与NH4Cl溶液共热制N2:NaNO2+NH4Cl
 NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2
NaCl+N2↑+2H2O;②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。(1)氮化铝的制备

①实验中使用的装置如上图所示,请按照氮气流方向将各仪器接口连接:c→
②D装置内氯化钯溶液的作用可能是
(2) AlN粉末会缓慢发生水解反应,粒径为100 nm的AlN粉末水解时溶液pH的变化如下图所示。

①AlN粉末水解的化学方程式是
②相同条件下,请在图中画出粒径为40 nm的AlN粉末水解的变化曲线
您最近一年使用:0次
2020-12-18更新
|
524次组卷
|
3卷引用:【浙江新东方】105



