解题方法
1 . X 、Y 、Z 、W 、Q 、R为原子序数依次增大的短周期元素,在周期表中,X的原子半径最小,Z的主族序数是其周期数的三倍,Z与R的最外层电子数相等;Z与R的质子数之和是X与W的质子数之和两倍;Y元素的一种同位素可以用来测定文物年代;Q简单离子的半径是其所在周期中最小。请回答下列问题:
(1)Q元素在周期表中的位置是___________ ,W与R形成的化合物W2R的电子式是___________ 。
(2)Z、R的简单氢化物的沸点较高的是:___________ (填氢化物的化学式),解释原因是:___________ 。
(3)下列有关说法不正确 的是___________。
(1)Q元素在周期表中的位置是
(2)Z、R的简单氢化物的沸点较高的是:
(3)下列有关说法
| A.X与W形成的化合物属于共价化合物 |
| B.与Y同一主族的第四周期元素的原子序数为32 |
| C.X与Y形成的化合物中不可能含非极性键 |
| D.最高价氧化物对应的水化物碱性:Q<W |
您最近一年使用:0次
2 . 按要求解答下列各题。
(1)黄铜是人类最早使用的合金之一,主要由 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为_______ ;第二电离能
_______ (填“<”“>”或“=”)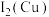 。
。
(2) 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为_______ 。 分子中
分子中
_______  分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇 ,其原因是
,其原因是_______ 。
(1)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为
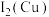 。
。(2)
 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为 分子中
分子中
 分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。(3)甲醇的沸点(64.7℃)介于水和甲硫醇
 ,其原因是
,其原因是
您最近一年使用:0次
解题方法
3 . 按要求回答下列问题:
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为___________ 。
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因___________ 。
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3___________  (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是___________ 。
(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序___________ ,并解释原因___________ 。
(1)前三周期元素中,基态原子核外有7组成对电子的原子,其价层电子的轨道表示式为
(2)已知H2O2的沸点为152℃,H2S的沸点-60.4℃。请解释两者沸点差异的原因
(3)BF3和NaBF4是硼的重要化合物,微粒中F-B-F键角:BF3
 (填“>”、“<”或“=” )。理由是
(填“>”、“<”或“=” )。理由是(4)将CH3COOH、FCH2COOH、CH3CH2COOH的酸性由强到弱排序
您最近一年使用:0次
解题方法
4 . 铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
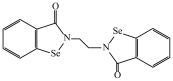
①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]_______ 。
②比较键角的大小:气态 分子
分子_______  离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是_______ 。
(2)富马酸亚铁(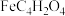 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
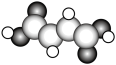
下列相关说法正确的是_______。
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为_______ 。
②Fe原子的配位数为_______ 。
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]
②比较键角的大小:气态
 分子
分子 离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是(2)富马酸亚铁(
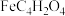 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
下列相关说法正确的是_______。
| A.富马酸分子中σ键和π键的数目比是10:3 |
B.富马酸分子中C的杂化方式有 、 、 |
| C.富马酸分子可以形成分子内氢键,使得富马酸一级和二级电离常数变大 |
| D.富马酸亚铁中各元素的电负性由大到小的顺序为O>C>H>Fe |
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为
②Fe原子的配位数为
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
5 . 茶文化是中国人民对世界饮食文化的一大贡献,茶叶中含有少量的咖啡因(结构简式如图)。下列关于咖啡因的说法正确的是
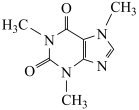

| A.咖啡因的分子式为C8H9N4O2 |
| B.咖啡因分子中sp2与 sp3杂化的C原子个数之比为5∶3 |
| C.咖啡因分子的一氯取代物只有3种 |
| D.咖啡因分子间存在氢键 |
您最近一年使用:0次
解题方法
6 . A、B、C、D、E为20号以前的元素,原子序数逐渐增大。A元素的原子最外层电子排布式为nsnnpn;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高能级的电子对数等于其最高能层的电子层数。下列说法正确的是
A.简单氢化物的沸点: |
| B.同周期元素第一电离能小于C的有5种 |
C.氧化物对应水化物的酸性: |
| D.A、D和C、E形成的化合物中可能均含有非极性共价键 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法不正确 的是
A.相同条件下的酸性:邻苯二甲酸 对苯二甲酸 对苯二甲酸 |
B.键角: |
C. 和甲醚 和甲醚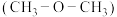 都是直线型非极性分子 都是直线型非极性分子 |
D.由三种元素构成的化合物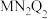 可能是极性分子,也可能是非极性分子 可能是极性分子,也可能是非极性分子 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
| A.由于固态水中水分子以氢键结合成排列规整的晶体,所以冰的密度比水小 |
| B.N、H、O三种元素组成的化合物一定只含共价键 |
C.NaOH和 中的化学键类型完全相同,都属于离子化合物 中的化学键类型完全相同,都属于离子化合物 |
D. 和 和 分子中,各原子均满足最外层8电子的稳定结构 分子中,各原子均满足最外层8电子的稳定结构 |
您最近一年使用:0次
2024-03-08更新
|
96次组卷
|
2卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
解题方法
9 . 下列说法正确的是
A. 的基态原子核外电子共占有8种不同的能级 的基态原子核外电子共占有8种不同的能级 |
B.邻羟基苯甲醛分子内氢键示意图: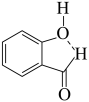 |
C.第四周期元素的基态原子中,未成对电子数最多的是 |
D. 分子中的 分子中的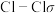 键形状: 键形状: |
您最近一年使用:0次
名校
10 . 下列对分子性质的解释中,不正确 的是

| A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键 |
| B.碘易溶于四氯化碳、甲烷难溶于水都可用“相似相溶”规律解释 |
| C.过氧化氢是含有极性键和非极性键的极性分子 |
D.青蒿素的分子式为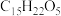 ,结构如图所示,该分子中包含7个手性碳原子 ,结构如图所示,该分子中包含7个手性碳原子 |
您最近一年使用:0次
2024-03-05更新
|
307次组卷
|
2卷引用:浙江省湖州市德清县求是高级中学有限公司2023-2024学年高二上学期期末考试化学试题



