解题方法
1 . X 、Y 、Z 、W 、Q 、R为原子序数依次增大的短周期元素,在周期表中,X的原子半径最小,Z的主族序数是其周期数的三倍,Z与R的最外层电子数相等;Z与R的质子数之和是X与W的质子数之和两倍;Y元素的一种同位素可以用来测定文物年代;Q简单离子的半径是其所在周期中最小。请回答下列问题:
(1)Q元素在周期表中的位置是___________ ,W与R形成的化合物W2R的电子式是___________ 。
(2)Z、R的简单氢化物的沸点较高的是:___________ (填氢化物的化学式),解释原因是:___________ 。
(3)下列有关说法不正确 的是___________。
(1)Q元素在周期表中的位置是
(2)Z、R的简单氢化物的沸点较高的是:
(3)下列有关说法
| A.X与W形成的化合物属于共价化合物 |
| B.与Y同一主族的第四周期元素的原子序数为32 |
| C.X与Y形成的化合物中不可能含非极性键 |
| D.最高价氧化物对应的水化物碱性:Q<W |
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
A. 的基态原子核外电子共占有8种不同的能级 的基态原子核外电子共占有8种不同的能级 |
B.邻羟基苯甲醛分子内氢键示意图: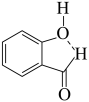 |
C.第四周期元素的基态原子中,未成对电子数最多的是 |
D. 分子中的 分子中的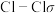 键形状: 键形状: |
您最近一年使用:0次
名校
解题方法
3 . 硼(B)及其化合物在化学中有重要的地位,请回答下列问题: 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:______ 。
(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。______ 。
②已知晶胞边长为361.5pm,则立方氮化硼的密度是______  。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
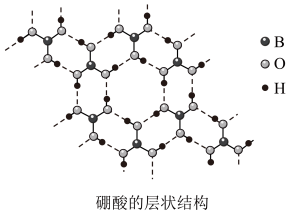
 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。①硼酸中B原子的杂化轨道类型为
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。

②已知晶胞边长为361.5pm,则立方氮化硼的密度是
 。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
您最近一年使用:0次
2024-03-05更新
|
151次组卷
|
3卷引用:浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期末考试化学试题
名校
4 . 下列说法正确的是
| A.硝酸是强电解质,在熔融状态下能导电 |
| B.硝酸分子中含有羟基,可形成分子间氢键,难挥发 |
C.工业制备硝酸第三步时不能用水直接吸收 |
| D.浓硝酸溅到皮肤上,皮肤会变黄 |
您最近一年使用:0次
名校
解题方法
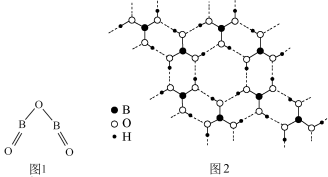
5 . B2O3的气态分子结构如图1所示,硼酸(H3BO3)晶体结构为层状,其二维平面结构如图2所示。下列说法不正确的是

| A.两分子中B原子分别采用sp杂化、sp2杂化 |
| B.硼酸晶体中层与层之前存在范德华力 |
| C.1molH3BO3晶体中含有6mol氢键 |
| D.元素第一电离能:B<Be |
您最近一年使用:0次
2024-01-30更新
|
128次组卷
|
2卷引用:08-2023新东方高二上期中考化学
名校
解题方法
6 . 下列化学用语的表达正确的是
A.邻羟基苯甲醛分子内氢键示意图: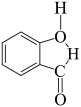 |
B.丙炔的球棍模型: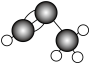 |
C. 过程中形成的是吸收光谱 过程中形成的是吸收光谱 |
D.Si原子电子排布式可能为: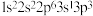 |
您最近一年使用:0次
名校
7 . 回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)高温下铝粉与氧化铁的反应可用来焊接钢轨。置换出的铁呈熔融态,熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。写出该反应的化学方程式,并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
8 . 黄铜矿的主要成份为 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。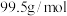 。请回答:
。请回答:
(1)尾气中 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:___________ 。
(2)煅烧含硫量高的矿物得到高浓度的 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
①写出物质A分子的结构式:___________ 。
②一定压强下,化合物A的沸点低于硫酸的原因是___________ 。
(3)生成沉淀D的离子反应方程式___________ 。
(4)请设计实验检验溶液C中的阳离子___________ 。
 ,现有如下转化关系制备有关物质。
,现有如下转化关系制备有关物质。
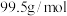 。请回答:
。请回答:(1)尾气中
 经过充分综合利用可以得到石膏,请写出石膏的化学式:
经过充分综合利用可以得到石膏,请写出石膏的化学式:(2)煅烧含硫量高的矿物得到高浓度的
 ,干燥的
,干燥的 气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。
气体与氯气在活性炭催化下可生成一种用于有机合成的常见物质A,该物质水解时发生非氧化还原反应得到两种强酸。①写出物质A分子的结构式:
②一定压强下,化合物A的沸点低于硫酸的原因是
(3)生成沉淀D的离子反应方程式
(4)请设计实验检验溶液C中的阳离子
您最近一年使用:0次
9 . 已知A、B、C、D是周期表中前三周期元素,且原子序数依次增大,其中A、B、C为同周期的非金属元素,且B、C原子中均有两个未成对电子,D元素s能级与p能级电子数相等,下列说法正确的是
| A.原子半径:A>B>C>D | B.第一电离能:A<B<C<D |
| C.D与 C 可形成高熔点的化合物 | D.最低价气态氢化物的沸点:A<C<B |
您最近一年使用:0次
名校
解题方法
10 . 某些微粒间相互作用的数据如下表所示:
根据表中数据,下列说法不正确 的是
微粒间相互作用 | 化学键 | 分子间作用力 | ||||||
|
|
|
|
|
|
| HCl | |
键能/范德华力强度 ( | 463 | 568 | 366 | 157 | 497 | 28.1 | 18.8 | 21.1 |
| A.上表的微粒间相互作用中有5种极性共价键,2种氢键 |
| B.键长:H-F<H-Br,但仅用上表数据无法比较两者与H-Cl的键长大小 |
C. 的 的 |
D.用上表数据可比较 与 与 的沸点高低 的沸点高低 |
您最近一年使用:0次
2023-07-31更新
|
230次组卷
|
2卷引用:浙江省台州市2022-2023学年高三上学期第一次教学质量评估化学试题






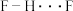
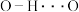
 )
)

