解题方法
1 . 漂白粉加水发生反应: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.沸点高低: | B.半径大小: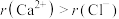 |
C.酸性强弱: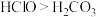 | D. 中只有离子键作用 中只有离子键作用 |
您最近一年使用:0次
2 . 已知胆矾(CuSO4•5H2O)中原子间的连接关系如图所示,其中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合。则该晶体中不含有的作用力有
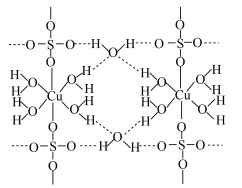
| A.氢键 | B.配位键 | C.极性键 | D.金属键 |
您最近一年使用:0次
解题方法
3 . 前4周期元素X、Y、Z、M、Q的原子序数依次增大,其中元素X的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;元素Y的2p轨道有3个未成对电子,元素Z的基态原子的2p轨道有1个成对电子,M是第4周期核外未成对电子数最多的元素,元素Q位于周期表Ⅷ族,是应用最广泛的金属。请用化学符号 回答下列问题:
(1)基态Q原子的核外电子排布式 为___________ 。
(2)X、Y、Z的简单气态氢化物中沸点最高的是___________ (写分子式 ),主要原因是___________ 。
(3)化合物H2Z2中Z原子的杂化方式为___________ 。
(4)XZ2中σ与π键数目之比为___________ 。
(5)MCl3·6H2O是六配位化合物,由于内界配体不同而有不同的颜色(暗绿色、浅绿色,紫色)。将1 mol暗绿色MCl3·6H2O晶体溶于水,加入足量硝酸银溶液,生成1 mol AgCl沉淀,则该暗绿色晶体中配离子的化学式 为___________ 。
(1)基态Q原子的
(2)X、Y、Z的简单气态氢化物中沸点最高的是
(3)化合物H2Z2中Z原子的杂化方式为
(4)XZ2中σ与π键数目之比为
(5)MCl3·6H2O是六配位化合物,由于内界配体不同而有不同的颜色(暗绿色、浅绿色,紫色)。将1 mol暗绿色MCl3·6H2O晶体溶于水,加入足量硝酸银溶液,生成1 mol AgCl沉淀,则该暗绿色晶体中配离子的
您最近一年使用:0次
4 . 下列物质的性质与用途具有对应关系的是
A. 有氢键,常用作制冷剂 有氢键,常用作制冷剂 |
B. 溶液呈酸性,可用作氮肥 溶液呈酸性,可用作氮肥 |
C. 受热易分解,可用作制备 受热易分解,可用作制备 |
D. 具有强氧化性,可用于制备硝酸纤维 具有强氧化性,可用于制备硝酸纤维 |
您最近一年使用:0次
5 . 已知A、B、C、D、E和F都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子价电子排布式为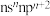 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
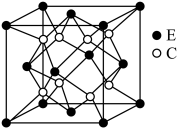
(1)元素F的符号是_____ ,基态F原子中有_____ 种能量不同的电子,其价电子轨道表示式为_____ 。
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是_____ 。
(3)从图中可以看出,C跟E形成的离子化合物的化学式为_____ ;E离子配位数为_____ 。
(4) 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为_____ , 是
是_____ (填“极性”或“非极性”)分子。
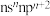 ,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
,C和D属同一主族,E和F属同一周期,又知F是周期表中1~18列中的第13列元素。C是周期表中电负性最大的元素,C跟E可形成离子化合物其晶胞结构如图。
(1)元素F的符号是
(2)C与A形成的化合物比D与A形成的化合物沸点高,其原因是
(3)从图中可以看出,C跟E形成的离子化合物的化学式为
(4)
 是一种强氧化剂,由
是一种强氧化剂,由 和
和 在低温下合成,
在低温下合成, 分子的电子式为
分子的电子式为 是
是
您最近一年使用:0次
解题方法
6 . 肼(N2H4)是一种良好的火箭推进剂,肼(N2H4)的燃烧热为624 kJ/mol。下列说法正确的是
A. 和NH3中的H—N—H键角前者大于后者 和NH3中的H—N—H键角前者大于后者 |
| B.N2H4分子中N原子轨道的杂化方式为sp2 |
C.肼在空气中燃烧的热化学方程式为:  |
| D.N2H4易液化是由于N2H4与H2O分子间形成氢键 |
您最近一年使用:0次
7 . 回答下列问题
(1)按要求填空:
① 的电子式为:
的电子式为:_____ ;
②基态N原子的电子排布式为_____ 。
(2)已知熔融的 不导电,则
不导电,则 属于
属于_____ 晶体,中心原子的杂化类型为_____ 。
(3)氨水是一种速效氮肥:
①氨水中存在_____ 种氢键,任写其中的一种_____ ;
②氨水中含有配位键的粒子有 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是_____ ,X离子能否作为其他配合物的配位体_____ (填“能”或“否”)。
(1)按要求填空:
①
 的电子式为:
的电子式为:②基态N原子的电子排布式为
(2)已知熔融的
 不导电,则
不导电,则 属于
属于(3)氨水是一种速效氮肥:
①氨水中存在
②氨水中含有配位键的粒子有
 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是
您最近一年使用:0次
名校
解题方法
8 . NH3易液化,能与多种物质发生反应。将金属钠投入液氨中有H2产生,NH3能与CaCl2结合生成CaCl2·8NH3,加热条件下,NH3能将CuO还原成Cu。NH3可用于制取肼(N2H4)和尿素[CO(NH2)2]等,工业上常用浓氨水检验输送氯气的管道是否泄漏,泄漏处有白烟生成。工业合成氨的反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。下列说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列说法正确的是
 2NH3(g) ΔH=-92.4 kJ/mol。下列说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列说法正确的是| A.N2H4分子中的H—N—H键角为120° | B.NH3与Cl2反应生成的白烟成分为NH4Cl |
| C.金属钠与液氨反应体现了NH3的还原性 | D.NH3易液化是由于NH3与H2O分子间形成氢键 |
您最近一年使用:0次
名校
9 . 下列关于化学键和分子间作用力的说法中正确的个数是
①含有金属元素的化合物一定是离子化合物
②第IA族和第VIIA族原子化合时,一定形成离子键
③由非金属元素形成的化合物一定是共价化合物
④物质中一定存在化学键
⑤冰的密度比水小,是因为水分子之间存在氢键
⑥CO2溶于水和干冰升华都只有分子间作用力的改变
⑦纯碱和烧碱熔化时克服的化学键类型相同
①含有金属元素的化合物一定是离子化合物
②第IA族和第VIIA族原子化合时,一定形成离子键
③由非金属元素形成的化合物一定是共价化合物
④物质中一定存在化学键
⑤冰的密度比水小,是因为水分子之间存在氢键
⑥CO2溶于水和干冰升华都只有分子间作用力的改变
⑦纯碱和烧碱熔化时克服的化学键类型相同
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
2024-03-02更新
|
195次组卷
|
2卷引用:江苏省无锡市辅仁高级中学2023-2024学年高一上学期期末复习化学模块综合试卷(一)
名校
解题方法
10 . VA族元素及其化合物应用广泛。 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。氨硼烷(
)是第三代半导体材料,熔点高,硬度大。氨硼烷( )是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
)是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
 催化氧化生成
催化氧化生成 ,
, 继续被氧化为
继续被氧化为 ,将
,将 通入水中制取
通入水中制取 。工业上用白磷(
。工业上用白磷( )与
)与 反应生成
反应生成 和一种盐,该盐可与
和一种盐,该盐可与 反应制备一元弱酸
反应制备一元弱酸 。雌黄(
。雌黄( )和
)和 在盐酸中反应转化为雄黄(
在盐酸中反应转化为雄黄( )和
)和 (沸点114℃)并放出
(沸点114℃)并放出 气体。砷化镓(
气体。砷化镓( )是第三代半导体材料,熔点高,硬度大。氨硼烷(
)是第三代半导体材料,熔点高,硬度大。氨硼烷( )是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是
)是最具潜力的储氢材料之一,与乙烷的相对分子质量相近,但沸点却比乙烷高得多。下列说法不正确的是A. 分子间存在氢键 分子间存在氢键 | B. 是由极性键构成的极性分子 是由极性键构成的极性分子 |
C.1mol 中含有16mol共价键 中含有16mol共价键 | D.固态 和砷化镓晶体都是分子晶体 和砷化镓晶体都是分子晶体 |
您最近一年使用:0次



