1 . 完成下列问题
(1)氨气极易溶于水,原因是___________
(2) 的VSEPR理想模型名称为
的VSEPR理想模型名称为___________ ,离子空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(3) 中存在的化学键类型有
中存在的化学键类型有___________
①离子键 ②极性共价键 ③非极性共价键 ④氢键
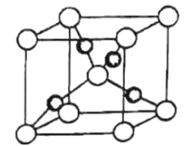
(4)一个 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为___________ 。
(1)氨气极易溶于水,原因是
(2)
 的VSEPR理想模型名称为
的VSEPR理想模型名称为(3)
 中存在的化学键类型有
中存在的化学键类型有①离子键 ②极性共价键 ③非极性共价键 ④氢键
(4)一个
 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)热稳定性:CH4___________  ;沸点:
;沸点:
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(2)实验室用 检验
检验 ,
, 中
中 键、
键、 键数目之比为
键数目之比为___________ 。
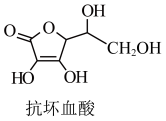
(3)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性___________ (填“难”或“易”)溶于水;
(4)单质铜及镍都是由___________ 键形成的晶体:元素铜与镍的第二电离能分别为: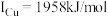 ,
, ,第二电离能
,第二电离能 的原因是
的原因是___________ 。
(5)Al的卤化物的熔点如下:
表中卤化物熔点差异的原因是___________ 。
(6)化合物AlN是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。
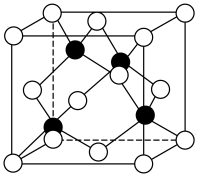
①若AlN的晶胞边长为apm( ),则晶体的密度为
),则晶体的密度为___________  (用
(用 表示阿伏加德罗常数AlN的相对分子质量为41)。
表示阿伏加德罗常数AlN的相对分子质量为41)。
②立方AlN和BN均为共价晶体,结构相似,BN的熔点高于AlN的原因是___________ 。
(1)热稳定性:CH4
 ;沸点:
;沸点:
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(2)实验室用
 检验
检验 ,
, 中
中 键、
键、 键数目之比为
键数目之比为(3)抗坏血酸的分子结构如图所示,推测抗坏血酸在水中的溶解性

(4)单质铜及镍都是由
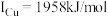 ,
, ,第二电离能
,第二电离能 的原因是
的原因是(5)Al的卤化物的熔点如下:
 |  |  | |
| 熔点/K | 256.8 | 304 | 413 |
(6)化合物AlN是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。

①若AlN的晶胞边长为apm(
 ),则晶体的密度为
),则晶体的密度为 (用
(用 表示阿伏加德罗常数AlN的相对分子质量为41)。
表示阿伏加德罗常数AlN的相对分子质量为41)。②立方AlN和BN均为共价晶体,结构相似,BN的熔点高于AlN的原因是
您最近一年使用:0次
3 . 下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)③原子的核外电子轨道表示式是_______ 。
(2)写出元素⑩的原子核外价电子排布式:_______ ,该元素属于_______ 区元素。
(3)在标号的主族元素中,电负性最大的是_______ (填元素符号)。
(4)元素④⑦⑪的气态氢化物沸点由高到低的顺序为:_______ (填化学式)。
(5)CO2中C原子采用_______ 杂化,是_______ 分子(填极性或非极性),干冰中每个CO2分子周围紧邻_______ 个CO2分子


请回答下列问题:
(1)③原子的核外电子轨道表示式是
(2)写出元素⑩的原子核外价电子排布式:
(3)在标号的主族元素中,电负性最大的是
(4)元素④⑦⑪的气态氢化物沸点由高到低的顺序为:
(5)CO2中C原子采用

您最近一年使用:0次
解题方法
4 . 下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
5 . 化合物Ⅲ是一种用于制备神经抑制剂的中间体,其合成路线如下:
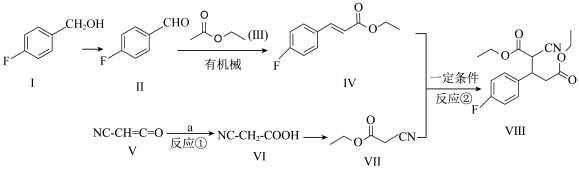
回答下列问题:
(1)①化合物I的分子式是_____ ,其命名为_____ 。其核磁共振氢谱中峰面积之比为_____ 。
②化合物Ⅳ中官能团的名称分别是_____ 。
(2)化合物I的沸点高于化合物Ⅱ,其原因是_____ 。
(3)反应①是原子利用率100%的反应,则a为_____ (填化学式)。
(4)VⅢ分子中含有_____ 个手性碳原子。Ⅱ分子中含有_____ 个sp3杂化的碳原子
(5)下列方法中可用于区分化合物I和Ⅱ的是_____ (填序号)。
a.质谱 b.核磁共振氢谱 c.红外光谱 d.原子的发射光谱

回答下列问题:
(1)①化合物I的分子式是
②化合物Ⅳ中官能团的名称分别是
(2)化合物I的沸点高于化合物Ⅱ,其原因是
(3)反应①是原子利用率100%的反应,则a为
(4)VⅢ分子中含有
(5)下列方法中可用于区分化合物I和Ⅱ的是
a.质谱 b.核磁共振氢谱 c.红外光谱 d.原子的发射光谱
您最近一年使用:0次
6 . 很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

(1)基态硫原子价层电子排布式为___________ ;其核外有___________ 个运动状态不同的电子;其最外层有___________ 个未成对电子;其最高能级的轨道有___________ 个伸展方向,电子云形状为___________ 。
(2) 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为___________
(3) (硒)与硫同主族,位于元素周期表第
(硒)与硫同主族,位于元素周期表第___________ 周期第___________ 族。
(4)化合物Ⅲ也是一种汞解毒剂。下列关于上述物质的说法正确的有___________ 。
A.在Ⅰ和Ⅳ中S原子均采取 杂化
杂化
B.在Ⅱ中所有元素中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)基态硫原子价层电子排布式为
(2)
 、
、 、
、 的沸点由高到低顺序为
的沸点由高到低顺序为(3)
 (硒)与硫同主族,位于元素周期表第
(硒)与硫同主族,位于元素周期表第(4)化合物Ⅲ也是一种汞解毒剂。下列关于上述物质的说法正确的有
A.在Ⅰ和Ⅳ中S原子均采取
 杂化
杂化B.在Ⅱ中所有元素中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
解题方法
7 . 前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(1)E元素基态原子简化电子排布式为___________ ;F元素价层电子轨道表示式为___________ ;
(2)A、B、C、D四种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)B、C、D三种元素的简单离子的半径由大到小顺序为___________ (用离子符号表示)。
(4)元素B的简单气态氢化物的沸点___________ (填“高于”或“低于”)元素D的简单气态氢化物的沸点;
(5)元素A的简单气态氢化物分子的空间结构为___________ ,分子中A原子的杂化类型为___________ 。
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子价电子排布式为 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
| F | 基态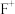 各能级电子全充满 各能级电子全充满 |
(1)E元素基态原子简化电子排布式为
(2)A、B、C、D四种元素第一电离能由大到小的顺序为
(3)B、C、D三种元素的简单离子的半径由大到小顺序为
(4)元素B的简单气态氢化物的沸点
(5)元素A的简单气态氢化物分子的空间结构为
您最近一年使用:0次
解题方法
8 . 下列说法中正确的是
A.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: |
| B.非极性分子中只有非极性键,极性分子中只有极性键。 |
| C.邻羟基苯甲醛能形成分子内氢键,而对羟基苯甲醛能形成分子间氢键,所以前者的熔点高于后者 |
| D.乙醇分子和水分子间只存在范德华力 |
您最近一年使用:0次
解题方法
9 . 下列有关物质结构和性质的比较中,错误的是
| A.熔点:MgCl2>AlCl3 |
| B.键角:CS2>SO2 |
| C.沸点:NH3>HF |
| D.沸点:对羟基苯甲醛>邻羟基苯甲醛 |
您最近一年使用:0次
2024-03-13更新
|
143次组卷
|
2卷引用:广东省普宁市勤建学校2023-2024学年高三上学期第三次月考化学试题
10 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 液氨常用作制冷剂 | 氨分子间能形成氢键 |
| B | 电解氯化镁溶液可制得金属 |  可在电解池的阴极还原成 可在电解池的阴极还原成 |
| C | 热的 溶液可去除油污 溶液可去除油污 |  能与油污中的羧基反应 能与油污中的羧基反应 |
| D |  的硫酸中 的硫酸中 浓度大于同 浓度大于同 的醋酸 的醋酸 | 硫酸是强酸,醋酸是弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



