完成下列问题
(1)氨气极易溶于水,原因是___________
(2) 的VSEPR理想模型名称为
的VSEPR理想模型名称为___________ ,离子空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(3) 中存在的化学键类型有
中存在的化学键类型有___________
①离子键 ②极性共价键 ③非极性共价键 ④氢键
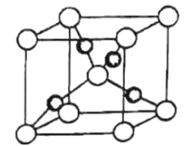
(4)一个 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为___________ 。
(1)氨气极易溶于水,原因是
(2)
 的VSEPR理想模型名称为
的VSEPR理想模型名称为(3)
 中存在的化学键类型有
中存在的化学键类型有①离子键 ②极性共价键 ③非极性共价键 ④氢键
(4)一个
 晶胞(见图)中,Cu原子的数目为
晶胞(见图)中,Cu原子的数目为
更新时间:2024-04-03 20:41:25
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)写出下列物质的电子式:
NH4Cl_______ ,N2_______ ,HClO_______ 。
(2)用电子式表示出下列化合物形成过程:
Na2O_______ ,CO2_______ 。
(3)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是_______ ;只含有共价键的是_______ ;既含有离子键又含有共价键的是_______ ;含有非极性共价键的化合物是_______ ;不含化学键的是_______ 。
NH4Cl
(2)用电子式表示出下列化合物形成过程:
Na2O
(3)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有下列八种物质: HCl、NH4Cl、N2、Na2O2、CaCl2、Cl2、NaF、CO2。
(1)只含有离子键的物质是______ (填化学式,下同)。
(2)既含有离子键,又含有共价键的物质是______ 。
(3)属于共价化合物的是____ ,其中所有原子都满足8电子结构的是_____ 。
(4)写出NaF的电子式_________________ 。
(1)只含有离子键的物质是
(2)既含有离子键,又含有共价键的物质是
(3)属于共价化合物的是
(4)写出NaF的电子式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)在①NaCl、②NaOH、③Na2O2、④N2、⑤H2S、⑥H2O2中,只含有离子键的是_____ ;只含有极性键的是____ ;只含有非极性键的是___ ;既含有离子键,又含有极性键的是____ ;既含有离子键,又含有非极性键的是______ 。
(2)请用电子式表示NaCl的形成过程:______ 。
(3)N2的结构式为:_____ ;H2O2的结构式为:_____ 。
(4)写出下列微粒的电子式。
①CO2___________ ;
②
___________ 。
(2)请用电子式表示NaCl的形成过程:
(3)N2的结构式为:
(4)写出下列微粒的电子式。
①CO2
②

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】 与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
___________  (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:___________ 。
 与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
 (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)计算下列分子或离子中带“•”原子的价电子对数。
①C Cl4______ ②B eCl2______ ③B Cl3______ ④P Cl3_____ 。
(2)计算下列微粒中带“•”原子的孤电子对数。
①H2S ______ ②P Cl5______ ③B F3______ ④N H3______ 。
(3)用价层电子对互斥模型推测下列分子或离子的立体构型。
①H2Se______ ;②NH
______ ;③BBr3______ ;④CHCl3______ ;⑤SiF4_____ 。
(1)计算下列分子或离子中带“•”原子的价电子对数。
①
(2)计算下列微粒中带“•”原子的孤电子对数。
①H2
(3)用价层电子对互斥模型推测下列分子或离子的立体构型。
①H2Se

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
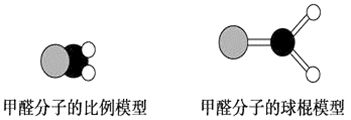
(1)甲醛分子中碳原子的杂化方式是__________ ,作出该判断的主要理由是__________________________ 。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________ (填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________ (填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________ 。

(1)甲醛分子中碳原子的杂化方式是
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)比较结合H+能力的相对强弱:
_________  ( 填“> ”“< ”或“= ”)用一个离子方程式说明
( 填“> ”“< ”或“= ”)用一个离子方程式说明 给出 H+的能力比H2O强 :
给出 H+的能力比H2O强 :______________ 。
(2)联氨N2H4是共价化合物,各原子均满足2或8电子稳定结构。写出联氨的电子式:__________________________ 。
(3)NH3极易溶于水的主要原因是_____________________ 。

 ( 填“> ”“< ”或“= ”)用一个离子方程式说明
( 填“> ”“< ”或“= ”)用一个离子方程式说明 给出 H+的能力比H2O强 :
给出 H+的能力比H2O强 :(2)联氨N2H4是共价化合物,各原子均满足2或8电子稳定结构。写出联氨的电子式:
(3)NH3极易溶于水的主要原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)已知乙醛的沸点为20.8℃,乙醇的沸点为78℃。乙醛沸点比乙醇沸点低的主要原因是______ 。
(2)有科学家在实验室条件下将干冰制成了原子晶体。则同是原子晶体的 和
和 硬度大小关系
硬度大小关系
______  (填“>”、“<”或“=”),从结构的角度说明理由
(填“>”、“<”或“=”),从结构的角度说明理由______ 。
(2)有科学家在实验室条件下将干冰制成了原子晶体。则同是原子晶体的
 和
和 硬度大小关系
硬度大小关系
 (填“>”、“<”或“=”),从结构的角度说明理由
(填“>”、“<”或“=”),从结构的角度说明理由
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】数十亿年来,地球上的物质不断变化,大气的成分也发生了很大的变化。下表是目前空气和原始大气的主要成分:
用上表所涉及的分子填写下列空白:
(1)含有10个电子的分子有___________ (填化学式,下同)。
(2)由极性键构成的非极性分子有___________ 。
(3)沸点最高的是___________ ,用所学知识解释其沸点高的原因:___________ 。
(4)分子中不含孤电子对的分子(除稀有气体外)有___________ ,它的立体构型为___________ 。
(5)___________ 极易溶于水,它之所以极易溶于水是因为它的分子和水分子之间可形成___________ 。
| 目前空气的主要成分 |  、 、 、 、 、水蒸气及稀有气体(He、Ne等) 、水蒸气及稀有气体(He、Ne等) |
| 原始大气的主要成分 |  、 、 、CO、 、CO、 等 等 |
(1)含有10个电子的分子有
(2)由极性键构成的非极性分子有
(3)沸点最高的是
(4)分子中不含孤电子对的分子(除稀有气体外)有
(5)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】物质的组成与结构决定了物质的性质与变化,回答下列问题:
(1)量子力学把电子在原子核外的一个空间运动状态称为一个____________ ,电子除空间运动状态外,还有一种运动状态叫做____________ 。
(2)硒常用作光敏材料,基态硒原子的价电子排布式为_______________ ;与硒同周期的p区元素中第一电离能大于硒的元素有_________ 种。
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下图,As原子的杂化方式为___________ ,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式________________ 。SnCl4分子的空间构型为_______ 。
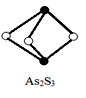
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心则形成的储氢化合物的化学式为_________ 。
②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为_______ 。(不必计算出结果,用NA表示阿伏伽德罗常数。)
(1)量子力学把电子在原子核外的一个空间运动状态称为一个
(2)硒常用作光敏材料,基态硒原子的价电子排布式为
(3)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如下图,As原子的杂化方式为

(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心则形成的储氢化合物的化学式为
②测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)Li2O是离子晶体,其晶格能可通过图甲的Born-Haber循环计算得到。
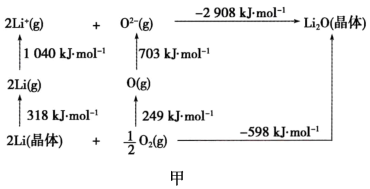
①由图甲可知,Li原子的第一电离能为______ kJ/mol,O=O键键能为______ kJ/mol,Li2O晶格能为______ kJ/mol。
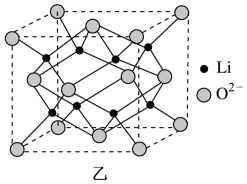
②Li2O具有反萤石结构,晶胞如图乙所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为______ g/cm3 (列出计算式)。
(2)FeS2晶体的晶胞如图所示。晶胞边长为anm、FeS2相对分子质量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______ g/cm3;晶胞中Fe2+位于S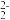 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为______ nm。

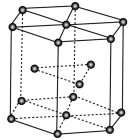
(3)金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为______ g/cm3 (列出计算式)。

①由图甲可知,Li原子的第一电离能为
②Li2O具有反萤石结构,晶胞如图乙所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为

(2)FeS2晶体的晶胞如图所示。晶胞边长为anm、FeS2相对分子质量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为
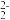 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
(3)金属Zn晶体中的原子堆积方式如图所示,六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为

您最近一年使用:0次




