名校
解题方法
1 . Ⅰ.8−羟基喹啉( )被广泛用作
)被广泛用作 等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
(1)8−羟基喹啉的熔点明显低于7−羟基喹啉(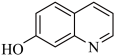 )、6−羟基喹啉(
)、6−羟基喹啉(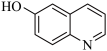 )的熔点的原因是
)的熔点的原因是___________ 。
(2)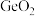 不能形成类似
不能形成类似 分子中的
分子中的 键,原因是
键,原因是___________ 。
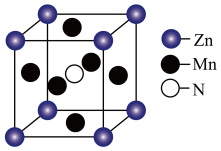
(3)某种含 特殊材料的晶胞结构如图所示,若该晶体的密度为
特殊材料的晶胞结构如图所示,若该晶体的密度为 ,则晶体中相邻N之间的最短距离为
,则晶体中相邻N之间的最短距离为___________  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
Ⅱ. 等氟化物可以做光导纤维材料,一定条件下,某
等氟化物可以做光导纤维材料,一定条件下,某 的晶体结构如下图。
的晶体结构如下图。

(4)与 距离最近且相等的
距离最近且相等的 有
有___________ 个,与 距离最近且相等的F-有
距离最近且相等的F-有___________ 个。
(5) 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶胞为正方体,边长为
晶胞为正方体,边长为 ,则晶体的摩尔体积
,则晶体的摩尔体积
___________  。(
。( )
)
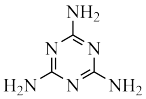
(6)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。
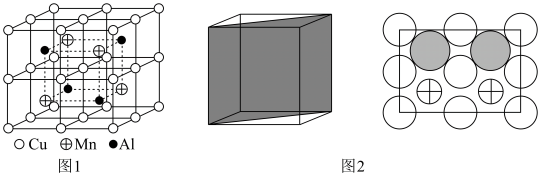
将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是___________。(填字母序号)
(7)一种类石墨的聚合物g﹣C3N4可由三聚氰胺制得。三聚氰胺分子不溶于冷水,溶于热水,主要原因是___________ 。
 )被广泛用作
)被广泛用作 等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:
等金属离子的络合剂和萃取剂,也是重要的医药中间体。回答下列问题:(1)8−羟基喹啉的熔点明显低于7−羟基喹啉(
 )、6−羟基喹啉(
)、6−羟基喹啉( )的熔点的原因是
)的熔点的原因是(2)
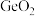 不能形成类似
不能形成类似 分子中的
分子中的 键,原因是
键,原因是(3)某种含
 特殊材料的晶胞结构如图所示,若该晶体的密度为
特殊材料的晶胞结构如图所示,若该晶体的密度为 ,则晶体中相邻N之间的最短距离为
,则晶体中相邻N之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
Ⅱ.
 等氟化物可以做光导纤维材料,一定条件下,某
等氟化物可以做光导纤维材料,一定条件下,某 的晶体结构如下图。
的晶体结构如下图。
(4)与
 距离最近且相等的
距离最近且相等的 有
有 距离最近且相等的F-有
距离最近且相等的F-有(5)
 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶胞为正方体,边长为
晶胞为正方体,边长为 ,则晶体的摩尔体积
,则晶体的摩尔体积
 。(
。( )
)(6)Cu-Mn-Al合金的晶胞如图1所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,如图2是沿立方格子对角面取得的截图。

将Cu-Mn-Al合金晶胞沿棱投影于垂直面的是___________。(填字母序号)
A.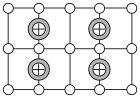 | B.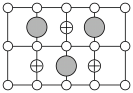 |
C. | D.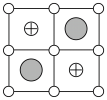 |
(7)一种类石墨的聚合物g﹣C3N4可由三聚氰胺制得。三聚氰胺分子不溶于冷水,溶于热水,主要原因是

您最近一年使用:0次
解题方法
2 . 下列有关物质结构和性质的比较中,错误的是
| A.熔点:MgCl2>AlCl3 |
| B.键角:CS2>SO2 |
| C.沸点:NH3>HF |
| D.沸点:对羟基苯甲醛>邻羟基苯甲醛 |
您最近一年使用:0次
2024-03-13更新
|
143次组卷
|
2卷引用:2024年中华人民共和国普通高等学校联合招收华侨港澳台学生高三下学期第二次模拟考试化学试题
名校
解题方法
3 . 下列关于分子的结构或性质的解释正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角: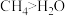 |  的键长大于 的键长大于 的键长 的键长 |
| B | 用乙酸乙酯而不用水溶解油漆 | 乙酸乙酯与油漆中的成分极性都较小,利用了相似相溶原理,而水分子极性较大,对油漆溶解效果不好 |
| C | 酸性: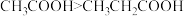 | 烃基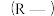 越长,推电子效应越小,羧基中羟基的极性越大,羧酸的酸性越弱 越长,推电子效应越小,羧基中羟基的极性越大,羧酸的酸性越弱 |
| D | 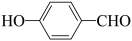 的沸点高于 的沸点高于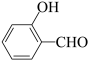 | 因为 分子间的范德华力大于 分子间的范德华力大于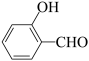 分子间的范德华力 分子间的范德华力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
590次组卷
|
3卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期末考试化学试题
4 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X的原子半径小于Y的原子半径,Z基态原子核外有3个未成对电子,Y的核外电子数与Z的价层电子数相等,Q2是氧化性最强的单质,下列说法正确的是
| A.键能:Z2<W2<Q2 | B.YQ3、ZQ3 均为非极性分子 |
| C.沸点:X2W<XQ | D.同周期中第一电离能介于Y和Z之间的元素有3种 |
您最近一年使用:0次
2024-03-09更新
|
344次组卷
|
4卷引用:名校期末好题汇编-分子结构与性质(选择题)
名校
解题方法
5 . 下列说法正确的是
| A.由于固态水中水分子以氢键结合成排列规整的晶体,所以冰的密度比水小 |
| B.N、H、O三种元素组成的化合物一定只含共价键 |
C.NaOH和 中的化学键类型完全相同,都属于离子化合物 中的化学键类型完全相同,都属于离子化合物 |
D. 和 和 分子中,各原子均满足最外层8电子的稳定结构 分子中,各原子均满足最外层8电子的稳定结构 |
您最近一年使用:0次
2024-03-08更新
|
117次组卷
|
3卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
名校
6 . As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3。下列说法正确的是

| A.As2O3分子中As原子的杂化方式为sp3 |
| B.LiAlH4为共价化合物 |
| C.AsCl3空间构型为平面正三角形 |
| D.沸点:NH3<PH3<AsH3 |
您最近一年使用:0次
2024-03-08更新
|
224次组卷
|
2卷引用:安徽省阜阳市第三中学2023-2024学年高二上学期1月期末化学试题
解题方法
7 . 下列关于晶体的说法中,正确的是
| A.冰融化时,分子中H—O键发生断裂 |
| B.共价晶体中,共价键的键能越大,熔点越高 |
| C.分子晶体中,共价键的键能越大,该晶体的熔、沸点一定越高 |
| D.分子晶体中,分子间作用力越大,对应的物质越稳定 |
您最近一年使用:0次
名校
8 . 下列现象与氢键无关的是
| A.乙醇可以和水以任意比互溶 | B.冰的密度比液态水的密度小 |
| C.HF的沸点比HCl的沸点高 | D.水分子在较高温度下也很稳定 |
您最近一年使用:0次
2024-03-07更新
|
158次组卷
|
2卷引用:名校期末好题汇编-分子结构与性质(选择题)
名校
解题方法
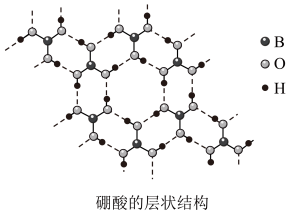
9 . 硼(B)及其化合物在化学中有重要的地位,请回答下列问题: 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:______ 。
(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。______ 。
②已知晶胞边长为361.5pm,则立方氮化硼的密度是______  。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
 是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。①硼酸中B原子的杂化轨道类型为
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性、硼酸的电离方程式:
而呈酸性、硼酸的电离方程式:(2)立方氮化硼的结构与金刚石相似,晶胞结构如图所示。

②已知晶胞边长为361.5pm,则立方氮化硼的密度是
 。(只要求列算式,不必计算出数值,阿伏加德罗常数用
。(只要求列算式,不必计算出数值,阿伏加德罗常数用 表示)
表示)
您最近一年使用:0次
2024-03-05更新
|
151次组卷
|
3卷引用:浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 物质结构决定性质。下列叙述1和叙述2都正确且二者有相关性的是
| 叙述1 | 叙述2 | |
| A | NF3分子中N原子价层有4个电子对 | NF3分子是非极性分子 |
| B |
| 邻羟基苯甲酸的Ka2大于苯酚 |
| C | 酸性:HCOOH>CH3COOH | O-H的极性:HCOOH强于CH3COOH |
| D | O2与O3分子极性相同 | 都是由非极性键构成的非极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-05更新
|
206次组卷
|
2卷引用:河北省石家庄市第二中学2023-2024学年高三上学期期末考试化学试题

 分子内氢键较稳定
分子内氢键较稳定

