回答下列问题
(1)按要求填空:
① 的电子式为:
的电子式为:_____ ;
②基态N原子的电子排布式为_____ 。
(2)已知熔融的 不导电,则
不导电,则 属于
属于_____ 晶体,中心原子的杂化类型为_____ 。
(3)氨水是一种速效氮肥:
①氨水中存在_____ 种氢键,任写其中的一种_____ ;
②氨水中含有配位键的粒子有 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是_____ ,X离子能否作为其他配合物的配位体_____ (填“能”或“否”)。
(1)按要求填空:
①
 的电子式为:
的电子式为:②基态N原子的电子排布式为
(2)已知熔融的
 不导电,则
不导电,则 属于
属于(3)氨水是一种速效氮肥:
①氨水中存在
②氨水中含有配位键的粒子有
 和X,则X离子中形成的配位键中提供孤电子对的原子是
和X,则X离子中形成的配位键中提供孤电子对的原子是
更新时间:2024-03-15 08:08:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其价电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其原子的简化电子排布式为_______ ,有_______ 个未成对电子。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ 。
(5)碳和氢形成的最简单碳正离子CH ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为_______ ,该阳离子的空间构型为_______ 。
(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_______ ,离子反应方程式为_______ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为_______ ,中心原子的配位数为_______ 。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)碳和氢形成的最简单碳正离子CH
 ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】硅的原子结构、性质、用途及存在形式
硅元素的原子核外电子排布为_______ ,从结构可知,硅的最低价为_______ 价,最高价为_______ 价,硅在周期表中的位置是_______ 。硅在周期表中金属与非金属的交界处,所以硅能导电,但是导电性介于导体与绝缘体之间,是目前应用最为广泛的_______ 。硅元素在地壳中含量排名第_______ ,主要以_______ 和_______ 形式存在。
硅元素的原子核外电子排布为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为-96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)铬(24号元素)基态原子的电子排布式为____ 。
(2)CH3COCH3分子中含有____ 个π键,含有____ 个σ键。
(3)固态氯化铬酰属于____ 晶体,丙酮中碳原子的杂化方式为____ ,二硫化碳属于____ (填“极性”或“非极性”)分子,分子中含有____ (填“极性”或“非极性”)键。
(1)铬(24号元素)基态原子的电子排布式为
(2)CH3COCH3分子中含有
(3)固态氯化铬酰属于
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】乙炔( )、丙烯腈(
)、丙烯腈( )、乙烯酮(
)、乙烯酮(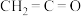 )是有机合成工业的重要原料。工业上曾用
)是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与
反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与 在一定条件下反应生成乙烯酮。回答下列问题:
在一定条件下反应生成乙烯酮。回答下列问题:
(1)写出基态钙原子的核外电子排布式:___________ ;Cu元素在元素周期表中的位置为___________ 。
(2)乙炔分子的空间结构为___________ ,乙炔分子属于___________ (填“极性”或“非极性”)分子。
(3)丙烯腈分子中碳原子的杂化轨道类型是___________ 。
(4)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为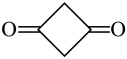 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为___________ 。
 )、丙烯腈(
)、丙烯腈( )、乙烯酮(
)、乙烯酮(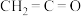 )是有机合成工业的重要原料。工业上曾用
)是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与
反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与 在一定条件下反应生成乙烯酮。回答下列问题:
在一定条件下反应生成乙烯酮。回答下列问题:(1)写出基态钙原子的核外电子排布式:
(2)乙炔分子的空间结构为
(3)丙烯腈分子中碳原子的杂化轨道类型是
(4)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为
 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知A、B、C、D都是短周期元素,它们的原子半径大小顺序为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。
试回答下列问题(用元素符号或化学式表示):
(1)基态B原子中,核外存在___________ 个未成对电子。
(2)基态E2+的核外电子排布式为___________ 。
(3)基态D原子的最高能层的电子排布图为___________
(4)M分子中B原子轨道的杂化类型为___________ 。
(5)B、C、D三种元素的第一电离能由小到大的顺序为___________ 。
试回答下列问题(用元素符号或化学式表示):
(1)基态B原子中,核外存在
(2)基态E2+的核外电子排布式为
(3)基态D原子的最高能层的电子排布图为
(4)M分子中B原子轨道的杂化类型为
(5)B、C、D三种元素的第一电离能由小到大的顺序为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】B、C、N、 是几种常见的非金属元素,其形成的各种化合物在自然界中广泛存在。
是几种常见的非金属元素,其形成的各种化合物在自然界中广泛存在。
(1)基态硅原子的电子排布式为_______ ;C、N、O元素的第一电离能由大到小的顺序为_______ 。
(2) 与一定量的水可形成如图甲所示晶体R。
与一定量的水可形成如图甲所示晶体R。
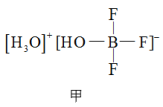
①晶体R中各种微粒间的作用力涉及_______ (填序号);
a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
②晶体R中阴离子的空间结构为_______ 。
(3)乙二胺( )与
)与 溶液可形成配离子(结构如图乙所示),乙二胺分子中氮原子的杂化类型为
溶液可形成配离子(结构如图乙所示),乙二胺分子中氮原子的杂化类型为_______ 。
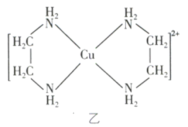
乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是_______ 。
 是几种常见的非金属元素,其形成的各种化合物在自然界中广泛存在。
是几种常见的非金属元素,其形成的各种化合物在自然界中广泛存在。(1)基态硅原子的电子排布式为
(2)
 与一定量的水可形成如图甲所示晶体R。
与一定量的水可形成如图甲所示晶体R。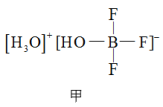
①晶体R中各种微粒间的作用力涉及
a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
②晶体R中阴离子的空间结构为
(3)乙二胺(
 )与
)与 溶液可形成配离子(结构如图乙所示),乙二胺分子中氮原子的杂化类型为
溶液可形成配离子(结构如图乙所示),乙二胺分子中氮原子的杂化类型为
乙二胺和三甲胺
 均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】将少量 粉末溶于盛有水的试管中得到一种天蓝色溶液,现进行以下实验:①向试管中滴加氨水,先形成蓝色沉淀;②继续滴加氨水,沉淀溶解,得到深蓝色溶液;③再加入乙醇溶剂,将析出深蓝色的晶体。
粉末溶于盛有水的试管中得到一种天蓝色溶液,现进行以下实验:①向试管中滴加氨水,先形成蓝色沉淀;②继续滴加氨水,沉淀溶解,得到深蓝色溶液;③再加入乙醇溶剂,将析出深蓝色的晶体。
(1)溶液中呈天蓝色微粒的化学式为_______ ,1mol②中深蓝色微粒所含的 键数目为
键数目为_______ 。
(2)写出②的离子方程式_______ 。
(3)③中析出的深蓝色晶体为 ,该物质的名称为
,该物质的名称为_______ 。
(4)生活中用来制银镜的银氨溶液也是配合物,制备银氨溶液的方法是向_______ 中滴加_______ (写物质名称),该过程的总反应的离子方程式为_______ 。
(5)检验 的最优方法的离子方程式为
的最优方法的离子方程式为_______ 。
 粉末溶于盛有水的试管中得到一种天蓝色溶液,现进行以下实验:①向试管中滴加氨水,先形成蓝色沉淀;②继续滴加氨水,沉淀溶解,得到深蓝色溶液;③再加入乙醇溶剂,将析出深蓝色的晶体。
粉末溶于盛有水的试管中得到一种天蓝色溶液,现进行以下实验:①向试管中滴加氨水,先形成蓝色沉淀;②继续滴加氨水,沉淀溶解,得到深蓝色溶液;③再加入乙醇溶剂,将析出深蓝色的晶体。(1)溶液中呈天蓝色微粒的化学式为
 键数目为
键数目为(2)写出②的离子方程式
(3)③中析出的深蓝色晶体为
 ,该物质的名称为
,该物质的名称为(4)生活中用来制银镜的银氨溶液也是配合物,制备银氨溶液的方法是向
(5)检验
 的最优方法的离子方程式为
的最优方法的离子方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)比较得电子能力的相对强弱:
_______ (填“>”“<”或“=”) ;用一个化学方程式说明
;用一个化学方程式说明 和
和 得电子能力的相对强弱:
得电子能力的相对强弱:_______ 。
(2)液态 中存在分子缔合现象,原因是
中存在分子缔合现象,原因是_______ 。

 ;用一个化学方程式说明
;用一个化学方程式说明 和
和 得电子能力的相对强弱:
得电子能力的相对强弱:(2)液态
 中存在分子缔合现象,原因是
中存在分子缔合现象,原因是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器中得到广泛应用。 的键角为
的键角为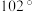 ,其沸点为
,其沸点为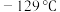 ,可在铜的催化作用U下由
,可在铜的催化作用U下由 和过量
和过量 反应得到。
反应得到。
(1)根据VSEPR理论计算可知。 的理想模型为
的理想模型为___________ 形,实际为___________ 形。
(2) 的沸点比
的沸点比 的点(
的点(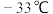 )低得多的主要原因是
)低得多的主要原因是___________ 。
(3)简述 的键角为
的键角为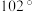 而不是
而不是 的原因
的原因___________ 。
 的键角为
的键角为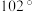 ,其沸点为
,其沸点为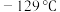 ,可在铜的催化作用U下由
,可在铜的催化作用U下由 和过量
和过量 反应得到。
反应得到。(1)根据VSEPR理论计算可知。
 的理想模型为
的理想模型为(2)
 的沸点比
的沸点比 的点(
的点(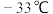 )低得多的主要原因是
)低得多的主要原因是(3)简述
 的键角为
的键角为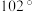 而不是
而不是 的原因
的原因
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】乙硫醇(C2H5SH)和乙醇(C2H5OH)结构相似,乙硫醇是无色透明易挥发的高毒油状液体,以具有强烈、持久且具刺激性的蒜臭味而闻名(比硫化氢H2S更甚);微溶于水,具有弱酸性,易溶于碱液和有机溶剂中。回答下列问题:
(1)乙硫醇是_______ (填“极性”或“非极性”)分子。
(2)乙硫醇比乙醇的水溶性差的原因为_______ 。
(3)乙硫醇的沸点比乙醇(C2H5OH)的沸点_______ (填“高”或“低”),主要原因为:_______ 。
(4)乙硫醇的酸性比H2S弱,比乙醇强,是因为乙基是给电子(推电子)基团,乙硫醇中硫原子的电子密度比H2S中里硫原子_______ (填“高”或“低”),对质子氢的吸引力强,写出乙硫醇和NaOH溶液反应的离子方程方式:_______ 。
(1)乙硫醇是
(2)乙硫醇比乙醇的水溶性差的原因为
(3)乙硫醇的沸点比乙醇(C2H5OH)的沸点
(4)乙硫醇的酸性比H2S弱,比乙醇强,是因为乙基是给电子(推电子)基团,乙硫醇中硫原子的电子密度比H2S中里硫原子
您最近半年使用:0次

 与NO反应生成的
与NO反应生成的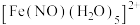 中,NO以N原子与
中,NO以N原子与 形成配位键。请在
形成配位键。请在
 蓝色溶液。在
蓝色溶液。在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为 中
中 与
与 的C原子形成配位键。不考虑空间结构,
的C原子形成配位键。不考虑空间结构,

