2014高三·全国·专题练习
名校
1 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用,请回答下列问题:
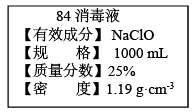
(1)该“84消毒液”的物质的量浓度约为___ mol·L-1。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___ mol·L-1。
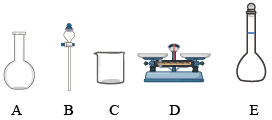
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是___ (填字母)。
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g·cm-3)的浓硫酸配制2L2.3mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为___ mol·L-1;
②需用浓硫酸的体积为____ mL。

(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是

| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| D.需要称量NaClO固体的质量为143.0g |
①所配制的稀硫酸中,H+的物质的量浓度为
②需用浓硫酸的体积为
您最近一年使用:0次
2021-09-16更新
|
652次组卷
|
24卷引用:第一章章末检测(2)——《高中新教材同步备课》(鲁科版 必修第一册)
(已下线)第一章章末检测(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)2014年高考化学苏教版一轮复习1-2-2溶液的配制及误差分析练习卷2015-2016学年北大附中河南分校高一上9月考化学试卷2017届福建省南安一中高三暑假阶段性考试化学试卷河南省安阳县第一高级中学2017-2018学年高一上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第2讲 物质的量浓度及一定物质的量浓度溶液的配制【押题专练】吉林省长春市九台区师范高级中学2018-2019学年高一上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第2讲 物质的量在化学实验中的应用( 题型专练)(已下线)2018年12月22日 《每日一题》人教必修1- 周末培优河北省大名县第一中学2018-2019学年高二(普通班)5月月考化学试题第一章章末检测(1)——《高中新教材同步备课》(鲁科版 必修第一册)河北省辛集中学2019-2020学年高一上学期第一次月考(理)化学试题山东省东明县第一中学2019-2020学年高一上学期第一次月考化学试题(已下线)第04讲 一定物质的量浓度的溶液及其配制(精练)——2021年高考化学一轮复习讲练测(已下线)第02章 海水中的重要元素——钠和氯(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)河南省郑州市第一中学2020-2021学年高一上学期第一次月考化学试题黑龙江省大庆中学2020—2021学年高一下学期开学考试化学试题(已下线)第02讲 物质的量浓度与溶液的配制(精练)-2022年高考化学一轮复习讲练测(已下线)第02讲 物质的量浓度(练)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第02讲 物质的量浓度与溶液的配制(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题二 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省黑河市第九中学2022-2023学年高三上学期摸底考试化学试题湖南省衡阳县四中2022-2023学年高一上学期开学摸底考试化学试题(B卷)山东省曹县第一中学2023-2024学年高一上学期10月月考化学试题
解答题-实验探究题
|
较易(0.85)
|
名校
解题方法
2 . 要配制480mL 0.2mol·L-1的FeSO4溶液,配制过程中有如下操作步骤:
①把称量好的绿矾(FeSO4·7H2O)放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入___________ 中;
③继续向容量瓶中加蒸馏水至液面距离刻度l~2cm处,改用___________ 滴加蒸馏水至液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,反复上下颠倒,摇匀; ⑥待溶液恢复到室温。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号)___________ ,完成此配制实验,除了量筒、烧杯、玻璃棒外还需要的常见的玻璃仪器有___________ 。
(2)实验室用绿矾(FeSO4·7H2O)来配制该溶液,用托盘天平称量绿矾___________ g。
(3)由于错误操作,使得实际浓度比所要求的偏小的是___________ (填写编号)。
A.称量绿矾时,左码右物
B.使用容量瓶配制溶液时,俯视液面定容,
C.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有干燥
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
(4)定容时,若加蒸馏水时不慎超过刻度线,处理方法是___________
①把称量好的绿矾(FeSO4·7H2O)放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入
③继续向容量瓶中加蒸馏水至液面距离刻度l~2cm处,改用
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞紧,反复上下颠倒,摇匀; ⑥待溶液恢复到室温。
请填写下列空白:
(1)实验操作步骤的正确顺序为(填序号)
(2)实验室用绿矾(FeSO4·7H2O)来配制该溶液,用托盘天平称量绿矾
(3)由于错误操作,使得实际浓度比所要求的偏小的是
A.称量绿矾时,左码右物
B.使用容量瓶配制溶液时,俯视液面定容,
C.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有干燥
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
(4)定容时,若加蒸馏水时不慎超过刻度线,处理方法是
您最近一年使用:0次
2021-07-28更新
|
1653次组卷
|
8卷引用:内蒙古杭锦后旗奋斗中学2020-2021学年高一上学期期中考试化学试题
内蒙古杭锦后旗奋斗中学2020-2021学年高一上学期期中考试化学试题(已下线)2.3.3 物质的量浓度-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)专题2.3.4 配制一定物质的量浓度的溶液(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)必考点10 以物质的量为中心的化学计算-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)(已下线)第二章 海水中的重要元素——钠和氯(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)江苏省扬州中学2022-2023学年高一上学期期中检测化学试题河南省潢川第一中学2022-2023学年高一上学期期末考试化学试题河北省唐县第一中学2023-2024学年高一上学期开学考试化学试题
名校
解题方法
3 . 用质量分数为36.5%的盐酸(密度为1.16g·cm-3)配制1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为_____ mL的容量瓶。
(2)计算已知盐酸的物质的量浓度为__________ 。
(3)经计算需要_____ mL浓盐酸,在量取时宜选用下列量筒中的________ 。
A 5mL B 10mL C 25mL D 50mL
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入相应规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是__________ (填序号)。
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是______ (填“偏高”、“偏低”或“无影响”).若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是______ (填“偏高”、“偏低”或“无影响”)。
(1)配制稀盐酸时,应选用容量为
(2)计算已知盐酸的物质的量浓度为
(3)经计算需要
A 5mL B 10mL C 25mL D 50mL
(4)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入相应规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(5)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是
您最近一年使用:0次
2020-11-25更新
|
574次组卷
|
11卷引用:人教版(2019)高一必修第一册第二章 海水中的重要元素 素养拓展区
人教版(2019)高一必修第一册第二章 海水中的重要元素 素养拓展区【全国百强校】安徽省合肥市第六中学2018-2019学年高一上学期第一次段考化学试题安徽省合肥市第六中学2018-2019学年高二上学期第一次段考化学试题新疆维吾尔自治区喀什地区二中2019届高三上学期9月月考化学试题1新疆维吾尔自治区喀什地区二中2019届高三上学期9月月考化学试题2浙江省温州市求知中学2018-2019学年高一下学期第二次月考化学试题黑龙江省哈尔滨市第一中学2019-2020 学年高二下学期期末考试化学试题四川省攀枝花市第十五中学2019-2020学年高一上学期第一次月考化学试题江西省南昌市八一中学、麻丘高级中学等六校2020-2021学年高一上学期期中联考化学试题(已下线)【南昌新东方】10. 2020 高一上 洪八联考 晏梓超河南省濮阳市第一高级中学2021-2022学年高一上学期第二次质量检测化学试题
名校
解题方法
4 . 下列有关溶液配制说法错误的是( )
| A.称取12.5g胆矾[CuSO4·5H2O]溶于水中,并加水稀释至500mL,所得溶液物质的量浓度为0.1mol•L-1 |
| B.取58.5gNaCl固体放入1L水中充分溶解,所得溶液中NaCl的物质的量浓度为1mol·L-1 |
| C.将100g5%的食盐水加热蒸发掉50g水后(没有晶体析出),所得溶液中NaCl的质量分数为10% |
| D.将浓度为2mol•L-1硫酸钠溶液10mL加水稀释至200mL,所得溶液浓度为0.1mol•L-1 |
您最近一年使用:0次
2020-11-17更新
|
756次组卷
|
13卷引用:苏教版(2020)高一必修第一册专题2 第二单元 溶液组成的定量研究
苏教版(2020)高一必修第一册专题2 第二单元 溶液组成的定量研究人教版(2019)高一必修第一册 第二章 第三节课时3 物质的量浓度鲁科版(2019)高一必修第一册第1章 认识化学科学 第3节 物质的量 课时3 物质的量浓度(已下线)2010年福建省厦门六中高一上学期期中考试化学试卷黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高一上学期10月考试化学试题湖南省双峰县第一中学2018-2019学年高一上学期第一次月考化学试题陕西省西安中学2019-2020学年高一上学期期末考试化学试题云南省玉溪第一中学2019-2020学年高一上学期期末考试化学试题内蒙古赤峰二中2020-2021学年高一上学期第一次月考化学试题山东省新泰第一中学老校区(新泰中学)2020-2021学年高一上学期期中考试化学试题贵州省贵阳市清镇养正学校2019-2020学年高一上学期期中考试化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期期中线上考试化学试题云南省红河哈尼族彝族自治州蒙自市第一高级中学2023-2024学年高一上学期12月月考化学试题
解题方法
5 . 利用碳酸钠晶体(Na2CO3∙10H2O,相对分子质量为286)来配制0.1 mol∙L−1的碳酸钠溶液980mL,假如其他操作均准确无误,下列情况会引起所配溶液的浓度偏大的是( )
| A.称取碳酸钠晶体28.6g |
| B.定容时俯视刻度线 |
| C.转移时,对用于溶解碳酸钠晶体的烧杯没有进行洗涤 |
| D.定容后,摇匀、静置,发现液面低于刻度线,又加入少量蒸馏水至刻度线 |
您最近一年使用:0次
10-11高一上·江苏南通·期中
名校
解题方法
6 . 下列说法正确的是( )
A.1L水中溶解了58.5g NaCl,该溶液的物质的量浓度为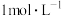 |
B.从1L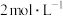 的 的 溶液中取出0.5L,该溶液的浓度为 溶液中取出0.5L,该溶液的浓度为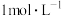 |
C.配制480mL 的 的 溶液,需称量62.5g胆矾 溶液,需称量62.5g胆矾 |
D.中和100mL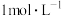 的 的 溶液,需要4g NaOH 溶液,需要4g NaOH |
您最近一年使用:0次
2020-10-07更新
|
174次组卷
|
22卷引用:2015河北保定某重点中学同步作业(必修1苏教版)1.2.3溶液的配制
(已下线)2015河北保定某重点中学同步作业(必修1苏教版)1.2.3溶液的配制高一必修第一册(苏教2019版)专题2 C 高考挑战区(已下线)2010年江苏省海安县南莫中学高一上学期期中考试化学试卷(已下线)2012-2013学年黑龙江友谊县红兴隆第一高级中学高二6月月考化学卷(已下线)2013-2014学年四川省乐山一中高一上学期期中考试化学试卷(已下线)2013-2014江西省南昌市八一中学高二下学期期末考试化学试卷2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷2016届河南省宜阳县实验学校高三第二次月考化学试卷2016届江西省上高县第二中学高三上学期第二次月考化学试卷2015-2016学年黑龙江哈尔滨六中高一上期中测试化学试卷河北省深州中学2016-2017学年高一下学期期末考试化学试题云南省大理市下关一中2017-2018学年高一上学期期中考试化学试题江西省上饶市广丰区2017-2018学年高一上学期期中考试卷化学江西省会昌中学2018-2019学年高一上学期第一次10月月考化学试题【市级联考】云南省大理市2017-2018学年高一上学期期中考试化学试题【市级联考】新疆维吾尔自治区乌鲁木齐市2018-2019学年高二下学期期末考试化学试题安徽省滁州市定远县育才学校2019-2020学年高一上学期期中考试(实验班)化学试题四川省绵阳南山中学实验学校2020-2021学年高二9月月考化学试题云南省保山市第九中学2021届高三上学期阶段测试化学试题西藏自治区日喀则市第二高级中学2020-2021学年高一上学期期中考试化学试题新疆北屯高级中学2020-2021学年高一上学期10月月考化学试题广西百色市平果县第二中学2020-2021学年高一10月月考化学试题
解题方法
7 . 已知某市售84消毒液瓶体部分标签如图所示,该84消毒液通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该84消毒液中NaClO的物质的量浓度约为___________ mol/L。(保留1位小数)
(2)84消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用98%的浓硫酸(密度为 )配制500mL 2.3mol/L的稀硫酸用于增强84消毒液的消毒能力。
)配制500mL 2.3mol/L的稀硫酸用于增强84消毒液的消毒能力。
①需用浓硫酸的体积为___________ mL。
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是___________ 。
A 溶液中 的物质的量 B 溶液的浓度
的物质的量 B 溶液的浓度
C 溶液的质量 D 溶液的密度
③配制该稀硫酸过程中,下列情况会使所配制的溶液的浓度大于2.3mol/L的有___________ 。
A 未经冷却趁热将溶液注入容量瓶中并进行定容
B 摇匀后发现液面低于刻度线,再加水至刻度线
C 容量瓶中原有少量蒸馏水
D 定容时俯视容量瓶刻度线

(1)该84消毒液中NaClO的物质的量浓度约为
(2)84消毒液与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用98%的浓硫酸(密度为
 )配制500mL 2.3mol/L的稀硫酸用于增强84消毒液的消毒能力。
)配制500mL 2.3mol/L的稀硫酸用于增强84消毒液的消毒能力。①需用浓硫酸的体积为
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是
A 溶液中
 的物质的量 B 溶液的浓度
的物质的量 B 溶液的浓度C 溶液的质量 D 溶液的密度
③配制该稀硫酸过程中,下列情况会使所配制的溶液的浓度大于2.3mol/L的有
A 未经冷却趁热将溶液注入容量瓶中并进行定容
B 摇匀后发现液面低于刻度线,再加水至刻度线
C 容量瓶中原有少量蒸馏水
D 定容时俯视容量瓶刻度线
您最近一年使用:0次
解题方法
8 . 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。下列说法正确的是
| 硫酸化学纯(CP)(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
| A.该硫酸的物质的量浓度为9.2mol/L |
| B.该硫酸与等体积的水混合所得溶液的质量分数为49% |
| C.配制250mL 4.6mol/L的稀硫酸需取该硫酸62.5mL |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2mol/L |
您最近一年使用:0次
解题方法
9 . 如图是某校实验室从化学试剂商店买回的硫酸试剂瓶上的标签。下列说法正确的是
| 硫酸 化学纯(CP)(500mL) 品名:硫酸溶液 化学式:  相对分子质量:98 密度:  质量分数:98% |
A.配制250 mL 4.6 稀硫酸需取该硫酸溶液的体积为62.5mL 稀硫酸需取该硫酸溶液的体积为62.5mL |
B.配制250 mL 4.6 稀硫酸时,向该硫酸溶液中加蒸馏水直到溶液体积为250mL 稀硫酸时,向该硫酸溶液中加蒸馏水直到溶液体积为250mL |
C.该硫酸溶液中溶质的物质的量浓度为 |
D.等质量的蒸馏水与该硫酸溶液混合所得溶液中溶质的物质的量浓度大于 |
您最近一年使用:0次
解题方法
10 . 某学校实验室从化学试剂商店买回浓度为 浓硫酸。现用该浓硫酸配制
浓硫酸。现用该浓硫酸配制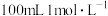 稀硫酸。可供选用的仪器有:
稀硫酸。可供选用的仪器有:
①胶头滴管;②烧瓶;③玻璃棒;④药匙;⑤量筒;⑥托盘天平;⑦试剂瓶。
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有___________ (填序号),还缺少的仪器有__________ (填仪器名称)。
(2)配制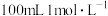 稀硫酸,需要用量筒量取上述浓硫酸的体积为
稀硫酸,需要用量筒量取上述浓硫酸的体积为_____ mL(保留一位小数),量取浓硫酸时应选用__________ (填“10mL”“50mL”或“100mL”)的量筒。
(3)向容量瓶中转移溶液及加蒸馏水定容时,玻璃棒下端应靠在容量瓶刻度线____________ (填“上方”或“下方”)的内壁上。
(4)关于容量瓶的四种叙述:①容量瓶是配制准确浓度溶液的仪器;②可以长期贮存溶液;③不能加热;④使用之前要检查是否漏水。上述叙述正确的是____________ (填字母)。
A.①②③ B.②③ C.①③④ D.②③④
 浓硫酸。现用该浓硫酸配制
浓硫酸。现用该浓硫酸配制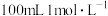 稀硫酸。可供选用的仪器有:
稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③玻璃棒;④药匙;⑤量筒;⑥托盘天平;⑦试剂瓶。
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有
(2)配制
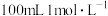 稀硫酸,需要用量筒量取上述浓硫酸的体积为
稀硫酸,需要用量筒量取上述浓硫酸的体积为(3)向容量瓶中转移溶液及加蒸馏水定容时,玻璃棒下端应靠在容量瓶刻度线
(4)关于容量瓶的四种叙述:①容量瓶是配制准确浓度溶液的仪器;②可以长期贮存溶液;③不能加热;④使用之前要检查是否漏水。上述叙述正确的是
A.①②③ B.②③ C.①③④ D.②③④
您最近一年使用:0次



