1 . 海水资源开发利用的部分过程如图所示。
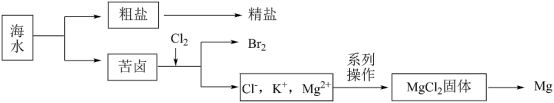
(1)向苦卤中通入Cl2制备溴的离子方程式为:___________ 。
(2)从MgCl2制取金属Mg,工业上常用___________ 方法。
(3)粗盐中含的杂质离子有Ca2+、Mg2+、SO ,提纯过程中加入试剂的顺序不正确的是
,提纯过程中加入试剂的顺序不正确的是___________
A.NaOH、BaCl2、Na2CO3、盐酸 B.BaCl2、NaOH、Na2CO3、盐酸
C.Na2CO3、BaCl2、NaOH、盐酸 D.Ba(OH)2、Na2CO3、盐酸
实验过程中,验证SO 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是___________ 。
(4)加入Na2CO3溶液时发生的离子方程式为___________ 。
(5)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和___________ 。
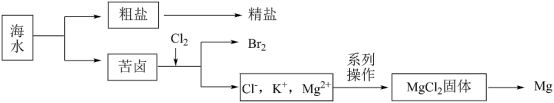
(1)向苦卤中通入Cl2制备溴的离子方程式为:
(2)从MgCl2制取金属Mg,工业上常用
(3)粗盐中含的杂质离子有Ca2+、Mg2+、SO
 ,提纯过程中加入试剂的顺序不正确的是
,提纯过程中加入试剂的顺序不正确的是A.NaOH、BaCl2、Na2CO3、盐酸 B.BaCl2、NaOH、Na2CO3、盐酸
C.Na2CO3、BaCl2、NaOH、盐酸 D.Ba(OH)2、Na2CO3、盐酸
实验过程中,验证SO
 已完全沉淀的简单操作及现象是
已完全沉淀的简单操作及现象是(4)加入Na2CO3溶液时发生的离子方程式为
(5)从除杂后的氯化钠溶液中获得NaCl固体需要的仪器有铁架台(带铁圈)、酒精灯和
您最近一年使用:0次
名校
解题方法
2 . 提纯下列物质(括号内为少量杂质),能达到目的的是
| 选项 | 混合物 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| B | 苯(苯酚) | 浓溴水 | 过滤 |
| C | 溴苯(溴) | Na2SO3溶液 | 分液 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-31更新
|
617次组卷
|
5卷引用:重庆市主城区六校2020-2021学年高二下学期期末联考化学试题
名校
3 . 已知硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O,其摩尔质量为392g·mol-1]可用作净水剂、颜料、媒染剂、鞣革、防腐剂等,它在空气中不及硫酸亚铁容易被氧化,易溶于水,不溶于乙醇。回答下列问题:
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和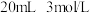 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是___________ ;由于加入的铁粉不纯,反应过程中会产生少量H2S,可以用CuSO4溶液进行吸收处理,发生的反应化学方程式为:___________ 。
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是___________ (用离子方程式表示),过滤后的硫酸亚铁铵晶体最好用___________ 洗涤;
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。
(3)滴定过程中高锰酸钾溶液应装在___________ 仪器中(填“A”或“B”);
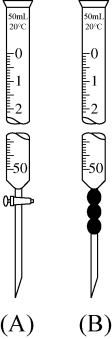
(4)滴定终点的现象是___________ ;
(5)若进行平行滴定三次,消耗 溶液的体积如下表所示:
溶液的体积如下表所示:
则制得的硫酸亚铁铵晶体纯度(质量分数)为___________ (用百分数表示,保留小数点后两位);
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
I.制备过程
步骤1:制备硫酸亚铁溶液:将5.6g铁粉和
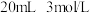 硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。
硫酸置于锥形瓶中,水浴加热至几乎不产生气泡,趁热过滤掉残余的少量铁粉。步骤2:获得硫酸亚铁铵晶体:向滤液中加入一定量的硫酸铵溶液,然后蒸发浓缩、冷却结晶、过滤、洗涤、晾干。
(1)步骤1中,加入过量铁粉的目的是
(2)步骤2中,所用到的硫酸铵溶液呈酸性,原因是
II.定量分析——氧化还原滴定法
称取20.00g制得的硫酸亚铁铵晶体溶于稀硫酸,加水配制成100mL溶液,取25.00mL于锥形瓶中,然后用
 的酸性高锰酸钾溶液进行滴定。
的酸性高锰酸钾溶液进行滴定。(3)滴定过程中高锰酸钾溶液应装在

(4)滴定终点的现象是
(5)若进行平行滴定三次,消耗
 溶液的体积如下表所示:
溶液的体积如下表所示:| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液的体积/ 溶液的体积/ | 24.54 | 24.01 | 23.99 |
(6)上表中第一次的数据明显大于后两次的数据,其原因可能是___________;
| A.第一次滴定用的锥形瓶用待测液润洗过 |
| B.第一次滴定过程中高锰酸钾溶液滴出锥形瓶外 |
| C.第一次滴定前滴定管尖嘴无气泡,滴定后有气泡 |
| D.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积 |
您最近一年使用:0次
2022-03-25更新
|
111次组卷
|
2卷引用:重庆市主城区六校2021-2022学年高二上学期期末联考化学试题
4 . 下列叙述正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 通入适量 |
| B |  | HCl | 通入浓硫酸中 |
| C |  |  | 加入 溶液并过滤 溶液并过滤 |
| D | Fe | Al | 加入过量 溶液并过滤 溶液并过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-24更新
|
155次组卷
|
2卷引用:重庆市2021-2022学年高一上学期期末联合检测化学试题
名校
解题方法
5 . 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去Al2O3中的Fe2O3 | 向固体中先加入过量NaOH溶液,过滤后向滤液中加入过量盐酸 |
| B | 证明溶液中无NH | 向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置于试管口试纸不变蓝 |
| C | 证明二氧化硫具有还原性 | 将二氧化硫通入Ba(NO3)2溶液中,有白色沉淀生成 |
| D | 验证:Ksp(AgI)<Ksp(AgCl) | 向盛有1mL0.1mol·L-1AgNO3溶液的试管中滴加2滴0.1mol·L-1NaCl溶液,有白色沉淀生成,向其中继续滴加0.1mol·L-1KI溶液,有黄色沉淀产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-18更新
|
368次组卷
|
3卷引用:重庆市南开中学校2021-2022学年高二上学期期末考试化学试题
名校
解题方法
6 . 下列实验符合操作要求且能达到实验目的的是
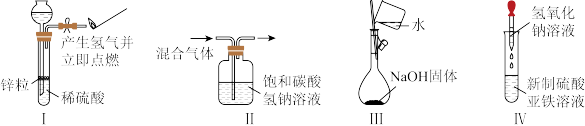

| A.I可用于制备并检验氢气的可燃性 |
| B.II可用于除去CO2中的HCl |
| C.用Ⅲ来配制一定物质的量浓度的NaOH溶液 |
| D.用IV中操作可制备长久稳定的氢氧化亚铁 |
您最近一年使用:0次
2021-08-06更新
|
690次组卷
|
23卷引用:重庆市部分区2019-2020学年高一上学期期末考试化学试题
重庆市部分区2019-2020学年高一上学期期末考试化学试题重庆市南开中学2020-2021学年高一上学期期末考试化学试题安徽省滁州市2017-2018学年高一上学期期末考试化学试题新疆沙湾一中2019-2020学年高一上学期期末考试化学试题福建省泉州市2019-2020学年高一上学期教学质量跟踪监测化学试题天津市东丽区2020-2021学年高一上学期期末考试化学试题重庆市第七中学校2021-2022高一上学期第四次月检测化学试题新疆兵团第三师图木舒克市2021-2022学年高一上学期期末考试化学试题吉林省永吉县第四中学2022-2023学年高一上学期期末考试化学试题四川省成都市天府实外2023-2024学年高一上化学期末复习试题 2015-2016学年山东省郯城县第一中学高一上学期12月月考化学试卷湖南师范大学附属中学2017-2018学年高一上学期第二次阶段性检测化学试题山东省济南市第二中学2018-2019学年高一第一学期期中考试化学试题甘肃省张掖市山丹县第一中学2019-2020学年高一11月月考化学试题宁夏石嘴山市第三中学2019-2020学年高一上学期第二次(12月)月考化学试题宁夏回族自治区石嘴山市平罗中学2019-2020学年高一上学期第三次月考化学试题河北省鸡泽县第一中学2019-2020学年高二下学期开学考试化学试题河北省曲周县第五中学2019-2020学年高二下学期5月考试化学试题江西省赣州市会昌县第五中学2020-2021学年高一上学期第二次月考化学试题江西省铜鼓中学2020-2021学年高二上学期开学考(非实验班)化学试题(已下线)2.2.1 物质的量浓度-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)浙江省湖州市三贤联盟2021-2022学年高一上学期期中考试化学试题浙江省宁波金兰合作组织2022-2023学年高一上学期期中联考化学试题
名校
解题方法
7 . 为提纯下列物质 (括号内的物质是杂质), 所选用的除杂试剂和分离方法都正确的是
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴化钠溶液 (NaI) | 溴水、CCl4 | 萃取、分液 |
| B | 氯化铵溶液(FeCl3) | 氢氧化钠溶液 | 过滤 |
| C | 二氧化氮 (NO) | O2 | |
| D | 水[Al(OH)3胶体] | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 为提纯下列物质(括号内为杂质,不考虑引入的水蒸气),有关除杂试剂和分离方法的选择不正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | CH3CH3(CH2=CH2) | 溴水 | 洗气 |
| B | CH3CH2Br(Br2) | NaOH溶液 | 分液 |
| C | 溴苯(苯) | 蒸馏 | |
| D | 乙烯(乙醇蒸气) | 水 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 已知粗盐中含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,先将粗盐溶于水后,再通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液,②加入稍过量的NaOH溶液,③加入稍过量的BaCl2 溶液,④滴入稀盐酸至溶液呈中性,⑤过滤。正确的操作顺序是
| A.②①③⑤④ | B.③②①⑤④ | C.②③①④⑤ | D.③⑤②①④ |
您最近一年使用:0次
14-15高三上·四川广安·阶段练习
名校
解题方法
10 . 为除去某物质中所含的杂质,所选用的试剂及操作方法正确的是( )
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 滴入稀盐酸,同时用pH计测定至溶液呈中性 |
| ② | FeSO4溶液 | CuSO4 | 加入足量还原铁粉充分搅拌,然后过滤 |
| ③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | Na2SO4 | CaCO3 | 溶解、过滤、蒸发结晶 |
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
您最近一年使用:0次
2019-12-02更新
|
406次组卷
|
4卷引用:重庆市巴蜀中学2019-2020学年高一上学期期末考试化学试题
重庆市巴蜀中学2019-2020学年高一上学期期末考试化学试题(已下线)2015届四川省武胜中学高三(补习班)10月月考理综化学试卷华南师范大学附中2019-2020学年高一上学期期中考试化学试题(已下线)【南昌新东方】9. 南昌十九中 刘惠文.



