9. 2030年“碳达峰”、2060年实现“碳中和”的国际承诺使CO
2的回收及综合利用越来越受到我国科学家的重视。请根据如下信息回答相应问题:
(1)若用CO
2和H
2制取甲醇,反应的能量变化如下图所示:

根据上图可知用CO
2和H
2制取甲醇的热化学方程式为
_______。
(2)在2L恒容密闭容器中分别投入2molCO
2和6molH
2制取甲醇。温度一定时(水为气态),下列说法能说明该反应达到平衡状态的是_______。
| A.混合气体的密度不再改变 | B.混合气体的压强不再改变 |
C. (CO2)=2 (CO2)=2 (H2) (H2) | D.CO2 和H2的物质的量之比不再改变 |
(3)在2L恒容密闭容器a和b中分别投入2molCO
2和6molH
2,在不同温度下(水为气态)制取甲醇,各容器中甲醇的物质的量与时间的关系如下图所示。

①T
a _______ T
b (填“>”“<”或“=”)。若其他条件不变,改变一个条件反应由曲线b变为曲线c,则改变的条件是
_______。
②容器b中0~10 min氢气的平均反应速率v(H
2)为
_______mol·L
-1·min。 用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数。该反应达到平衡时体系的总压强为p,则容器b中反应平衡常数Kp=
_______ (用含 p的计算式表示,不必化简)。
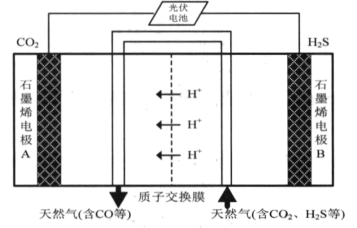
(4)一种利用光电驱动协同转化去除H
2S和CO
2的装置如图所示,石墨烯电极A的电极反应式为
_______。