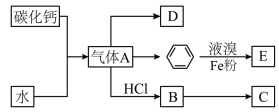
氯苯是染料、医药工业生产中的一种重要原料。实验室中制备氯苯的装置如图所示(其中夹持仪器已略去),其原理是苯与氯气在催化剂作用下生成氯苯,同时会有少量苯发生副反应生成二氯苯。苯及其生成物沸点如表所示:
请回答下列问题:
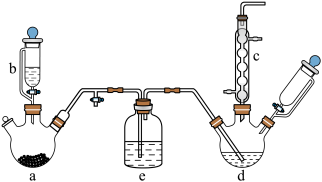
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器b中活塞,使浓盐酸缓缓滴下,仪器a中发生反应时,氧化剂与还原剂的物质的量之比为_______ 。
(2)仪器b中侧管的作用是_______ 。仪器c的名称是_______ 。
(3)仪器e中盛装试剂的作用是_______ 。
(4)仪器d中盛有苯、FeCl3 粉末,仪器a中生成的气体经过仪器e进入仪器d中,d中主要反应的化学方程式为_______ 。
(5)该方法制备的氯苯中含有很多杂质。可通过如下流程提纯氯苯:氯苯混合物

 纯净氯苯
纯净氯苯
①水洗并分液可除去HCl、部分Cl2和_______ (填化学式) ;
②碱洗前先进行水洗的目的是_______ ;
③最后一步分离出纯净氯苯的方法是_______ 。
(6)工业生产中使用1t苯可制得1.35t氯苯,则氯苯的产率为_______ 。

| 有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
| 沸点/℃ | 80.0 | 132.2 | 180.4 | 172.0 | 173.4 |
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸。打开仪器b中活塞,使浓盐酸缓缓滴下,仪器a中发生反应时,氧化剂与还原剂的物质的量之比为
(2)仪器b中侧管的作用是
(3)仪器e中盛装试剂的作用是
(4)仪器d中盛有苯、FeCl3 粉末,仪器a中生成的气体经过仪器e进入仪器d中,d中主要反应的化学方程式为
(5)该方法制备的氯苯中含有很多杂质。可通过如下流程提纯氯苯:氯苯混合物


 纯净氯苯
纯净氯苯①水洗并分液可除去HCl、部分Cl2和
②碱洗前先进行水洗的目的是
③最后一步分离出纯净氯苯的方法是
(6)工业生产中使用1t苯可制得1.35t氯苯,则氯苯的产率为
更新时间:2021-10-18 20:38:17
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图所示装置模拟工业制取及收集ClO2。(夹持仪器已省略)。回答问题:

(1)B必须添加温度控制装置,应补充的装置是__________________ ;A也必须添加温度控制装置,除酒精灯外,还需要的仪器是_______________ (不须填夹持仪器)。
(2)C中试剂为__________ 。C装置有缺陷需改进,在答题卡上画出改进的C装置。________
(3)A中反应产物有某种盐、ClO2和CO2等,写出相关化学方程式_________ 。

(1)B必须添加温度控制装置,应补充的装置是
(2)C中试剂为
(3)A中反应产物有某种盐、ClO2和CO2等,写出相关化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】如图中,A是氯气的发生装置,B、C是净化气体的装置,B装置中装有饱和食盐水,D中装铁丝网;反应后E的底部有棕色固体聚集;F是碱液用于吸收多余气体的装置。

(1)上述装置中有一处错误,请指出是___ 处(用字母表示)。
(2)B装置的作用是___ ,C装置中需要加入___ 。
(3)写出A中发生反应的化学方程式___ 。
(4)如果A中产生氯气2.24L(标准状况),则被氧化的HCl的物质的量为___ 。

(1)上述装置中有一处错误,请指出是
(2)B装置的作用是
(3)写出A中发生反应的化学方程式
(4)如果A中产生氯气2.24L(标准状况),则被氧化的HCl的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置Ⅰ中仪器c的名称是___________ 。写出舍勒发现的,至今仍应用于实验室制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
① ②
②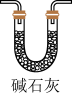 ③
③ ④
④ 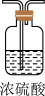
(5)有一种“地康法”制取氯气的反应原理如图所示:
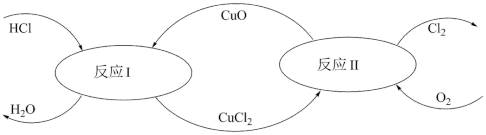
①反应Ⅰ属于___________ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为___________ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④ 
(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式_______ ,B分子式______ 。
(2)与A相邻的同系物C发生加聚反应生成有机高分子材料的反应的化学反应方程式:_______ 。
(3)在碘水中加入B振荡静置后的现象_______ 。
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_______ ,反应类型:________ 。
(5)等质量的A、B完全燃烧时消耗O2的物质的量多的是_______ (填分子名称)
(6)已知乙烯能发生以下转化:

①写出B与D反应的化学方程式_________ ;反应类型:________ 。
②写出反应②的化学方程式:________
(1)A的结构简式
(2)与A相邻的同系物C发生加聚反应生成有机高分子材料的反应的化学反应方程式:
(3)在碘水中加入B振荡静置后的现象
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:
(5)等质量的A、B完全燃烧时消耗O2的物质的量多的是
(6)已知乙烯能发生以下转化:

①写出B与D反应的化学方程式
②写出反应②的化学方程式:
您最近一年使用:0次
【推荐2】工业中很多重要的化工原料都来源于石油化工,如图中的苯、丙烯、有机物A等,其中A的年产量可以用来衡量一个国家的石油化工发展水平。请回答下列问题:

(1)A的结构简式为_______ ,丙烯酸中含氧官能团的名称为______ ;
(2)写出下列反应的反应类型①________ ,④________ ;
(3)下列说法正确的是:________ ;
A.为除去硝基苯中混有的浓HNO3和H2SO4,可将其倒入到NaOH溶液中,静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.有机物C与丙烯酸属于同系物
(4)写出④的反应方程式:__________ 。

(1)A的结构简式为
(2)写出下列反应的反应类型①
(3)下列说法正确的是:
A.为除去硝基苯中混有的浓HNO3和H2SO4,可将其倒入到NaOH溶液中,静置,分液
B.除去乙酸乙酯中的乙酸,加NaOH溶液、分液
C.有机物C与丙烯酸属于同系物
(4)写出④的反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】蒸馏是实验室制备蒸馏水的常用方法。
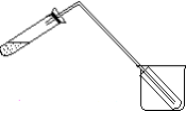
(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是__________________________ 。
(2)仪器A的名称是____________________ ,仪器B的名称是____________________________ 。
(3)实验时A中除加入少量自来水外,还需加入几粒______________ ,其作用是防止液体暴沸。
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入___________________ 和 _______________ (填试剂的化学式),检验是否存在Cl-。
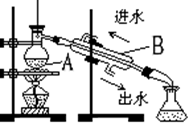
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是______________________________ ;为了提高冷凝效果,烧杯中最好盛有的物质是 ___________ (填名称)。

(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是
(2)仪器A的名称是
(3)实验时A中除加入少量自来水外,还需加入几粒
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】丙炔酸甲酯(CH≡C-COOCH3)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为CH≡C-COOH+CH3OH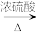 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。
实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
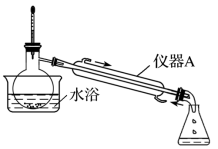
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。___________ 。
(2)步骤2中,如图所示的装置中仪器A的名称是___________ ;蒸馏烧瓶中加入碎瓷片的目的是___________ 。
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是___________ ;分离出有机相的操作名称为___________ 。
(4)步骤4中,蒸馏时不能用水浴加热的原因是___________ 。
(5)实验中丙炔酸甲酯的产率为___________ 。
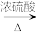 CH≡C-COOCH3+H2O。
CH≡C-COOCH3+H2O。实验步骤如下:
步骤1:在反应瓶中,加入14.00 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置如图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5% Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯10.08 g。
(2)步骤2中,如图所示的装置中仪器A的名称是
(3)步骤3中,用5% Na2CO3溶液洗涤,主要除去的物质是
(4)步骤4中,蒸馏时不能用水浴加热的原因是
(5)实验中丙炔酸甲酯的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】工业纯碱中常常含有NaCl、Na2SO4等杂质。为测定某工业纯碱的纯度,设计了如下图实验装置。

依据实验设计,请回答:
(1)装置中盛装稀硫酸的仪器名称是_________ ;装置D的作用是_________________ 。
(2)为达到测定某工业纯碱的纯度实验目的,一次实验中至少应进行称量操作的次数为__________ 。
(3)若不考虑操作、药品及其用量等方面的影响,该实验测得结果会______ 填“偏高”、“偏低”、“无影响”);原因是___________________ (你若认为无影响,该空不用回答)。

依据实验设计,请回答:
(1)装置中盛装稀硫酸的仪器名称是
(2)为达到测定某工业纯碱的纯度实验目的,一次实验中至少应进行称量操作的次数为
(3)若不考虑操作、药品及其用量等方面的影响,该实验测得结果会
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】ClNO(亚硝酰氯)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到,ClNO的熔点为−64.5℃、沸点为−5.5℃,气态呈黄色,液态时呈红褐色,遇水发生水解反应生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。回答下列问题:
Ⅰ.ClNO的制备:实验室中可用如图所示装置制备ClNO。
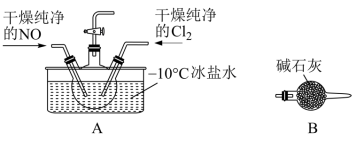
(1)装置A中−10℃冰盐水的作用是:___ 。
(2)实验开始时应先通入Cl2,让三颈瓶中充满黄绿色,再将NO缓缓通入。先通入Cl2的目的是___ ;一段时间后,两种气体在A中反应的现象为___ 。
(3)装置B除了进行尾气处理外,另一个作用是___ ,实验过程中发现即使碱石灰过量尾气也不能被完全吸收,其原因是___ 。
Ⅱ.ClNO纯度的测定:取所制备的亚硝酰氯13.10g溶于水配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用0.8 mol∙L−1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL(已知:Ag2CrO4为砖红色固体)。
(4)ClNO与水反应的化学方程式为___ 。
(5)滴定终点的实验现象为___ 。
(6)ClNO的质量分数为___ 。
Ⅰ.ClNO的制备:实验室中可用如图所示装置制备ClNO。

(1)装置A中−10℃冰盐水的作用是:
(2)实验开始时应先通入Cl2,让三颈瓶中充满黄绿色,再将NO缓缓通入。先通入Cl2的目的是
(3)装置B除了进行尾气处理外,另一个作用是
Ⅱ.ClNO纯度的测定:取所制备的亚硝酰氯13.10g溶于水配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用0.8 mol∙L−1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL(已知:Ag2CrO4为砖红色固体)。
(4)ClNO与水反应的化学方程式为
(5)滴定终点的实验现象为
(6)ClNO的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】富马酸亚铁为棕红色固体,较难溶于水,是一种治疗缺铁性贫血的安全有效的补铁制剂。某实验小组用富马酸(HOOCCH=CHCOOH)和 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:
Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入50mL热水搅拌使之溶解;
②向烧杯中加入50mL一定浓度的 溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
③通 并加热一段时间后,通过仪器a缓慢加入40mL新配置的
并加热一段时间后,通过仪器a缓慢加入40mL新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。
④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。___________ ,仪器b适宜的规格是___________ 。
A.100mL B.250mL C.500mL
(2)已知反应容器中反应物 和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的
和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的 溶液要适量,若
溶液要适量,若 溶液加入过量,溶液pH偏高,则制得产品可能含有
溶液加入过量,溶液pH偏高,则制得产品可能含有___________ (填写化学式)。
(3)合成富马酸亚铁反应的化学方程式为___________ 。
(4)采用减压过滤的优点是___________ ,步骤④检验沉淀是否洗净的试剂是___________ 。
Ⅱ.产品纯度测定
取0.510g样品置于250mL锥形瓶中,加入15.00mL稀硫酸,加热使之溶解,冷却后再加入50.00mL新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:
(5)①硫酸铈铵 溶液应装入
溶液应装入___________ (填“酸式”或“碱式”)滴定管。
②滴定终点的现象为___________ ,该滴定过程的标准液不宜为酸性高锰酸钾溶液,原因是___________ 。
③产品的纯度是___________ %(保留4位有效数字)。
 制备富马酸亚铁,并对其纯度进行测定,过程如下:
制备富马酸亚铁,并对其纯度进行测定,过程如下:Ⅰ.制备富马酸亚铁
①将少量富马酸固体置于烧杯中,加入50mL热水搅拌使之溶解;
②向烧杯中加入50mL一定浓度的
 溶液,控制pH为6.5~6.7,并将其转移到仪器b中;
溶液,控制pH为6.5~6.7,并将其转移到仪器b中;③通
 并加热一段时间后,通过仪器a缓慢加入40mL新配置的
并加热一段时间后,通过仪器a缓慢加入40mL新配置的 溶液,继续加热约1小时后,出现大量棕红色沉淀。
溶液,继续加热约1小时后,出现大量棕红色沉淀。④将反应混合液冷却后,减压过滤,洗涤,干燥,得粗产品。

A.100mL B.250mL C.500mL
(2)已知反应容器中反应物
 和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的
和富马酸按恰好完全反应的比例进行起始投料,步骤②中加入的 溶液要适量,若
溶液要适量,若 溶液加入过量,溶液pH偏高,则制得产品可能含有
溶液加入过量,溶液pH偏高,则制得产品可能含有(3)合成富马酸亚铁反应的化学方程式为
(4)采用减压过滤的优点是
Ⅱ.产品纯度测定
取0.510g样品置于250mL锥形瓶中,加入15.00mL稀硫酸,加热使之溶解,冷却后再加入50.00mL新煮沸过的冷水和2滴邻二氮菲指示剂(邻二氮菲遇
 呈红色,遇
呈红色,遇 呈无色);立即用
呈无色);立即用 硫酸铈铵
硫酸铈铵 标准液滴定(还原产物为
标准液滴定(还原产物为 ),滴定至终点。平行测定三次,消耗标准液体积如下:
),滴定至终点。平行测定三次,消耗标准液体积如下:| 第一次 | 第二次 | 第三次 |
| 19.96mL | 20.20mL | 20.04mL |
 溶液应装入
溶液应装入②滴定终点的现象为
③产品的纯度是
您最近一年使用:0次