解题方法
1 . 我国制碱工业先驱侯德榜发明了侯氏制碱法。其模拟流程如图:
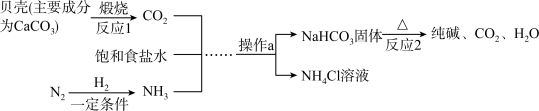
回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:________ 。
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:_________ 。
(3)进行操作a时所需的玻璃仪器有玻璃棒、________ 和________ 。
(4)NaHCO3固体受热分解的化学方程式为_______ 。
(5)现有ag质量分数为w的NH4Cl溶液(不考虑 与水发生的反应):
与水发生的反应):
①该溶液中所含溶质的总质量为________ (用含a、w的代数式表示,写出计算式即可)g。
②________ gNH3中所含的氮元素的总质量与该溶液中所含的氮元素的总质量相等。

回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:
(3)进行操作a时所需的玻璃仪器有玻璃棒、
(4)NaHCO3固体受热分解的化学方程式为
(5)现有ag质量分数为w的NH4Cl溶液(不考虑
 与水发生的反应):
与水发生的反应):①该溶液中所含溶质的总质量为
②
您最近一年使用:0次
名校
解题方法
2 . 磁性氧化铁因其特殊的超顺磁性,在巨磁电阻、磁性液体和磁记录、软磁、永磁、磁致冷、巨磁阻抗材料以及磁光器件、磁探测器等方面具有广阔的应用前景。以高硫铝土矿(主要含Al2O3、Fe2O3、SiO2和少量的FeS2等)为原料提取氧化铝和磁性氧化铁的流程如图:
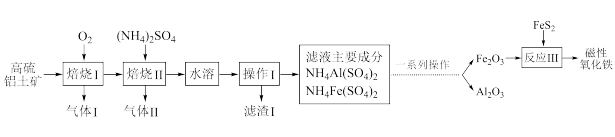
(1)磁性氧化铁的化学式为____ ;写出滤渣I中主要成分的一种用途:____ 。
(2)操作I在实验中要用到的玻璃仪器有____ 。
(3)焙烧I中,FeS2发生反应的化学方程式为____ 。
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是____ (任答一点)。

(5)焙烧II中氧化铝参与反应的化学方程式为_____ 。
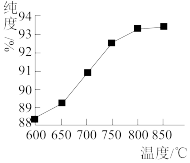
(6)反应III中加入FeS2的目的是作_____ (填“氧化剂”或“还原剂”)。反应Ⅲ的煅烧温度对磁性氧化铁的纯度有很大影响。已知温度对磁性氧化铁纯度的影响如图所示,则煅烧时,温度最好控制在____ ℃。
(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:_____ 。

(1)磁性氧化铁的化学式为
(2)操作I在实验中要用到的玻璃仪器有
(3)焙烧I中,FeS2发生反应的化学方程式为
(4)焙烧I的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(5)焙烧II中氧化铝参与反应的化学方程式为
(6)反应III中加入FeS2的目的是作

(7)滤液经过一系列操作可获得Al2O3,请简述这一系列操作的具体过程:
您最近一年使用:0次
2022-10-01更新
|
271次组卷
|
5卷引用:河北省保定市2022-2023学年高三上学期9月份考试化学试题



